
8.下列说法正确的是 ( )
A.pH=3的醋酸溶液和pH=11的Ba(OH)2溶液以等体积混合后pH=7
B.pH=3的醋酸溶液稀释10倍后pH=4
C.pH=1的稀硫酸与0.1mol/L的Ba(OH)2溶液等体积混合后pH=7
D.0.2mol/L的盐酸溶液,与水等体积混合后pH=1
7.下图是四种定量容器的一部分,在酸碱中和滴定时应该选用的是 ( )

6.下列现象或操作与盐类的水解无关的是 ( )
A.配制CuC12溶液时,要滴加少量的盐酸
B.加热蒸干并灼烧Na2SO3溶液,得到Na2SO4固体
C.明矾净水
D.氨态氮肥(含NH4)不能与草木灰混合使用
5.下列溶液中能大量共存并且溶液为无色透明的离子组是 ( )
A.A13+、Na、A1O22-、SO42- B.Cu2+、C1-、A13+、SO42-
C.K+、Ca2+、HCO3-、NO3- D.Ca2+、Na+、Fe3+、NO3-
4.往醋酸溶液中滴加稀氨水时,溶液的导电能力发生变化,其电流强度I随加入稀氨水的体积V变化曲线图为 ( )
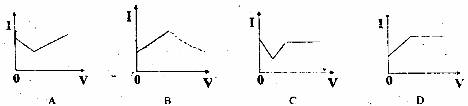
3.下列对化学反应速率和化学平衡的分析中,不正确的是 ( )
①在一密闭容器中充入1molH2和1molI2,达到平衡后,保持恒压,同其中再加入1molH2和1molI2,重新达到平衡时,反应速率增大
②已达平衡的反应N2(g)+3H2(g) 2NH3(g)△H<0,升高温度,可以同时增大反应速率和N2的转化率
③在2L密闭容器中充入2molA气体和1molB气体,在一定条件下发生反应:2A(g)+B(g) 2C(g),达到平衡时,C的浓度为0.6mol/,则A的转化率为30%
2C(g),达到平衡时,C的浓度为0.6mol/,则A的转化率为30%
④Mg、A1在相同条件下分别与0.1mol/L盐酸反应,反应速率相同
A.①② B.①②③ C.②③④ D.①②③④
2.灰锡(以粉末状存在)和白锡是锡的两种同素异形体。
已知:①Sn(s、白)+2HC1(aq)=SnC12(aq)+H2(g);△H1
② Sn(s、灰)+2HC1(aq)=SnC12(aq)+H2(g);△H2>13.2℃
③Sn(s、灰) Sn(s、白)(g);△H3=+2.1kJ/mol<13.2℃
A.△H1>△H2
B.锡在常温下以灰锡状态存在
C.灰锡转化为白锡的反应是放热反应
D.锡制器皿长期处于低于13.2℃的环境中,会自行毁坏
1.下列说法正确的是 ( )
A.工业上常采用电解熔融A1C13制备金属铝
B.汽油是纯净物,有固定的沸点
C.煤气化可以得到水煤气
D.海水提镁过程中一般采用NaOH使海水中的Mg2+沉淀
32.(10分)在一定条件下,向体积为2 L的容器中加入2 mol O2和3 mol SO2使之反应生成SO3气体:2SO2+
O2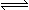 2SO3
,2 min后反应达平衡,测得O2的物质的量为1.6 mol,则:
2SO3
,2 min后反应达平衡,测得O2的物质的量为1.6 mol,则:
(1)2min内,平均反应速率v(O2)= ; v(SO3)= 。
(2)平衡时,SO2的浓度为
(3)若达平衡时测得上述反应放出Q kJ的热量,试写出该反应的热化学方程式
31.(11分)(1)某实验兴趣小组以Zn和Cu为电极,稀硫酸为电解质溶液组成原电池进行实验,实验结束后,记录如下:
①Zn为阳极,Cu为阴极 ②H+向负极移动
③电子流动方向Zn→Cu ④Cu极有H2产生
⑤若有1mol电子流过导线,则产生H2为0.5mol。
⑥正极的电极反应式:Zn-2e- =Zn2+
以上叙述正确的是__________________(填序号)
(2)下图为用石墨电极电解饱和食盐水的装置,往电解液中滴入几滴酚酞试液,接通电源:
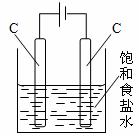
①写出电极反应式
阴极 ;
阳极 。
②电解池总反应的化学方程式为 ,
(填“阴”或“阳”)极附近溶液变红。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com