
19.(9分)根据下列转化关系回答:
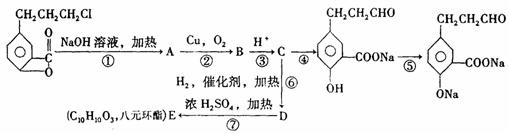
(1)化合物C含有的官能团有________________________________。
(2)反应④需加入的试剂是__________,⑥的反应类型是____________。
(3)写出下列反应的化学方程式:
反应①______________________________________________;
反应⑦______________________________________________。
18.下图是一个乙醇燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题:
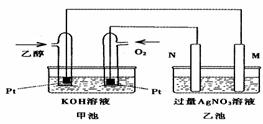
(1)M电极的材料是 ,电极名称是 ,N的电极反应式
为 ,通入乙醇的铂电极的电极反应式为 。
(2)在此过程中,乙池中某一电极析出金属银4.32g时,甲池中理论上消耗氧气为
L(标准状况下);若此时乙池溶液的体积为400mL,则乙池中溶液的pH为 。
(3)若在常温常压下,1g C2H5OH燃烧生成CO2和液态H2O时放出29.71kJ热量,表
示该反应的热化学方程式为 。
17.(10分)在元素周期表中,锌(30Zn)、镉(48Cd)、汞(80Hg)同属于锌族,锌和汞在自然界中常共生,镉的金属活动性介于锌和汞之间。湿法炼锌过程中产生的铜镉渣中含有Cu、Cd、Zn等多种金属,可用于生产金属镉。镉的主要用途可以用作镍-镉电池,以及用于颜料生产,镉化合物还在PVC稳定剂、发光材料、半导体材料、杀菌剂等方面有广泛的应用。镉的生产流程如图示意如下:
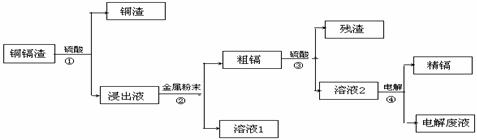
请回答下列问题:
(1)镉元素位于周期表中第 周期,第 族,其原子结构示意图为 ;
(2)写出步骤①反应的离子方程式 。
(3)步骤②所加入的金属是 。
(4)步骤④用“溶液2”作电解液,镉在 极析出,该电极材料是
(5)“电解废液”中含有镉,不能直接作为污水排放。目前含镉的废水处理的方式有两种,
一种是在含镉污水中加入硫化钠,沉淀镉离子,另一种是加入聚合硫酸铁和聚合氯化铝,沉
淀镉离子。写出硫化钠沉淀镉离子的离子方程式 。
16.(12)下图为中学化学中几种常见物质的转化关系(部分产物已略去)。已知:A、C、D是常见的气体单质,F气体极易溶于水,且液态常做制冷剂。
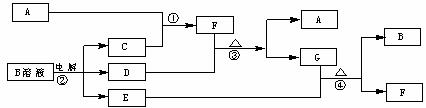
(1)写出化学式A ,D ,F ,写出电子式G ;
(2)鉴定G中阳离子的实验方法和现象___________________________ _;
(3)D单质和E溶液反应,生成一种常见的消毒剂和漂白剂的有效成分,写出D+E溶
液反应的离子方程式和③的化学方程式 、
。
(4)工业上电解B溶液制得一系列化工原料,写出其电解的化学方程式,并标出电子
转移的方向和数目 。
15.(1)(4分)化学实验必须注意安全,下列做法存在安全隐患的是 (选填序号)。
A.氢气还原氧化铜实验中,先加热氧化铜后通氢气
B.蒸馏石油时,加热一段时间后发现未加碎瓷片,立刻拔开橡皮塞并投入碎瓷片
C.实验室做钠的实验时,余下的钠屑投入到废液缸中
D.配制浓硫酸与酒精混合液时,将1体积的酒精倒入3体积的浓硫酸中
E.皮肤上沾有少量浓硝酸时,立刻用大量水冲洗,再涂上稀碳酸氢钠溶液
F.制乙烯时,用量程为300℃的温度计代替量程为200℃的温度计,测反应液的温度
(2)(8分)下图甲是课本中验证铜和浓硝酸反应的装置,乙、丙是师生对演示实验改进后
的装置:
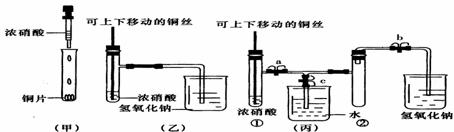
(1)甲、乙、丙三个装置中共同发生的反应的化学方程式是
(2)和甲装置相比,乙装置的优点是 ① ;② 。
(3)为了进一步验证NO2和水的反应,某学生设计了丙装置。先关闭弹簧夹 ,再打开弹簧夹 ,才能使NO2气体充满试管②。
(4)当气体充满试管②后,将铜丝提起与溶液脱离,欲使烧杯中的水进入试管②应如何操作?
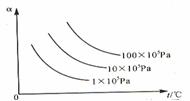
14.下图纵坐标为反应物的转化率,横坐标为温度,下列符合此图情况的反应是 ( )
A.C(s) + CO2(g)  2CO(g);△H >0
2CO(g);△H >0
B.H2(g) + Br2(g)
 2HBr(g);△H<0
2HBr(g);△H<0
C.N2(g) + 3H2(g)
 2NH3(g);△H<0
2NH3(g);△H<0
D.2SO3(g)  2SO2(g)
+ O2(g);△H>0
2SO2(g)
+ O2(g);△H>0
13.通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能的大小可用于
估算化学反应的反应热(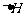 ),化学反应的
),化学反应的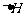 等于反应中断裂旧化学键的键能之和与反
等于反应中断裂旧化学键的键能之和与反
应中形成新化学键的键能之和的差。
|
化学键 |
H-H |
Cl-Cl |
H-Cl |
|
生成1 mol化学键时放出的能量 |
436 kJ·mol-1 |
243 kJ·mol-1 |
431 kJ·mol-1 |
则下列热化学方程式不正确的是 ( )
A.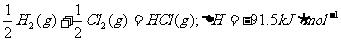
B.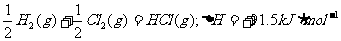
C. 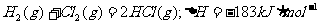
D.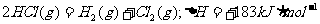
12.2008 年北京奥运会主体育场的外形好似“鸟巢” ( The Bird Nest )。有一类硼烷也好似鸟巢,故称为巢式硼烷。巢式硼烷除 B10H14不与水反应外,其余均易与水反应生成氢气和硼酸,硼烷易被氧化。下图是三种巢式硼烷,有关说法正确的是 ( )
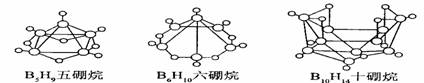
A.这类巢式硼烷的通式是 B nH n + 4
B.2B5H9 + 12O2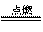 5B2O3
十9H2O,l molB5H9完全燃烧转移25mol电子
5B2O3
十9H2O,l molB5H9完全燃烧转移25mol电子
C.8 个硼原子的巢式棚烷化学式应为 B8H10
D.硼烷与水反应是非氧化还原反应
11.分析下图所示的四个原电池装置,其中结论正确的是 ( )
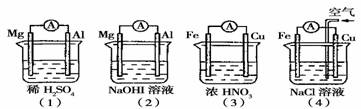
A.(1)(2)中Mg作负极,(3)(4)中Fe作负极
B.(2)中Mg作正极,电极反应式为:6H2O+6e-→6OH-+3H2↑
C.(3)中Fe作负极,电极反应式为:Fe→Fe2++2e-
D.(4)中Cu作正极,电极反应式为:2H++2e-→H2↑
10.常温下,甲、乙两杯醋酸稀溶液,甲的pH=a,乙的pH=a+1,对下列叙述的判断正确的是 ( )
A.甲中水电离出来的H+的物质的量浓度是乙中水电离出来的H+的物质的量浓度的10倍
B.中和等物质的量的NaOH溶液需甲、乙两杯醋酸溶液的体积,10V(甲)=V(乙)
C.物质的量浓度c(甲)>10c(乙)
D.甲中的c(OH-)为乙中的c(OH-)的10倍
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com