
3.晶体A中Hg占据什么典型位置,占有率是多少?
2.晶体A中,NH3、Cl的堆积方式是否相同,为什么?
1.写出A、B的化学式和B的生成反应方程式;
4.下面是一种刚获得专利的KNO3制备方法的主要步骤:①将CaSO4·2H2O与NH4HCO3按摩尔比约为1︰2加入饱和的(NH4)2SO4母液中搅拌反应;②反应结束后过滤,滤饼为CaCO3,___________________________________________________________,结晶出(NH4)2SO4晶体。③经过滤得到(NH4)2SO4晶体,干燥得到固态的(NH4)2SO4,____________________。④按固态(NH4)2SO4与KCl按摩尔比约为1︰2,配料后混合粉碎。⑤将上述混合物送入干法反应器中,在常压下加热反应,得到固态的K2SO4。⑥ __________________。⑦将第②步反应得到的CaCO3与硝酸溶液反应,得到Ca(NO3)2水溶液。⑧ 。⑨将第⑧步得到的反应物热过滤,滤饼用于 ,滤液冷却到常温结晶析出KNO3晶体。⑩将第⑨步得到的含有KNO3晶体的物料过滤,滤液 ,滤饼KNO3晶体干燥得到最终产品。
(1)请将上面的实验步骤补充完整;
(2)写出上述反应方程式和总反应方程式;
(3)请简要评价该方法的优点。
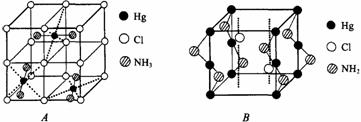
第4题(9分)下图所示为HgCl2和不同浓度NH3-NH4Cl反应得到的两种含汞的化合物A和B的微观结构重复单元图。
3.用固态KCl同有机溶剂(如丁醇或乙醚,均用ROR表示)中的硝酸稀溶液发生反应,可使反应物中的NO3-转化率达到100%。
(1)写出该反应方程式;
(2)加入ROR的作用是什么;
(3)该方法相对于上述其余两种方法的优点是什么?
2.将硝酸与浓的KCl溶液混合,可以得到一种黄绿色气体A和另一种气体B,KNO3是一种副产品。B具有腐蚀性,B与O2反应又可生成A和气体C,C是一种无色的平面型分子。写出上述两个反应方程式;
1.利用NaNO3和KCl进行制备是最常见最简单的方法,写出制备原理;
4.写出H2S代替H2O进行光合作用的主要产物。5.画出D的一种合理结构式,并指出有几种不同的成键方式。
第2题(7分)H2O2的水溶液是一种常用的杀菌剂,其质量百分比一般为3%和30%。
2-1 在H2O2作用下可实现Fe(CN)63-与Fe(CN)64-之间的相互转化,在酸性溶液中H2O2可使Fe(CN)64-转化为Fe(CN)63-;在碱性溶液里H2O2可使Fe(CN)63-转化为Fe(CN)64-。写出以上相互转化的离子方程式 。
2-2 分别写出实验室、老工业、新工业制备H2O2的三种方法。
2-3 写出二种定量测定H2O2水溶液中H2O2含量的化学方程式和简要实验步骤。
2-4 将H2O2溶液滴入含有酚酞的NaOH溶液中,红色消失。甲学生认为这是由于H2O2是二元弱酸,消耗了OH-,而使红色褪去;乙学生认为,H2O2具有强氧化性,将酚酞氧化,红色消失。试设计一个实验论证甲、乙两位学生的解释中哪种正确?
第3题(9分)KNO3是一种重要的化工产品。工业上制备KNO3的方法较多,常见有下列四种方法:
1.写出M的元素符号;2.写出上述所有核化学反应方程式;3.写出B与C互相转化的离子方程式;
13若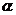 是第二象限角,判定
是第二象限角,判定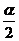 所在象限,然后化简
所在象限,然后化简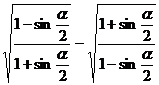
14已知函数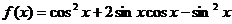
(1) 求f(x)的最小正周期;
(2) 求f(x)的最大值、最小值;
(3) 试说明f(x)怎样由sinx变换得来。
|

 15在高出地面15m的小山顶上建造一个塔CD,如图所示.今在距B点30m的地面上取一点A,若测得CD的张角为45
15在高出地面15m的小山顶上建造一个塔CD,如图所示.今在距B点30m的地面上取一点A,若测得CD的张角为45 ,试求这座塔的高度。
,试求这座塔的高度。
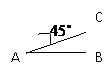
16 已知函数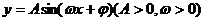 的图象过点P
的图象过点P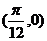 ,图象上与点P最近的一个最高点是Q
,图象上与点P最近的一个最高点是Q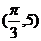 。 (1)求函数的解析式;(2)指出函数的单调递增区间;(3)求使
。 (1)求函数的解析式;(2)指出函数的单调递增区间;(3)求使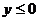 的x的取值范围。
的x的取值范围。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com