
6、(八校)下列有关物质的分类或归类正确的是( )
①混合物:石炭酸、福尔马林、水玻璃、水银 ②化合物:CaCl2、烧碱、聚苯乙烯、HD ③电解质:明矾、胆矾、冰醋酸、硫酸钡 ④同系物:CH2O2、C2H4O2、C3H6O2、C4H8O2 ⑤同位素:612C、613C、614C
A、①③④ B、③⑤ C、②③④ D、②④
4.(闵行一)下列各组物质的类别归属正确的是( )
A.同位素:1H2、2H2、3H2
B.分子晶体:I2、SO3、固态氩
C.非电解质:Cl2、BaSO4、C2H5OH
D.化合物:重水、双氧水、矿泉水
3.(闵行二)下列各组物质的分类正确的是( )
A.同分异构体:乙酸、乙二酸
B.同位素: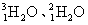
C.同素异形体:金刚石、C60 D.同系物:甲醇、苯甲醇
4.(十四校二)下列各组物质的分类,正确的是( )
 A.同位素:红磷、白磷 B.非电解质:Cl2、C2H5OH
A.同位素:红磷、白磷 B.非电解质:Cl2、C2H5OH
C.非极性分子:CO2、CCl4 D.同系物: OH、 OCH3
5.(闵行二)以下是人们对原子结构的认识所经历的几个重要历史阶段:①道尔顿提出的原子论;②汤姆孙提出的葡萄干面包原子摸型;③德谟克里特的古典原子论;④卢瑟福的原子结构行星模型。其先后顺序正确的是( )
A.①②③④ B.②③①④ C.③④②① D. ③①②④
31.(1)1-2.33a%(2分) (2)10; 200; 50(元素守恒) (各2分)
(提示:设通入的水蒸气为Xm3,则有
CH4+CO2→2H2+2CO CH4+H2O→3H2+CO
5 5 10 10 X X 3X X
2CH4 + O2→ 4H2 + 2CO
95-5-X 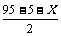 2(95-5-X) 95-5-X
2(95-5-X) 95-5-X
所以有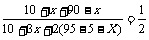 ,可以得出X=10m3,
,可以得出X=10m3,
通入的空气的体积为:5×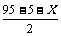 =200 m3 ).
=200 m3 ).
(3)CO(1分);360(1分)。
31.(静安二)甲醚(CH3OCH3)是一种新型的合成“柴油”,它可由天然气(体积分数:CO2为5%,CH4为95%)合成。合成甲醚主要步骤为造气和合成。过程如下(气体体积均在同温同压下测定;氧气由空气提供,其中N2和O2的体积比为4:1;不考虑CO与水的反应;各步反应转化率均为100%):
|
|

(1)若造气得到的气体只含CO和H2,该混合气体中,碳元素的质量分数为a%,则氢元素的质量分数为 %(用含a的式子表示)。
(2)造气时每使用100m3天然气,应同时通入水蒸气________m3、空气_________m3,才能保证合成时CO与H2的体积比为1:2;合成甲醚后,有________m3的水蒸气可参加循环生产。
(3)若只用天然气和空气造气,合成后得到的蒸气成分如下表:
|
气体 |
CH3OCH3 |
H2O |
N2 |
A |
|
体积(m3) |
95 |
95 |
x |
y |
则A气体的分子式为 ; x = 。
30.(6分,各2分)(1) 21.43 (2)17.53 (3)53.33
30.(静安二)某工厂的生产废水中含糖类[以(CH2O)n表示],该厂用化学和生物方法处理废水,若废水中的糖类有45%被完全氧化,即发生反应 (CH2O)n + nO2 → nCO2 + nH2O;另有10% 经过发酵过程进行无氧分解,即 2(CH2O)n → nCO2 + nCH4 。其余部分糖类仍然留在沉积物中。该厂每天处理废水得到的CO2和CH4共16.0m3(标准状况)。
(1)每天被氧化和被发酵的糖类共 千克。(2)每天有 千克糖类留在沉积物中。
(3)COD(化学耗氧量)是指1L水样中还原性物质完全被氧化所需要的氧气的毫克数。若该工厂的生产废水中糖类的质量分数为百万分之五十(设废水的密度为1g/cm3;无其它还原性物质),则其COD为 mg/L.
30.(1)b=4(或A分子式中氢原子数为4);CH4O(2分)
(2)A和CH4分子式相差n个CO2,n为正整数; C2H4O2(2分)
(3)y=b 和2(a-x) = c(2分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com