
10.(粤西北九校)⑴CO32-+H2O HCO3-+OH-
(4分)
HCO3-+OH-
(4分)
⑵c(Na+)>c(Cl-)=c(CO32-)= c(HCO3-)>c(OH-)>c(H+) (4分)
⑶Na2CO3恰好转化为NaHCO3,此时溶液的pH值为8 (4分) ⑷6(4分)
(韶关一模--32)1)NO2(g)+CO(g)=CO2(g)+NO(g) ΔH=-234kJ/mol
2)①> ②AC 3) ①N2H62++H2O
 NN2H6OH+ [(N2H5
H2O]++H+ ②A
NN2H6OH+ [(N2H5
H2O]++H+ ②A
(茂名一模--31)(1)①1:2 ②BF
(2)K=4.5L/mol 转化率为60%
(3)①SO2、H2混合气 ②将所得气体通过品红,褪色即可证明含有SO2。将所得气体通过浓度硫酸后通入灼热的CuO中,若CuO变红色,有水蒸气生成则证明有H2。
9.(深圳一模)Ⅰ(2)CH2OH(CHOH)4CHO + 2Cu(OH)2 → CH2OH(CHOH)4COOH+Cu2O↓+2H2O (3分)
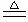 (3)Cu2O 2分)
(3)Cu2O 2分)
(4)4Cu(OH)2 + N2H4 2Cu2O + N2 + 6H2O (3分)
Ⅱ(1)5.0×10-5 mol·L-1 min-1 (2分)


或 (2分) 0.97 (2分)
(2)ACD (3分,选对一个只得1分,错选一个倒扣1分,最少得0分)
注:(有效数字错误或单位错误共扣1分)
8.(佛山一模)(1)CH4 (g) + 2O2 (g) = 2H2O (l) + CO2(g) △H =-4Q kJ·mol-1 。……………(2分)
(2)50-60均可,95%(填近似值即可)…………………………(各2分,共4分)
(3)①40% …………………(3分)
② ………(3分,无单位不扣分,写单位但写错扣1分)
………(3分,无单位不扣分,写单位但写错扣1分)
>……(1分) (4)CDE………(对1个给1分共3分,错、漏1个倒扣1分)
7.(广东六校联考)(1) 0.0003 mo1·L -1·min-1(2) ① <; ② V 2/a2 ③增大;不变
4.(华附四校)(1)2Fe3++2I-=2Fe2++I2 (2分,此处写“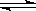 ”不扣分)
”不扣分)
(2)萃取;分层,上层为紫色(浅紫色到紫红色均给分),下层接近无色;正反应方向(或右)(各2分,共6分)
(3)淀粉溶液;变蓝 (各2分,共4分)(4)m=1;n=2 (各2分,共4分)
(5)3.645х104 L • mol -1 (4分)
2.(广州一模)(17分)
(1)①-247kJ.mol-1
(3分) ②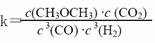 (3分)
(3分)
(2)增大(3分)。
(3)反应③消耗了反应②中的产物H2O(3分),使反应②的化学平衡向正反应方向移动(1分),从而提高CH3OCH3的产率。(共4分)
(4)温度低于240℃时,CO的转化率随着
温度的升高而增大;温度高于240℃时,CO的转化率随着温度的升高而减小。(2分,答“CO的转化率先增大,后减小”,得1分;没有明确提出“240℃”,不扣分)
在较低温时,各反应体系均未达到平衡,CO的转化率主要受反应速率影响,随着温度的升高反应速率增大,CO的转化率也增大;在较高温时,各反应体系均已达到平衡,CO的转化率主要受反应限度影响,随着温度的升高平衡向逆反应方向移动,CO的转化率减小。(共2分,平衡或未平衡状态,得1分;速率影响和平衡移动方向影响,得1分。)
1.(广州市高三调研题)
(1)降低了活化能(3分)
(2)H2O2 H++HO2-(3分)
H++HO2-(3分)
(3)探究浓度对反应速率的影响 (3分)
向反应物中加入等量同种催化剂(或将盛有反应物的试管放入同一热水浴中)(3分)
(4)碱性环境能增大H2O2分解的速率,酸性环境能减小H2O2分解的速率 (4分)
5.(金山中学)⑴ 0.15(2分) 2(1-1/a) (2分)
⑵N2+6e-+6H+=2NH3 (2分)
⑶N2 (1分) 生成NO的反应为放热反应,升高温度转化率下降 (1分)
进一步与NO反应生成硝酸(1分)
⑷ NO+NO2+H2O=2HNO2;(1分) CO (NH2)2+2HNO2=CO2+2N2+3H2O(1分)
(5)CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H =867kJ/mol
4.(16分)(1)1×10-5(4分)
(2)①对于平衡BaSO4(s) Ba2+(aq) + SO42-(aq),H+不能减小Ba2+或SO42-的浓度,故平衡不能向溶解方向移动.(4分)
Ba2+(aq) + SO42-(aq),H+不能减小Ba2+或SO42-的浓度,故平衡不能向溶解方向移动.(4分)
②胃酸可与BaCO3反应,使CO32-浓度降低,从而使平衡BaCO3(s) Ba2+(aq) + CO32-(aq) 向溶解方向移动,使Ba2+浓度增大。(4分) (3)2×10-10(4分)
Ba2+(aq) + CO32-(aq) 向溶解方向移动,使Ba2+浓度增大。(4分) (3)2×10-10(4分)
3.(16分)
(1)172.5 (4分)
(2)S2-
+ H2O HS-
+OH- HS-
+ H2O
HS-
+OH- HS-
+ H2O H2S
+OH-(可不写) (4分)
H2S
+OH-(可不写) (4分)
(3)Ⅰ.使BaSO4得到充分的还原(或提高BaS的产量) (4分)
Ⅱ. ①②为吸热反应,炭和氧气反应放热维持反应所需高温 (4分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com