
27.(12分)
纳米材料二氧化钛(TiO2)具有很高的化学活性,可做性能优良的催化剂。
(1)工业上二氧化钛的制备是:
|
资料卡片 |
||
|
物质 |
熔点 |
沸点 |
|
SiCl4 |
-70 ℃ |
57.6 ℃ |
|
TiCl4 |
-25 ℃ |
136.5 ℃ |
Ⅰ.将干燥后的金红石(主要成分TiO2,主要杂质SiO2)与碳粉混合装入氯化炉中,在高温下通入Cl2反应,制得混有SiCl4杂质的TiCl4。
Ⅱ.将SiCl4分离,得到纯净的TiCl4。
Ⅲ.在TiCl4中加水、加热,水解得到沉淀TiO2·xH2O。
Ⅳ.TiO2·xH2O高温分解得到TiO2。
① TiCl4与SiCl4在常温下的状态是 ,分离二者所采取的操作名称是 。
② Ⅲ中反应的化学方程式是 。
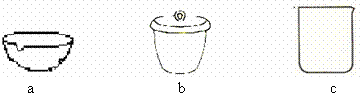
③ 如Ⅳ在实验室完成,应将TiO2·xH2O放在 (填仪器编号)中加热。
(2)据报道:“生态马路”是在铺设时加入一定量的TiO2,TiO2受太阳光照射后,产生的电子被空气或水中的氧获得,生成H2O2,其过程大致如下:
a.O2 2O
b.O+H2O
2O
b.O+H2O 2OH(羟基) c.OH+OH
2OH(羟基) c.OH+OH H2O2
H2O2
① b中破坏的是 (填“极性共价键”或“非极性共价键”)。
② H2O2能清除路面空气中的CxHy、CO等,其主要是利用了H2O2的 (填“氧化性”或“还原性”)。
(3)某研究小组用下列装置模拟“生态马路”部分原理。(夹持装置已略去)
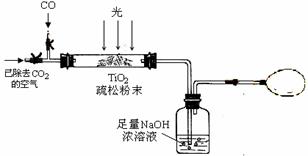
① 如缓慢通入22.4 L(已折算成标准状况)CO气体,结果NaOH溶液增重11 g,则CO的转化率为 。
② 当CO气体全部通入后,还要通一会儿空气,其目的是 。
26.(14分)
在下列物质转化关系中,反应的条件和部分产物已略去。
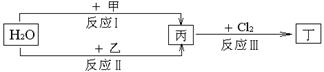
回答下列问题:
(1)若甲、乙是两种常见金属,且反应Ⅲ是工业制盐酸的反应。
①反应Ⅰ中甲在通常条件下和水剧烈反应,除丙外,还生成一种焰色反应为黄色的物质,则工业上生产甲的一般方法是 。
A.热分解法 B.热还原法 C.电解法
②反应Ⅱ中乙与H2O在高温下反应,除丙外,还生成一种有磁性的物质,则反应Ⅱ的化学方程式是 。
③ 通过比较反应Ⅰ、Ⅱ的反应条件,可得出甲的金属性比乙的金属性 (填“强”或“弱”),比较二者金属性强弱的依据还可以是 (写出一种即可)。
(2)若甲、乙是化合物,且反应Ⅲ是工业上制漂白粉的反应。
① 反应Ⅲ的化学方程式是 。
② 反应Ⅰ的另一种产物为有机物,则该有机物的电子式是 。
③ 反应Ⅱ是化合反应。乙可与硫酸铵共热反应制氨气,则此反应的化学方程式是 。
④ 在饱和氯水中加块状石灰石,能制得较浓HClO溶液,同时放出一种气体。其反应的离子方程式是 。
25.(16分)
 高分子化合物Z在食品、医疗方面有广泛应用。下列是合成Z的流程图:
高分子化合物Z在食品、医疗方面有广泛应用。下列是合成Z的流程图:
(1) 烃A的结构简式是 。W中含有的官能团名称是 。
(2) X(C3H8O3)分子中每个碳原子上均连有相同的官能团,X的结构简式是 。
(3) B为烃。核磁共振氢谱显示:B、D均有三种类型氢原子的吸收峰,且峰面积之比均为1:2:3。则B生成C的化学方程式是 。
(4)① Z的单体分子中含甲基,由其生成Z的化学方程式是 。
② W可发生加聚反应,生成的高分子化合物的链节是_________。
(5)戊二酸( HOOC-CH2-CH2-CH2-COOH )是合成树脂的引发剂。现以CH≡CH、CH3CH2OH、HCN为原料,设计合理方案合成戊二酸,用类似合成Z的流程图表示。
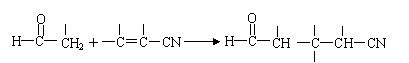 提示:
提示:
①
② 合成过程中无机试剂任选。
12.T ℃时,在1 L的密闭容器中充入2 mol CO2和6 mol H2,一定条件下发生反应:
CO2(g)+3H2(g) 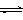 CH3OH(g)+H2O(g) △H=-49.0 kJ/mol
CH3OH(g)+H2O(g) △H=-49.0 kJ/mol
测得H2和CH3OH(g)的浓度随时间变化如下图所示。下列说法不正确的是
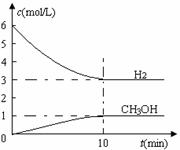 A.0~10 min 内υ(H2)=0.3 mol/(L·min)
A.0~10 min 内υ(H2)=0.3 mol/(L·min)
B.T ℃时,平衡常数K = 1/27,CO2与H2的转化率相等
C.T ℃时,上述反应中有64 g CH3OH生成,同时放出98.0 kJ的热量
D.达到平衡后,升高温度或再充入CO2气体,都可以提高H2的转化率
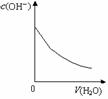
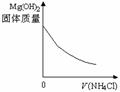
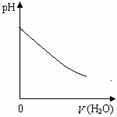
11.室温下,下列图形与实验过程相符合的是
 |
 |
 |
 |
|
A. 盐酸加水稀释 |
B.Mg(OH)2悬浊液中滴加NH4Cl溶液 |
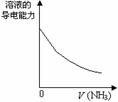
C.NH4Cl稀溶液加水稀释 |
D.
NH3通入醋酸溶液中 |
10.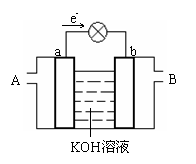 右图是水煤气 (成分为CO、H2)空气燃料电池的工作原理示意图,a、b均为惰性电极。下列叙述中正确的是
右图是水煤气 (成分为CO、H2)空气燃料电池的工作原理示意图,a、b均为惰性电极。下列叙述中正确的是
A.A处通入的是空气,B处通入的是水煤气
B.a电极发生还原反应,b电极发生氧化反应
C.a电极的反应式包括:CO + 4OH-+ 2e-== CO32-+ 2H2O
D.如用这种电池电镀铜,待镀金属增重6.4 g,则至少消耗
标准状况下的水煤气2.24 L
9.电子层数相同的短周期元素X、Y、Z、W,其中X的最外层电子数比K层少1,Y的最外层电子数比K层多1,Z的单质是一种半导体材料,常用于制造太阳能电池,W的原子半径是同周期中最小的。下列推断中正确的是
A.Z的氢化物的热稳定性强于W的氢化物
B.Z的氧化物与水反应可制得相应的含氧酸
C.X、Y、W的原子半径依次减小,对应的离子半径依次增大
D.X、Y、W的最高价氧化物对应水化物之间互相都能发生反应
8.已知A、B为单质,C为化合物。
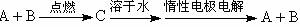
能实现上述转化关系的是
① 若C溶于水后得到强碱溶液,则A可能是Na
② 若C的溶液遇Na2CO3放出CO2气体,则A可能是H2
③ 若C的溶液中滴加KSCN溶液显红色,则B可能为Fe
④ 若C的溶液中滴加NaOH溶液有蓝色沉淀生成,则B可能为Cu
A.① ② B.② ④ C.① ③ D.③ ④
7.磷酸氢二铵 [(NH4)2HPO4]可用作化肥。下列关于该物质的说法不正确的是
A.HPO42-中含有共价键,其中P的化合价为+5价
B.是一种离子化合物,其中铵根离子的电子式为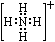
C.该化合物中所有原子均满足8电子稳定结构
D.其中P元素的质量分数比N元素的质量分数高
6.下列有关安全事故的处理不恰当的是
A.不慎将苯酚沾到皮肤上,应立即用酒精洗涤
B.一氧化碳中毒后,应尽快将中毒者抬到空气新鲜处
C.不慎将浓硫酸沾到皮肤上,应立即用氢氧化钠溶液洗涤
D.解救Cu2+、Hg2+等重金属盐中毒的病人,可让病人服用大量牛奶或豆浆
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com