
(1)根据元素的化合价
[练 习]下列微粒:H+、Cu2+、Ag+、Fe2+、Fe3+、Cl-、S2-、I-、MnO4-、ClO3-、NO3-、SO32-、S、Cl2、Na、H2;其中只有氧化性的是 ;只有还原性的
是 ,既有氧化性又有还原性的是 ;
[思考]如果物质中某元素具有最高价,该元素只有 性;物质中元素具有最低价,该元素只有 性;物质中元素具有中间价态,该元素既有 又有 性。对于同一种元素,价态越高,则 性越强,价态越低,则 性越强。
(2)根据氧化还原反应方程式
强还原剂(A)+强氧化剂(B)=弱氧化产物(a)+弱还原产物(b)
则氧化性:B>a,还原性:A>b
氧化剂的氧化性越强,则其对应的 产物的还原性则越 ;还原剂的还原性越强,则其对应的 产物的氧化性则越 。
(3)根据金属活动性顺序表
在金属活动性顺序表中,位置越靠前,其还原性就越 ,其阳离子的氧化性就越 。
(4)根据元素周期表
同周期元素,随着核电荷数的递增,氧化性逐渐 ,还原性逐渐 ;同主族元素,随着核电荷数的递增,氧化性逐渐 ,还原性逐渐 。
(5)根据反应的难易程度
氧化还原反应越容易进行(表现为反应所需条件越低),则氧化剂的氧化性和还原剂的还原性就越 。
不同的还原剂(或氧化剂)与同一氧化剂(或还原剂)反应时,条件越易或者氧化剂(或还原剂)被还原(或被氧化)的程度越大,则还原剂(或氧化剂)的还原性(或氧化性)就越 ;
(6)其它条件
一般溶液的酸性越强或温度越高,则氧化剂的氧化性和还原剂的还原性就越 ,反之则越弱。
注意:
1物质的氧化性或还原性的强弱只决定于得到或失去电子的 ,与得失电子的 无关。如:Na、Mg、Al的还原性强弱依次为Na>Mg>Al;浓HNO3、稀HNO3的氧化性强弱依次为:浓HNO3 >稀HNO3;
2同一元素相邻价态间不发生氧化还原反应。
|
概 念 |
得失氧的角度 |
化合价变化的角度 |
电子转移的角度 |
|
氧 化 剂 |
在反应中失去氧的物质 |
所含元素化合价降低的物质 |
在反应过程中得到电子的物质 |
|
还 原 剂 |
|
|
|
|
氧化反应 |
物质得到氧的反应 |
物质所含元素化合价升高的反应 |
物质失去电子的反应 |
|
还原反应 |
|
|
|
|
氧化产物 |
---- |
还原剂中所含元素化合价升高以后的对应产物 |
还原剂中失去电子以后的对应产物 |
|
还原产物 |
---- |
|
|
|
氧 化 性 |
---- |
---- |
氧化剂所具有的得到电子的能力 |
|
还 原 性 |
---- |
---- |
还原剂所具有的失去电子的能力 |
判断氧化反应、还原反应及氧化剂和还原剂、氧化产物和还原产物时可抓住下表中的关系:
|
反应物 |
变化特点 |
生成物 |
|
还原剂 |
失、高、氧---氧化反应 |
氧化产物 |
|
氧化剂 |
得、低、还---还原反应 |
还原产物 |
氧化还原反应的实质是电子的 (包括电子的得失或电子对的偏移),特征是反应前
后 ;判断某反应是否属于氧化还原反应可根据反应前后 是否发生了变化这一特征。
22、(本题满分15分)
已知函数 ,
, ,且
,且 ).
).
(1)讨论函数 的单调性;
的单调性;
(2)若 ,关于
,关于 的方程
的方程 有唯一解,求a的值.
有唯一解,求a的值.
2010年浙江省湖州部分地区高考适应性考试(理科)
21、(本题满分14分)
在平面直角坐标系xOy中,已知对于任意实数 ,直线
,直线 恒过定点F. 设椭圆C的中心在原点,一个焦点为F,且椭圆C上的点到F的最大距离为
恒过定点F. 设椭圆C的中心在原点,一个焦点为F,且椭圆C上的点到F的最大距离为 .
.
(1)求椭圆C的方程;
(2)设(m,n)是椭圆C上的任意一点,圆O: 与椭圆C有4个相异公共点,试分别判断圆O与直线l1:mx+ny=1和l2:mx+ny=4的位置关系.
与椭圆C有4个相异公共点,试分别判断圆O与直线l1:mx+ny=1和l2:mx+ny=4的位置关系.
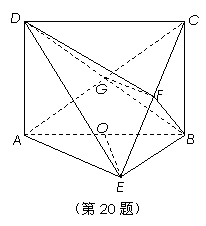
20、(本题满分15分)
如图,已知四边形ABCD为矩形, 平面ABE,AE=EB=BC=2,
平面ABE,AE=EB=BC=2,
F为CE上的点,且 平面ACE.
平面ACE.
(1)求证:AE//平面BDF;
(2)求三棱锥D-ACE的体积.
19、(本题满分14分)
某地区有甲,乙,丙,丁四个单位招聘工作人员,已知一大学生到这四个单位应聘的概率分别是0.4,0.5,0.5,0.6,且他是否去哪个单位应聘互不影响,用 表示他去应聘过的单位数与没有去应聘的单位数之差的绝对值。
表示他去应聘过的单位数与没有去应聘的单位数之差的绝对值。
(1)求 的分布列及数学期望;
的分布列及数学期望;
(2)记“数列 (
( )是严格单调的数列”为事件A,求事件A发生的概率。
)是严格单调的数列”为事件A,求事件A发生的概率。
18、(本小题共14分)
已知向量 与
与 共线,其中A是△ABC的内角.
共线,其中A是△ABC的内角.
(1)求角 的大小;
的大小;
(2)若BC=2,求△ABC面积 的最大值,并判断S取得最大值时△ABC的形状.
的最大值,并判断S取得最大值时△ABC的形状.
17、数列 满足:
满足: ,若数列
,若数列 有一个形如
有一个形如 的通项公式,其中
的通项公式,其中 均为实数,且
均为实数,且 ,则
,则 ▲ .(只要写出一个通项公式即可)
▲ .(只要写出一个通项公式即可)
16、已知点 在直线
在直线 上,点Q在直线
上,点Q在直线 上,PQ的中点为
上,PQ的中点为 ,且
,且 ,则
,则 的取值范围是____▲____.
的取值范围是____▲____.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com