
9.下图为A、B两种物质间的转化关系(其中C、D是反应物,部分产物已省略)。

以下判断不正确的是
A.若A是AlCl3,则C既可以是强碱,也可以是弱碱
 若A是碱性气体,则A和k^s*5#uC可能发生氧化还原反应,也可能发生非氧化还原反应
若A是碱性气体,则A和k^s*5#uC可能发生氧化还原反应,也可能发生非氧化还原反应
C.若A→B是氧化还原反应,则C、D在上述转化过程中一定有一种为氧化剂,另一种为还原剂
D.上述变化过程中,A可以是酸、碱、盐,也可以是单质或氧化物
8.下列各组溶液,用括号内的试剂及物质问相互反应不能鉴别的一组是
A.Ba(OH)2、KSCN、NaCl、Mg(NO3)2 (FeCl3溶液)
 NaNO3、NaHCO3、(NH4)2SO3、Na2SiO3 (H2SO4溶液)
NaNO3、NaHCO3、(NH4)2SO3、Na2SiO3 (H2SO4溶液)
C.NH4Br、K2CO3、NaI、CaCl2 (AgNO3溶液)
D.(NH4)2SO4、MgSO4、CuSO4、AlCl3 (KOH溶液)
7.a、b、c、d、e为原子序数依次增大的五种短周期元素,下表列出了它们的一些重要参数:

以下说法正确的是
A.a、b两种元素氢化物的沸点高于同主族其它元素的氢化物,原因是它们的分子之间都存在氢键
 e单质与c元素的最高价氧化物对应水化物反应的离子方程式为
e单质与c元素的最高价氧化物对应水化物反应的离子方程式为
2Al+2OH-+H2O=2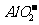 +2H2↑
+2H2↑
C.氢化物的稳定性:a>b
D.d在a的单质中燃烧,产物中阳离子的半径大于阴离子的半径
6.下列对化学概念的理解正确的是
A.NaCl、NaClO、NaHSO4、Na2O2晶体中阳离子和k^s*5#u阴离子的个数比都是1 :1
B.在单质的晶体中可能存在原子、分子或阳离子,但不可能存在阴离子
C.共价键、离子键、范德华力和k^s*5#u氢键是形成晶体微粒之间的四种作用力,这四种作用力可能同时存在于同一晶体中
D.不同类型晶体的熔沸点不同,根据物质的熔沸点数据即可判断其所属的晶体类型
30.(15分)根据以下有机物之间的高*考#资^源*网转化关系框图,回答问题:
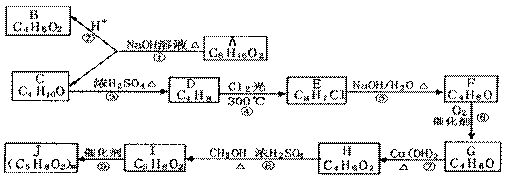
(已知:B的高*考#资^源*网分子结构中带有支链,可由C通过两步氧化反应得到)
(1)D的高*考#资^源*网名称为(用系统命名法命名)____________________。
(2)F中含有的高*考#资^源*网官能团的高*考#资^源*网名称为____________________。
(3)③和⑧的高*考#资^源*网反应类型分别是_______________________、____________________。
(4)写出与H具有相同官能团的高*考#资^源*网H的高*考#资^源*网所有同分异构体的高*考#资^源*网结构简式:__________________________.
(5)B与C可通过酯化反应生成A,反应方程式为_________________________。
(6)分别写出反应⑦和⑨的高*考#资^源*网化学方程式:
⑦_____________________________________________________;
⑨_____________________________________________________。
29.(15分)碳及其含碳化合物在人们的高*考#资^源*网生产生活中应用广泛。
(1)天然气是人们日常生活中的高*考#资^源*网清洁能源。
已知①CH4(g)+2O2(g)=CO2(g)+2 H2O(l); △H1=-890.3kJ·mol-1
②2 CO(g)+O2(g)=2CO2 (g); △H2=-566 kJ·mol-1
则反应2 CH4(g)+3O2(g)=2CO(g)+4H2O(l)的高*考#资^源*网△H=_____________。
(2)甲烷燃料电池的高*考#资^源*网化学方程式为CH4+2O2=CO2+2H2O。某甲烷燃料电池以甲烷为燃料,以空气为氧化剂,以熔融的高*考#资^源*网K2CO3(其中不含O2-和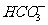 )为电解质,以具有催化作用和导电性能的高*考#资^源*网稀土金属为电极。
)为电解质,以具有催化作用和导电性能的高*考#资^源*网稀土金属为电极。
该燃料电池的高*考#资^源*网负极电极反应式为:CH4-8e-+4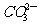 =5CO2+2H2O,则其正极电极反应式为____________;为使电解质的高*考#资^源*网组成保持稳定,使该燃料电池长时间稳定运行,在通入的高*考#资^源*网空气中必须加入________________物质。
=5CO2+2H2O,则其正极电极反应式为____________;为使电解质的高*考#资^源*网组成保持稳定,使该燃料电池长时间稳定运行,在通入的高*考#资^源*网空气中必须加入________________物质。
(3)以该燃料电池为电源,以铂作电极电解1000g 4.55%的高*考#资^源*网NaOH溶液,一段时间后,溶液中溶质的高*考#资^源*网质量分数变为5.00%,则阳极产生的高*考#资^源*网气体在标准状况下的高*考#资^源*网体积为________L。
(4)将不同量的高*考#资^源*网CO(g)和H2O(g)分别通入到体积为2 L的高*考#资^源*网恒容密闭容器中,进行反应CO(g)+H2O(g)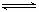 CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
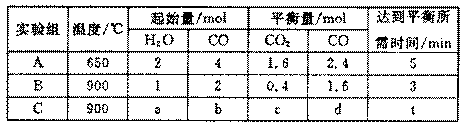
①实验A中以v(H2)表示的高*考#资^源*网反应速率为___________________。
②通过计算可知,CO的高*考#资^源*网转化率实验A_______________实验B(填“大于”、“等于”或“小于”),该反应的高*考#资^源*网正反应为______________热反应(填“吸”或“放”)。
③若实验C要达到与实验B相同的高*考#资^源*网平衡状态,则a、b应满足的高*考#资^源*网关系是_________________(用含a、b的高*考#资^源*网数学式表示)。
28.(15分)A、B、C、D、E为五种短周期元素,其中A、B、C位于同一周期,A元素的高*考#资^源*网气态氢化物是一种广泛应用的高*考#资^源*网优质气体燃料,B元素的高*考#资^源*网氢化物是用途最为广泛的高*考#资^源*网溶剂。B元素可分别与A、C、D、E组成RB2型化合物。已知在DB2中,D与B的高*考#资^源*网质量比为7 :8;在EB2中,E与B的高*考#资^源*网质量比为1 :1。根据以上条件回答下列问题:
(1)请写出C单质分子的高*考#资^源*网电子式______________;DB2晶体中化学键的高*考#资^源*网类型为_____________;写出AE2的高*考#资^源*网结构式 ___________________。
(2)C的高*考#资^源*网气态氢化物易液化,原因是___________________。
(3)C和D结合可生成一种超硬物质,有关该物质性质的高*考#资^源*网叙述中不正确的高*考#资^源*网是______________________.
①有润滑性 ②易磨损 ③抗腐蚀 ④强还原性 ⑤抗冷热
(4)B元素可分别与A、E形成多种由两种元素构成的高*考#资^源*网阴离子。某溶液是由其中若干种阴离子组成的高*考#资^源*网无机钠盐溶液,为了检验该溶液中的高*考#资^源*网阴离子,分别取两份溶液进行如下实验:
①第一份溶液中加入足量盐酸,只产生无色气体;
②第二份溶液中加入足量的高*考#资^源*网BaCl2溶液,有白色沉淀产生,再缓慢加入足量的高*考#资^源*网稀硝酸,白色沉淀质量减少。由此得出的高*考#资^源*网结论是_______________________。
(5)E元素的高*考#资^源*网一种氧化物可与过氧化钠及氯水发生氧化还原反应。该氧化物与过氧化钠反应的高*考#资^源*网化学方程式为_______________________;该氧化物与氯水反应的高*考#资^源*网离子方程式为____________________________。
27.(15分)某研究性学习小组为确定某纯净碱式碳酸镁样品的高*考#资^源*网组成,设计出了下图所示的高*考#资^源*网实验装置(图中A至D的高*考#资^源*网部分)。[已知碱式碳酸镁Mgx(OH)y(CO3)z(x、y、z为正整数)加热能分解生成氧化镁、水和二氧化碳]
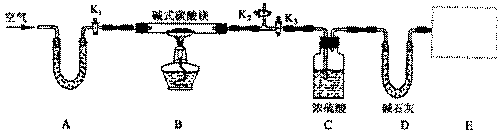
(1)按上图(夹持仪器未画出)组装好实验装置后,应首先进行的高*考#资^源*网操作是__________;A处U形管盛放的高*考#资^源*网药品是__________________,其作用为_______________________。
(2)指导老师在审阅设计方案后指出需要在E处增加一装置,你认为该装置应该是_____________________________.
(3)加热前需要向该装置缓缓鼓入空气数分钟,其目的高*考#资^源*网是___________________;此时对活塞的高*考#资^源*网操作方法是:打开活塞____________________,关闭活塞_________________。
(4)关闭活塞K1、K2,打开K3,加热一段时间后,同学们发现C处洗气瓶中几乎没有气泡冒出,这是由于_________________________。
(5)反应完全后,打开K1,再缓缓鼓入空气数分钟,其目的高*考#资^源*网是_____________________。
(6)实验测得数据如下:碱式碳酸镁样品22.6 g;反应前C装置的高*考#资^源*网质量为87.6 g,反应后质量为89.4 g;反应前D装置的高*考#资^源*网质量为74.7 g,反应后质量为83.5 g。请计算推导该碱式碳酸镁的高*考#资^源*网化学式______________________,该碱式碳酸镁受热分解的高*考#资^源*网化学方程式为____________。
13.25℃时,对下列各溶液的高*考#资^源*网叙述中正确的高*考#资^源*网是
A.pH=2的高*考#资^源*网盐酸与pH=l的高*考#资^源*网硫酸溶液中c(H+)之比为2 :1
B.4种pH相同的高*考#资^源*网溶液:①CH3COONa ②C6H5ONa ③NaHCO3 ④NaOH,各溶液的高*考#资^源*网物质的高*考#资^源*网量浓度由大到小的高*考#资^源*网顺序是③>②>①>④
C.0.1 mol·L-1HA(某酸)的高*考#资^源*网pH=3,0.1 mol·L-1 BOH(某碱)的高*考#资^源*网pH=13,则BA(盐)溶液的高*考#资^源*网pH<7
D.pH=3的高*考#资^源*网醋酸溶液与pH=11的高*考#资^源*网NaOH溶液等体积混合,c(Na)>c(CH3COO)>c(H)>c(OH)
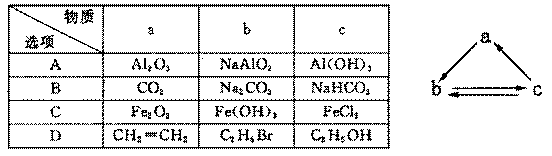
12.下表所列各组物质中,物质之间通过一步反应不能实现如图所示转化的高*考#资^源*网是
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com