
12.



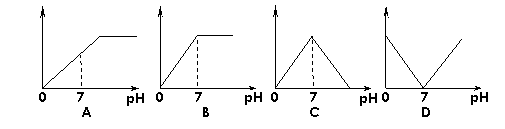 向盛有NaHSO4溶液的烧杯中不断滴Ba(OH)2溶液,随着Ba(OH)2溶液的不断滴入,溶液中产生的沉淀量与pH变化情况正确的是
( )
向盛有NaHSO4溶液的烧杯中不断滴Ba(OH)2溶液,随着Ba(OH)2溶液的不断滴入,溶液中产生的沉淀量与pH变化情况正确的是
( )
11.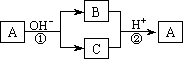 A是一种常见的单质,B、C为中学常见的化合物,A、B、C均含有元素X。它们有如下的转化关系(部分产物及反应条件已略去):下列判断正确的是
( )
A是一种常见的单质,B、C为中学常见的化合物,A、B、C均含有元素X。它们有如下的转化关系(部分产物及反应条件已略去):下列判断正确的是
( )
A.X元素可能为Al B.X元素一定为非金属元素
C.反应①和②互为可逆反应 D.反应①和②不一定为氧化还原反应
10.下列离子方程式正确的是 ( )
A.Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O
B.4mol·L-1的NaAlO2溶液和7mol·L-1的HCl等体积互相均匀混合
4AlO2–+ 7H+ + H2O = 3Al(OH)3↓+ Al3+
C.NaHCO3溶液中加入足量Ca(OH)2溶液 2HCO3– +Ca2+ +2OH–=CaCO3↓+ CO32–+2H2O
D.用惰性电极电解饱和MgCl2溶液:2Cl–+2H2O C12↑+H2↑+2OH–
C12↑+H2↑+2OH–
9.在下列给定条件的溶液中,一定能大量共存的离子组是 ( )
A.无色溶液:Ca2+、H+、Cl-、HSO3-
B.能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3-
C.含Al3+的溶液:K+、Na+、SO42-、AlO2-
D.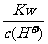 =0.1 mol·L-1的溶液:Na+、K+、SiO32-、NO3-
=0.1 mol·L-1的溶液:Na+、K+、SiO32-、NO3-
8.在标准状况下,将a L NH3完全溶于水得到V mL氨水,溶液的密度为ρ g/cm3,溶质的质量分数为ω,溶质的物质的量浓度为c mol/L。下列叙述中正确的是 ( )
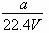
 A.ω=
B. c=
A.ω=
B. c=
C.上述氨水中再加入同物质的量浓度稀盐酸后溶液恰好呈中性,则消耗盐酸的体积<V mL
D.上述氨水中再加入V mL水后,所得溶液的质量分数大于0.5ω
7.下列叙述错误的是 ( )
A.Mg-Al及NaOH溶液构成的原电池中负极反应是:Al-3e-+ 4OH-=AlO2-+ 2H2O
B.无隔膜电解饱和NaCl溶液所得产物之一是“84”消毒液(主要成分NaClO)中的有效成分
C.增加反应物浓度化学反应速率加快,是因为单位体积内活化分子百分数增加
D.相同条件下同浓度钠盐溶液的碱性:NaA<NaB,是因为酸性:HA>HB
6.下列判断错误的是 ( )
A.分别用H2O2、KMnO4分解制O2,当制得等质量O2时,转移电子数之比为1∶2
B.10mL 0.3mol·L-1NaCl与10mL0.1mol·L-1AlCl3溶液中Cl-物质的量浓度比为3∶1
C.同温同压下,密度相同的两种气体的摩尔质量相同
D.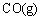 的标准燃烧热是283.0 kJ·mol-1,则
的标准燃烧热是283.0 kJ·mol-1,则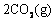 ═
═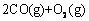 反应的△H=+566 kJ·mol-1
反应的△H=+566 kJ·mol-1
5.设NA为阿佛加德罗常数,下列叙述正确的 ( )
A.标准状况下,11.2 L乙醇完全燃烧生成CO2分子数为NA
B.106 g Na2CO3晶体中的阴离子数大于NA
C.1 mol乙烷分子含有8 NA个共价键
D.5.6 g铁与0.1 mol氯气充分反应转移电子数为 0.2NA
4.分类方法在化学学科的发展中起到了非常重要的作用。下列分类的标准合理的是 ( )
①根据分散系是否具有丁达尔现象将分散系分为溶液、胶体和浊液 ②根据酸分子中含有的氢原子的个数将酸分为一元酸、二元酸等 ③根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应 ④根据化学反应中的热效应将化学反应分为吸热反应和放热反应
A.①② B.②③ C.①④ D.③④
3.室温下,将小苏打投入足量水中,下列过程不会发生的是 ( )
A.溶解 B.电解 C.电离 D.水解
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com