
43、(6分)(1)把一个“熟”水果和几个“生”水果一起放在一个塑料袋内,扎紧袋口,“生”水果很快变“熟”了。若在水果贮藏室内,放几块被高锰酸钾溶液浸透过的“砖块”(即使有“熟”水果),“生”水果可保存较长的时间,为什么?
(2)写出一个以水或水气为催化剂的化学反应方程式及相应的实验现象。
42、(4分)硫与氧的原子结构相似,性质也相似,在许多物质中,硫原子可取代氧原子,如:
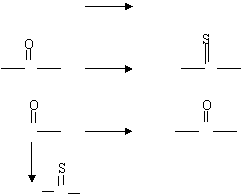 ①CH3CH2CH2OH
②CH3CH2CH2SH
①CH3CH2CH2OH
②CH3CH2CH2SH
③CH3 C CH3 ④ CH3 C CH3
⑤ CH3C OH ⑥CH3 C SH
⑦CH3 C OH
已知物质④命名为丙硫酮,则物质②命名为 ;
已知物质⑥命名为乙硫羟酸,则物质⑦命名为 。
41、(4分)乙硫醇(C2H5SH)和乙二醇相对分子质量都为62,但乙硫醇的熔、沸点比 的熔、沸点 (填“高”或“低”),产生的原因是
。
乙硫醇可用于合成农药及作为指示机械过热的警报器。推测氯乙烷与硫氢化钠在乙醇溶液中共热制乙硫醇的反应方程式为 。
40、(10分)四氯化钛是无色液体,沸点136℃,它非常容易与水反应:
TiCl4+H2O ==TiOCl2 +2HCl↑
遇空气中的水蒸即产生HCl,冒“白烟”。四氯化钛可以由二氧化钛氯化的方法制得:
TiO2 +2Cl2 == TiCl4 +O2
此反应在1000℃高温下进行得也很慢,但如果有炭粉存在时,在600℃-850℃反应便顺利进行。故制备四氯化钛的方法是,利用下图所给仪器,在炭粉存在下对二氧化钛进行氯化。实验步骤如下:
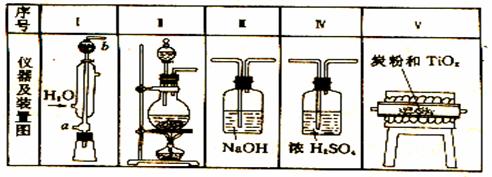
①将事先准备好的二氧化钛和炭粉的混合物放入管式电炉内的瓷管中;②接好装置,在通氯气之前,先通入CO2气体,持续一段时间;③将电炉升温到800℃左右,改通氯气,同时通冷凝水;④当无四氯化钛继续生成时,停止加热,改通二氧化碳气体;⑤冷却到室温,取出产品。
试回答下列问题:
(1)图中仪器从左到右连接的顺序是(填写仪器装置的序号): , , ,
, 其中气流经过装置Ⅰ时是从 到 (填a 或 b )。
(2)装置Ⅱ中的反应物是:固体 和液体 。
(3)装置Ⅰ上端干燥管的作用是 。
(4)装置Ⅰ下端的三角瓶的作用是 。
(5)实验步骤中的②目的是 。
(6)写出在炭粉存在时,制备四氯化钛的化学方程式: 。
39、(4分)化学试剂保存不当往往容易变质,对下面几种药品,试简述:
(1)你通过什么事实证明它们已经变质?
(2)变质的主要原因(不允许用化学方法进行鉴别)。
① Na2O2黄色粉末
②绿矾
38、(12分)同时测定混有少量杂质氯化钠的芒硝的纯度和结晶水含量。按以下图示进行实验:

(1)加热脱水时所用的仪器除了铁架台及铁圈、酒精灯以外,必须的仪器还有
。
(2)加热脱水后,应将样品立即 ,如果放在空气中冷却后称量,将导致测得的结晶水含量偏 。
(3)A溶液可能是:BaCl2 ,AgNO3 ,CaCl2 ,NaOH。从测定的准确性考虑,应该是 (填化学式)。
(4)按以上步骤,计算芒硝的纯度的计算式是:w ( Na2SO4)== ;
计算芒硝中结晶水数目n的算式是:n == 。
37、切割金属钾的方法跟切割金属钠一样,但要特别小心,新切取的钾的切面不要跟未切割钾的表面接触,否则发生剧烈反应会引起爆炸。爆炸的原因是
;
反应式为:
36、写出下列有关学方程式:
(1)将二氧化硫气体通入溴水中: ;
(2)将二氧化硫气体通入氢氧化钡溶液中: ;
(3)将二氧化硫气体通入棕黄色的三氯化铁溶液(在加热条件下),最后生成浅绿色溶液: ;
(4)用一氧化碳还原二氧化硫(500℃,铝钒土)是冶金工业中从烟道废气中回收硫的方法: 。
35、城市管道煤气中常充入极少量的 (填化学式)气体,作为煤气管道泄漏的指示气体。这是因为此气体有 气味,易于察觉;合成盐酸工业中,在制取氯化氢时,常用 (填化学式)气来检验管道是否漏气,这是因为(用化学方程式说明) 。
34、在试管里盛5mL0.1mol/LKI溶液,再加入2-3滴AgNO3溶液,产生黄色沉淀,再加入少量稀硝酸,溶液变为深黄色,其原因是
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com