
14.(3分)大气中CO2的浓度增大能导致温室效应,从而使全球温度升高。这是由于排入大气中的CO2总量与从大气中吸收或消耗的CO2总量不平衡所致。大气中CO2的主要来源有 、 、 ,而吸收或消耗CO2的主要途径有 、 、 。
13.(5分)在摄影化学中,用硫代硫酸钠配制定影液,定影过程的基本反应可表达为:AgBr(固)+2S2O32-=Ag(S2O3)23-+Br-
由此可知定影剂的作用是 。
从废定影液中回收金属银,可采用的方法之一是向其中加入Na2S溶液,反应得到难溶于水的 。过滤后,将此难溶物溶于浓硝酸,这是利用了浓硝酸的 性质,这时又得到的不溶物是 。分离后,向溶液中加入 以制得银。
12.(l分)1985年科学家发现碳的第三种结晶形式,它的组成表示式是 。
11.(3分)写出下列物质的分子式,各指出其一种重要用途。
(1)高氯酸铵
(2)乙酐
(3)砷化镓
10.(4分)写出下列反应的离子方程式:
(1)磷酸二氢钠溶液中加入过量的氢氧化钡溶液
(2)在酸性溶液中,用高锰酸钾将对二甲苯氧化为对苯二甲酸
9.(6分)写出下列反应的化学方程式:
(1)亚碲酸在盐酸中被重铬酸钾氧化为碲酸。
(2)实验室用NH4Cl的饱和溶液与亚硝酸钠晶体混合加热制氮气。
(3)砒霜(三价砷的氧化物)与烧碱溶液反应
已知在溶液中,[H+]·[OH-]=Kw,而溶液的pH=-lg[H+]。试回答7-8题。
7.0℃时,某1mol/L的NaOH溶液中,Kw=10-15,则溶液的pH值是
A 0 B 14 C 15 D 1
8.某温度下,CO2饱和溶液的浓度是0.03mol/L,其中1/3的CO2转变为H2CO3,而H2CO3仅有0.1%发生如下电离:H2CO3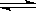 H++HCO3-,则溶液的pH值约是
H++HCO3-,则溶液的pH值约是
A 1 B 3 C 5 D 7
6.生成氨的热化学方程式可用下式表示:
N2(气)+3H2(气)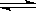 2NH3(气)+92kJ
2NH3(气)+92kJ
如果N2和H2的键能分别为94kJ和435kJ,由此可以算出氮分子中N-H键能为
A 390kJ B 359kJ C 1169kJ D 244kJ
5.分子式为C8H10的芳烃,其一澳代物的同分异构体的总数为
A 10 B 12 C 15 D 16
4.相同质量的下列物质与水反应时,放出氢气最多的是
A 钠 B 锂 C 锂化氢 D 铯
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com