
20.(14分)右图是元素周期表的另一种画法--塔式周期表,在上面标有部分族及部分元素。请回答下列问题:
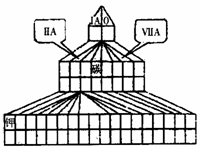 (1)现有A、B、C、D四种短周期主族元素,其中原子序数依次增大。已知A、C位于同一主族,A在周期表中原子半径最小。B、D的最外层电子数相等,且B、D的原子序数之和为A、C原子序数之和的两倍。
(1)现有A、B、C、D四种短周期主族元素,其中原子序数依次增大。已知A、C位于同一主族,A在周期表中原子半径最小。B、D的最外层电子数相等,且B、D的原子序数之和为A、C原子序数之和的两倍。
①在右图塔式周期表相应位置标出A、B、C、D四种元素的元素符号。
②写出上述元素组成的具有漂白作用的四种物质的化学式:_________、___________、____________、_____________。
③C与D形成D的最低价化合物的电子式____________________。
④仅由B、C、D三种元素组成的一种盐,溶于水后呈碱性,请用一个离子方程式表示其呈碱性的原因______________________________________________________________。
(3)在上述塔式周期表中列出了5行元素,每行所包含的元素种类分别为2、8、8、18、18,可分为三类。第四类元素有两行,其中每行所包含的元素均为________种。请根据行数与元素种类的关系,预言第八行最多可能含有________种元素。
19.(13分)实验室里用乙醇和浓硫酸反应生成乙烯,接着再用溴与之反应生成1,2-二溴乙烯,在制备过程中有部分乙醇被浓硫酸氧化产生CO2、SO2、SO3进一步与Br2反应生成HBr等物质。
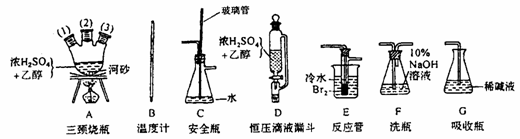
(1)用上列仪器,以上述三种物质为原料制备1,2-二溴乙烷,如果气体流向为从左到右,正确的连接是(短口或橡皮管均已略去):_____经A(1)插入A中,_____接A(2)接______接_____接______接______(填各装置的代号)
(2)在三颈烧瓶A中的主要反应的化学方程式为_______________________________。
(3)在反应管E中进行的主要反应的化学方程式为____________________________。
(4)温度计水银球的正确位置是___________________________________________。
(5)反应管E中加入少量水并把反应管E置于盛有冷水的小烧杯中是因为_________
___________________________________________________________________________。
18.(14分)欲用浓硝酸法(测定反应后生成气体的量)测定某铜银合金中铜的质量分数,但资料表明:①反应中除生成NO2气体外还有少量NO生成;②常温下NO2和N2O4混合存在,在低于0℃时,几乎只有无色的N2O4液体或晶体存在。为完成测定并验证确有NO生成,有人设计了如图所示的实验装置。
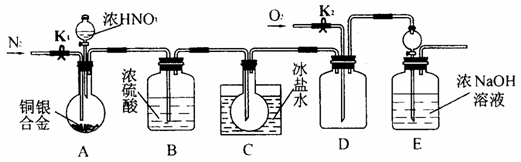
(1)实验开始前要先打开A部分的活塞K1,持续一段通时间的氮气再关闭K1,这样做的目的是_________________________________________________________________。
(2)写出A瓶中Cu与硝酸可能反应的离子方程式______________________________
___________________________________________________________________________。
(3)装置中B瓶的作用是______________________________________。
(4)A中的反应停止后,打开D中的活塞K2,并通入氧气,若反应确有NO产生,则D中应出现的现象是__________________________________________________________。
(5)为减少测量误差,在A中反应完成和D中出现现象后,还应继续进行的操作是_
_____________________________________________________________________________。
(6)C装置烧瓶中的物质是_______________________,用简单的实验证实你的判断:_____________________________________________________________________________。
(7)实验已测出一定质量的铜银合金完全反应后E装置的生成物中含氮元素的质量,为确定合金中铜的质量分数还需测定的数据是____________________________________。
(8)若实验只测定Cu的质量分数,不验证NO的产生,则在铜银合金与浓硝酸反应后,只需简单的实验操作就可达到目的,请简述实验过程:___________________________
_____________________________________________________________________________。
17.将0.2molKMnO4在一定温度下加热后生成amolO2;将剩余固体与过量浓盐酸混合加热又生成bmolCl2,此时锰元素均以Mn2+形式存在。若a + b = m,则m的值可能为
A.0.35 B.0.45 C.0.50 D.0.60
16. 根据量子力学计算,氮化碳结构有五种,其中
根据量子力学计算,氮化碳结构有五种,其中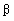 -氮化碳硬度超过金刚石晶体,成为首屈一指的超硬新材料,已知氮化碳的二维晶体结构如右图所示,虚线框内表示晶体结构。下列有关氮化碳的说法正确的是
-氮化碳硬度超过金刚石晶体,成为首屈一指的超硬新材料,已知氮化碳的二维晶体结构如右图所示,虚线框内表示晶体结构。下列有关氮化碳的说法正确的是
A.β-氮化碳属于分子晶体
B.每个碳原子与四个氮原相连,每个氮原子与三个碳原子相连
C.碳化氮的化学式为C4N3
D.左上角和右下角框内晶胞中均含有四个氮原子和三个碳原子
15.据2006年12月28日CCTV-1新闻联联播报道,韩国最近研制了新型的大容量燃料电池,能供电脑等用电器连续使用160小时。其工作原理是:甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路,质子经内电路到达另一极与氧气反应,电池总反应式为:2CH3OH + 3O2 → 2CO2 + 4H2O。下列关于该电池的分析:①H+向负极移动;②负极反应:CH3OH - 6e- + H2O = CO2 + 6H+ ;③1molCH3OH完全反应转移12mol电子;④正极反应:O2 + 4e- + 12H2O = 4OH- 。其中正确的是
A.①⑤ B.①②③④ C.② D.③④
14.Some properties elements belonging to the short periods are listed in the following table.Which of the following statements is true?
|
Element No. |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
|
Atonic
radius(10-9m) |
0.74 |
1.52 |
1.60 |
1.10 |
0.99 |
0.75 |
1.86 |
0.82 |
|
Highest/lowest
valence |
-2 |
+1 |
+2 |
+5 -3 |
+7 -1 |
+5 -3 |
+1 |
+3 |
A.②号元素和③号元素位于同一周期
B.⑦号元素和⑧号元素位于同一周期
C.④号元素的原子序数大于⑥号元素的原子序数
D.⑤号元素最高价氧化物的水化物的酸性比其他7种元素的相应化合物都强
13.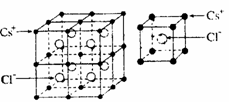 CsCl晶体结构如图所示,对相距最近的两个Cs+与它最近的Cl-之间的夹角的判断正确的是
(D)
CsCl晶体结构如图所示,对相距最近的两个Cs+与它最近的Cl-之间的夹角的判断正确的是
(D)
A.120° B.90°
C.109°28′ D.以上均不正确
12.最新报道,绿色农药--信息素已推广使用,这对环境保护有重要意义。有一种信息素的结构简式为CH3(CH2)5CH=CH(CH2)9CHO。下列关于检验该信息素中官能团的试剂和顺序正确的是
A.先加酸性高锰酸钾溶液;后加银氨溶液,微热
B.先加溴水;后加酸性高锰酸钾溶液
C.先加银氨溶液,微热;再另取该物质加入溴水
D.先加入新制氢氧化铜悬浊液,微热;再加入溴水
11.断肠草(Gelsemium)为中国古代必大毒花之一,据记载能“见血封喉”,现代查明它是葫蔓藤科植物葫蔓藤,其中的毒素很多,下列是分离出来的四种毒素的结构式。下列推断不正确的是
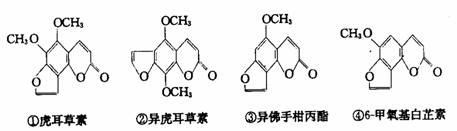
A.①与②;③与④分别互为同分异构体
B.①、③互为同系物
C.①、②、③、④均能与NaOH 溶液反应
D.等物质的量的②、④分别在足量的氧气中完全燃烧,前者消耗氧气比后者多
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com