
13、(1)BaS+CuO+9H2O=Ba(OH)2·8H2O+CuS[也可写Ba(OH)2]
(2)CuS的溶度积比CuO小得多(更难溶),有利于该反应正向进行。
(3)CuS为难溶物(未反应的CuO也不溶),过滤后,将滤液浓缩、冷却,就可在溶液中析出Ba(OH)2·8H2O晶体,故生产效率高;CuS在空气中焙烧氧化可得CuO与SO2,故CuO可反复使用(SO2可用于制硫的化合物),因而成本低。
10、.③④①②;11、略;12、(1)①2SO2+O2+2CaCO3+4H2O=2(CaSO4·H2O)+2CO2或
2SO2+O2+2CaCO3+4H2O=2(CaSO4·H2O)+2CO2
②2SO2+O2+2Ca(OH)2+2H2O=2(CaSO4·2H2O)或2SO2+O2+2Ca(OH)2=2CaSO4+2H2O
(2) Ca(OH)2微溶于水,石灰水中Ca(OH)2浓度小,不利于吸收SO2
9、溶解能力 温度 浓度 沉淀的生成 溶解情况 沉淀溶解平衡移动方向
14.牙齿表面由一层硬的组成为Ca5 (PO4)3OH的物质保护着,它在唾液中存在下列平衡:
Ca5(PO4)3OH(s) 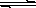 5Ca2++3PO43ˉ+OHˉ
5Ca2++3PO43ˉ+OHˉ
进食后,细菌和酶作用于食物,产生有机酸,这时牙齿就会受到腐蚀,其原因是
已知Ca5(PO4)3F(固)的溶解度比上面的矿化产物更小,质地更坚固。主动脉用离子方程式表示,当牙膏中配有氟化物添加剂后能防止龋齿的原因:
根据以上原理,请你提出一种其它促进矿化的方法:
1-5DAABA;6、难溶电解质;动态平衡;7、可逆过程 沉积和溶解速率相等 各离子浓度不变 改变温度、浓度等条件平衡移动;8、溶度积常数 溶度积 (略)
13.以BaS为原料制备Ba(OH)2·8H2O的过程是:BaS与HCl反应,所得溶液在70℃-90C时与过量NaOH溶液作用,除杂,冷却后得到Ba(OH)2·8H2O晶体。据最新报道,生产效率高、成本低的Ba(OH)2·8H2O晶体的新方法是使BaS与CuO反应……
①.新方法的反应方程式为:
②.该反应反应物CuO是不溶物,为什么该反应还能进行:
③.简述新方法生产效率高、成本低的原因。
12.己知碳酸钙和氢氧化钙在水中存在下列溶解平衡Ca(OH)2(s)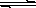 Ca2++2OHˉ,CaCO3(s)
Ca2++2OHˉ,CaCO3(s)
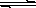 Ca2++CO32ˉ。在火力发电厂燃烧煤的废气中往往含有SO2、O2、N2,CO2等,为了除去有害气体SO2变废为宝,常常见粉末状的碳酸钙或熟石灰的悬浊液洗涤废气,反应产物为石膏。
Ca2++CO32ˉ。在火力发电厂燃烧煤的废气中往往含有SO2、O2、N2,CO2等,为了除去有害气体SO2变废为宝,常常见粉末状的碳酸钙或熟石灰的悬浊液洗涤废气,反应产物为石膏。
(1)写山上述两个反应的化学方程式:
①SO2与CaCO3悬浊液反应
②SO2与Ca(OH)2悬浊液反应
(2)试说明用熟石灰的悬浊液而不用澄清石灰水的理由
11.已知在室温时,Cu(OH)2的溶度积Ksp=2.2×10ˉ20 mol3·Lˉ3,求室温下Cu(OH)2饱和溶液中Cu2+和OHˉ的物质的量浓度。
10.将足量BaCO3分别加入:① 30mL 水 ②10mL 0.2 mol·Lˉ1Na2CO3溶液 ③50mL 0.01 mol·Lˉ1氯化钡溶液 ④100mL 0.01 mol·Lˉ1盐酸中溶解至溶液饱和。请确定各溶液中Ba2+的浓度由大到小的顺序为: _____
9.溶度积KSP反映了难溶电解质在水中的__ ______ ___,KSP的大小和溶质的溶解度不同,它只与__ ______ 有关,与__ ______ 无关。利用溶度积KSP可以判断 ______ __、__ ______ __以及__ _____ _ __。
8.难溶电解质在水中存在沉淀溶解平衡,其平衡常数称为_______ __,简称_______ __。请写出PbI2 、 Cu(OH)2 、 BaSO4 、 CaCO3 、 Al(OH)3 、 CuS的沉淀溶解平衡与溶度积KSP表达式:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com