
7.难溶电解质在水中的沉淀溶解平衡和化学平衡、电离平衡一样,合乎平衡的基本特征、满足平衡的变化基本规律,其基本特征为:
(1)________ ____ (2)__ ______ ____
(3)________ ____ (4)________
6.一些电解质如BaSO4在水中只能溶解很少、可以说是难以溶解,所以称为
______________。尽管这些电解质难以溶解于水中,但在水中也会建立一种________ _____。
5.为除去MgCl2酸性溶液中的Fe3+,可在加热搅拌的条件下,加入一种试剂,过滤后再加入适量盐酸,这试剂不可以是:
A.NH3·H2O B.MgO C.Mg(OH)2 D.MgCO3
4.除去KCl中的K2CO3应选用下列哪种物质:
A.H2SO4 B.HCl C.HNO3 D.三者均可
3.有关AgCl沉淀的溶解平衡说法正确的是:
A.AgCl沉淀生成和沉淀溶解不断进行,但速率相等
B.AgCl难溶于水,溶液中没有Ag+和Clˉ
C.升高温度,AgCl沉淀的溶解度不变
D.向AgCl沉淀中加入NaCl固体,AgCl沉淀的溶解度不变
2.一定温度下,在氢氧化钡的悬浊液中,存在氢氧化钡固体与其它电离的离子间的溶解平衡关系:Ba(OH)2(s) 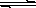 Ba2++2OHˉ。向此种悬浊液中加入少量的氢氧化钡粉末,下列叙述正确的是:
Ba2++2OHˉ。向此种悬浊液中加入少量的氢氧化钡粉末,下列叙述正确的是:
A.溶液中钡离子数目减小 B.溶液中钡离子浓度减少
C.溶液中氢氧根离子浓度增大 D.pH减小
1.试验室中,要使AlCl3溶液中的全部沉淀出来,最适宜选用的试剂是
A.Ba(OH)2溶液 B.NaOH溶液 C.盐酸 D.氨水
22.不正确。强酸强碱组成的盐是不水解,但其水溶液不一定呈中性,如NaHSO4就可在溶液中电离出H+使溶液呈酸性。
20.
 Al3+ +3H2O
Al(OH)3+
3 H+ Al3+
+3 HCO3-
Al(OH)3↓+3CO2↑
Al3+ +3H2O
Al(OH)3+
3 H+ Al3+
+3 HCO3-
Al(OH)3↓+3CO2↑
 21 CO32-+ H2O HCO3-+
OH-与铵台氮肥混用会逸出NH3而损失肥效。
21 CO32-+ H2O HCO3-+
OH-与铵台氮肥混用会逸出NH3而损失肥效。
14. ⑴ < ; ⑵ > ; ⑶ >; ⑷ >;15.增强,增强。16.冷,稀盐酸,抑制FeCl3水解。17.(1)抑制Fe2+水解(2)防止Fe2+氧化;18.酸性,电离出H+,(NH4)2 SO4水解出H+。19.现象是产生白色沉淀,且红色褪去,原因是在纯碱溶液中,CO32-水解,加入BaCl2溶液后,Ba2+ + CO32-=,BaCO3↓白色,由于c(CO32-)减小,CO32-水解平衡向左移动,c(OH-)减少,酚酞褪色。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com