
2、化学变化
实质:发生变化时,构成物质的粒子重新组合成其它物质。
特别注意:化学变化常伴有光、热、气体、沉淀产生或颜色、气味改变等,可参照这些现象来判断有无化学变化发生,但要注意有些物理变化也常伴有发光(电灯)、放热(摩擦)、放出气体(启开汽水瓶盖)、颜色变化(氧气变成液态氧)。
世界是由物质组成的,物质是不断运动和变化的。物质的变化分为物理变化和化学变化。
1、物理变化
实质:从宏观上看,是物质的状态、形状发生改变,从微观上看,是构成物质的粒子(分子、原子或离子)之间的间隔发生了改变。而粒子本身没有改变。
注意:扩散、聚集、膨胀、压缩、挥发、升华、摩擦生热、铁变磁铁、通电升温发光、活性炭吸附等都是物理变化,但同素异形体间的转化(如石墨在一定条件下变成金刚石)就不是物理变化,而是化学变化;生石灰在空气中变为粉末,从表面看是发生了形状变化,但实质上变成了熟石灰,生成了新物质,所以不属于物理变化,而是化学变化。
27.(6分)
现有Fe、Cu组成的合金,其中Cu、Fe的总物质的量为a mol,Cu的物质的
量分数为x;研成粉末后,全部投入含b mol。HNO 的稀溶液中,微热使其充分反应,
的稀溶液中,微热使其充分反应,
且硝酸的还原产物只有NO,试回答下列问题:
(1)若剩余的残渣只有cu,则溶液中含有的金属离子为 。(写出所有可能情况)
(2)当溶液中金属离子只有Fe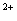 、Cu
、Cu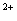 时,则b的取值范围是(用a、x表示)
时,则b的取值范围是(用a、x表示)
(3)当x=0.5,溶液中Fe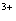 与Fe
与Fe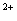 的物质的量相等时,在标准状况共产生672mL气体。
的物质的量相等时,在标准状况共产生672mL气体。
求a、b的值。(要有必要的计算过程)
25.(8分)A~J分别表示中学化学中常见的物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出),且已知G为某主族元素的氧化物,A、B、C、D、E、F六种物质中均含同一种元素。请回答:
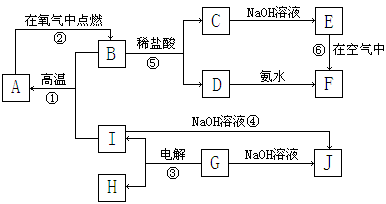
(1)A、B、C、D、E、F六种物质中,所含的相同元素位于周期表中位置
(2)反应①的化学方程式为 ;
(3) 写出反应③的电极方程式:
(4)反应 ⑥的现象
(5)从能量变化的角度看,①②③反应中属于△H<0的反应是___________。(填序号)
26(10分)(1)某学生用实验室常见的酸、碱、盐和金属为反应物,并利用一个底部有小孔的试管和一个广口瓶组装成如图所示的替代简易气体发生器的即开即停装置,该装置中装有铜丝网隔板,利用该装置可制取哪些气体 .若将铜丝网隔板改为铁丝网隔板,则该装置可用于制取何种气体 .写出反应的离子方程式
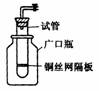
(2)某同学欲断定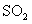 和
和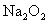 反应中是否有氧气生成,拟使用下列装置进行实验.
反应中是否有氧气生成,拟使用下列装置进行实验.
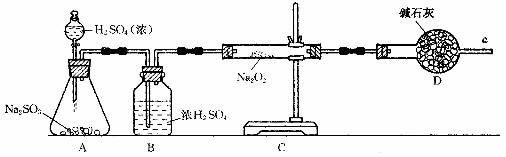
① D的作用是 .
②为确认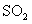 和
和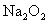 反应产物,该同学设计了以下实验步骤,你认为应进行的操作按顺序排列是(填序号)
.
反应产物,该同学设计了以下实验步骤,你认为应进行的操作按顺序排列是(填序号)
.
A.用带火星的细木条靠近干燥管口a,观察细木条是否着火燃烧.
B.将C装置中反应后的固体物质溶于适量水配成溶液.
C.在配成的溶液中加入用硝酸酸化的硝酸钡溶液,观察是否有沉淀生成.
D.在配成的溶液中先加入盐酸,再加入氯化钡溶液,观察是否有气泡或沉淀生成
24、(9 分)X、Y、Z、W四种短周期元素,原子序数依次递增,X原子形成的阳离子是一个质子,Y原子的最外层电子数是其次外层电子数的2倍,Z原子的最外层电子数与Y 原子的核外电子总数相等,w在同周期元素中原子半径最大。x、z、w三种元素可形成化合物甲,Y,z、w三种元素可形成化合物乙,甲和乙均为中学化学常见物质。请回答:
(1)甲的电子式为 ,乙的化学式为
(2) 的晶体类型为
晶体。X和Z形成
的晶体类型为
晶体。X和Z形成 的过程可用电子式表示为
的过程可用电子式表示为
(3)将3 g Y的单质在足量乙的单质中燃烧,所得气体通人 甲溶液
甲溶液
中,完全吸收后,溶液中的溶质及其物质的量分别为
溶液中所含离子的物质的量浓度由大到小的顺序为
23.(8分)某反应的化学方程式如下(未配平):
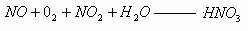
(1) 如果参加反应的氧气中有 被N0还原,则N0与
被N0还原,则N0与 的物质的量之比为
的物质的量之比为
配平该条件下的化学方程式,并用单线桥法标出电子转移的方向和数目;
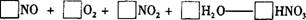
(2)上述反应的化学计量数有多种组合,NO、O2、NO2 的化学计量数之比可以为
(填选项)。A 3:2:4 B 1:1:1 C 4:9:24 D 2:4:3
22、(6分)水是生命之源,也是化学反应中的主角。试回答下列问题:
A、B、C是中学化学常见的三种有色物质(其组成的元素均属短周期元素),摩尔质量依次增大,它们均能与水发生氧化还原反应,但水既不是氧化剂也不是还原剂,请写出A、B、C与水反应的化学方程式:
A+H2O ; B+H2O ;
C+H2O 。
21.(6分)一定量的液体混合物,在一定量的O2中恰好完全燃烧,反应方程式为:XY2(l)+3O2(g)=XO2(g)+2YO2(g) 冷却后,在标况下测得生成物的体积是672mL,密度是2.56g/L。
⑴反应前O2的体积 mL(标况下) ⑵化合物XY2的摩尔质量是 。
⑶若XY2中X、Y两元素的质量比是3:16,则X、Y两元素形成化合物的结构式 。
20.浓度不等的两种硫酸溶液等质量混合后,溶液的质量分数为a%,而等体积混合后,溶液的质量分数为b%;浓度不等的两种氨水等质量混合后,其质量分数为a%,而等体积混合后,溶液的质量分数为c%,那么a、b、c数值的关系是
A. a>b>c B. b>a>c C. c>b>a D. c>a>b
II卷非选择题 共53分
19、把3体积的NO2气体,依次通过下列分别装有①NaHCO3饱和溶液,②浓硫酸,③Na2O2的装置后,用排水法把残留气体收集到集气瓶中,集气瓶内气体应是(同温同压测定)( )
A、1体积NO B、0.5体积O2 C、2体积O2 D、0.25体积O2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com