
1、(2009·达州)在一密闭容器中,有甲、乙、丙、丁四种物质,一定条件下充分反应,测得反应前后各物质的质量如下表:
|
物质 |
甲 |
乙 |
丙 |
丁 |
|
反应前的质量(g) |
20 |
50 |
80 |
30 |
|
反应后的质量(g) |
0 |
100 |
10 |
x |
请根据质量守恒定律判断x的值( )
A.50 B.40 C.10 D.70
6、验证实验:当有气体参加反应或有气体生成时,该反应必须在密闭容器内进行才能验证质量守恒定律。
[例4]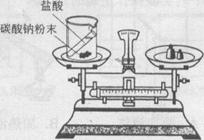 (2008·昆明)(1)某同学按下图装置对质量守恒定律进行实验探究,观察到反应后天平不平衡,该反应符合质量守恒定律(填“符合”或“不符合”),理由是
。
(2008·昆明)(1)某同学按下图装置对质量守恒定律进行实验探究,观察到反应后天平不平衡,该反应符合质量守恒定律(填“符合”或“不符合”),理由是
。
(2)由质量守恒定律可知,化学反应前后,一定不变的是 (填序号)。
①原子种类 ②原子数目 ③分子种类
④分子数目 ⑤元素种类 ⑥物质种类
(3)硝酸在工业生产中且有广泛的应用.工业上制取硝酸的关键反应为:  ,其中R的化学式为
。
,其中R的化学式为
。
[答案](1) 反应生成的CO2气体逸出,导致天平不平衡(2) ①②⑤(3)H2O
[解析]盐酸与碳酸钠反应生成了二氧化碳,二氧化碳逸出,致使天平不平衡。反应前后原子的种类、数目,及元素种类不会发生改变,但分子的种类,分子数目,及物质的种类,可能会发生变化,根据这条原则,可求出R的化学式为H2O。
[规律小结]化学反应是构成反应物分子的原子重新组合转变成生成物分子的过程。在化学反应中,反应前后原子的种类没有改变,原子的数目没有增减,原子的质量没有改变。
变式训练四
5、适用范围:所有的化学变化。
4、利用原子、分子知识解释质量守恒原因
解释“质量守恒”要从化学反应的实质去分析,由分子构成的物质在化学反应中的实质是:分子分裂成原子,原子从新组合成分子,分子聚集成新物质。 在化学反应中,不论物质分子经过怎样的变化,但反应前后原子种类和数目都不变,各原子质量也不变。所以,反应前后的质量总和必然相等。
3、运用质量守恒定律解释实验现象的一般步骤:①说明化学反应的反应物和生成物;②根据质量守恒定律,应该是参加化学反应的各物质质量总和等于各生成物质量总和③与题目中实验现象相联系,说明原因。
2、 质量守恒的理解 反越位和生成物的总质量不变
质量守恒的理解 反越位和生成物的总质量不变
 宏观
宏观
元素的种类不变
 (1)五个不变
原子的种类不变
(1)五个不变
原子的种类不变
微观 原子的数目不变
原子的质量不变
 宏观:物质的种类一定改变
宏观:物质的种类一定改变
(2)两个一定改变
微观:分子的种类一定改变
(3)可能改变:分子总数可能改变。
1、基本内容:参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。
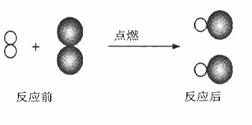
3、(2009·临沂)如果用“ ”表示氢原子,用“
”表示氢原子,用“  ”表示氯原子,如右图所示。请用化学方程式表示这个反应 ,该反应类型是
”表示氯原子,如右图所示。请用化学方程式表示这个反应 ,该反应类型是

2、(2008·长沙)下列反应属于化合反应的是 ( )
A、Zn + H2SO4==
ZnSO4+H2↑ B、CaCO3高温CO2↑ + CaO 
 C、CH4 + 2O2点燃CO2 + 2H2O D、S+O2点燃SO2
C、CH4 + 2O2点燃CO2 + 2H2O D、S+O2点燃SO2
1、(2009·东营)某种元素化合价在化学反应前后发生了变化,则该反应为氧化还原反应。据此可判断下列化学反应属于氧化还原的有( )
A.ZnO+H2SO4=ZnSO4+H2O
B.Fe2O3+3CO====2Fe+3CO2
C.Na2CO3+2HCl=2NaCl+H2O+CO2↑ D.CaCO3 高温 CaO+CO2↑
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com