
16.(10分)  浓H2SO4和木炭在加热时发生反应的化学方程式是
浓H2SO4和木炭在加热时发生反应的化学方程式是
 2H2SO4(浓)+C
2H2SO4(浓)+C  CO2↑+2H2O+2SO2↑
CO2↑+2H2O+2SO2↑
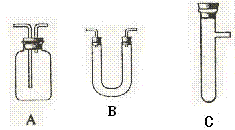
 请从右图中选用所需的仪器(可重复选用)组成一套进行该反应并要检出反应产物的装置。现提供浓H2SO4、木炭和酸性KMnO4溶液,其他固、液试剂自选。(连接和固定仪器所用的玻璃管、胶管、铁夹、铁架台及加热装置等均略去)
请从右图中选用所需的仪器(可重复选用)组成一套进行该反应并要检出反应产物的装置。现提供浓H2SO4、木炭和酸性KMnO4溶液,其他固、液试剂自选。(连接和固定仪器所用的玻璃管、胶管、铁夹、铁架台及加热装置等均略去)
 将所选的仪器连接顺序由上至下依次填入下表,并写出该仪器中应加试剂的名称及其作用。(提示:可以填满,可不填满)
将所选的仪器连接顺序由上至下依次填入下表,并写出该仪器中应加试剂的名称及其作用。(提示:可以填满,可不填满)
选用的仪器 (填字母) (填字母) |
加入的试剂 |
作用 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
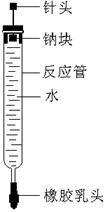
15.(10分)(I)用化学方程式解释下列有关实验现象:
(1)两只棉球分别滴有浓氨水和浓盐酸放入同一只烧杯中,用表面皿盖住烧杯口,烧杯内有白烟: ▲ ;
(2)氯化亚铁溶液中通入氯气,溶液颜色变为棕黄色: ▲ ;
(3)铜粉加入浓硝酸溶液后产生红棕色气体(标出电子转移的方向和数目): ▲ ;
(II)下列物质:①氯气 ②醋酸 ③铜 ④烧碱 ⑤硝酸钾 ⑥二氧化硫 ⑦自来水 ⑧蔗糖(用编号回答)其中属于电解质的有 ▲ 。
14.向50mL 1mol/L AlCl3溶液中加入1.5mol/L NaOH溶液amL,充分反应后,生成沉淀0.02mol,则a的数值可能是
A.40 B.65 C.90 D.120
第Ⅱ卷(共52分)
13.苹果汁是人们喜爱的饮料。由于饮料中含有 Fe2+ 离子,现榨的苹果汁在空气中会由淡绿色变为棕黄色,使Fe2+转变为Fe3+离子。若榨苹果汁时加入维生素C,会可有效防止这种现象的发生。这说明维生素C具有:
A.氧化性 B.还原性 C.酸性 D.碱性
12.在无色溶液中,下列离子能大量共存的是:
A.Na+ 、NH4+ 、NO3-、MnO4- B.K +、SO42-、OH-、AlO2-
C.K + 、Fe3+ 、Cl-、Br- D.Ba2+ 、Na+ 、OH-、CO32-
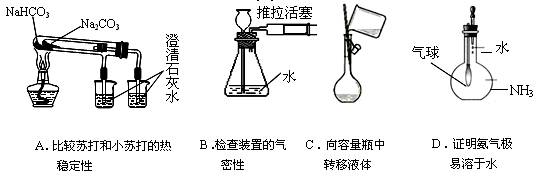
11.下列实验装置图所示的实验操作,不能达到相应实验目的的是
10.用坩埚钳夹住一小块刚用酸充分处理过的铝箔,在酒精灯上加热至熔化,发现熔化的铝并不滴落。下列关于上述实验现象的解释正确的是
A.火焰温度太低不能使铝燃烧 B.铝在空气中能很快形成氧化膜
C.氧化铝的熔点比铝的熔点高 D.用酸处理时未能将氧化铝溶解
9.下列实验方案设计中,可行的是
A.加稀盐酸后过滤,除去混在铜粉中的少量镁粉和铁粉
B.用萃取的方法分离汽油和煤油
C.用溶解和过滤的方法分离硝酸钾和氯化钠固体混合物
D.将O2和H2的混合气体通过灼热的氧化铜,以除去其中的H2
8.配制100 mL浓度为0.5mol/L CuSO4溶液过程中,下列部分实验操作正确的是
A.称取8.0g CuSO4固体放入烧杯中,加入100 mL蒸馏水,并不断搅拌至固体溶解
B.称取8.0g CuSO4固体,放入100 mL容量瓶中,加入蒸馏水使固体溶解,再加入水到刻度,盖好瓶塞,反复摇匀
C.称取8.0g CuSO4固体,放入100 mL量筒中,加入蒸馏水,待固体完全溶解后用蒸馏水稀释至100 mL
D.称取12.5g CuSO4.5H2O固体放入烧杯中,加入适量蒸馏水溶解,冷却后将烧杯中溶液注入100 mL容量瓶后,用少量蒸馏水洗涤烧杯内壁2-3次
7.设NA表示阿伏加德罗常数,下列叙述中正确的是
A.17g氨气中所含原子数为NA
B.标准状况下,1 L水中所含分子数为NA
C.常温常压下,16 g O2含有的氧原子数为NA
D.0.3 mol /L的MgCl2溶液中含Cl-数目0.6 NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com