
22ЃЎOn my birthday I got a watch from my uncle, ЁЁЁЁЁЁЁЁЁЁwas made in Japan.
ЁЁЁЁЁЁ AЃЎwhoЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎthatЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎwhichЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎwhat
ЕквЛНкЃКЕЅЯюЬюПе(ЙВ15аЁЬтЃЌУПаЁЬт1ЗжЃЌТњЗж15Зж
ДгAЁЂBЁЂCЁЂDЫФИібЁЯюжаЃЌбЁГіПЩвдЬюШыПеАзДІЕФзюМббЁЯюЃЌВЂдкД№ЬтПЈЩЯНЋИУбЁЯюЕФБъКХЭПКкЁЃ
21ЃЎ-My best friendЁЏs in a bad mood.
ЁЁЁЁЁЁ -How about ЁЁЁЁЁЁЁЁЁЁher some flowers?
ЁЁЁЁЁЁ AЃЎgivingЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎgivenЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎto giveЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎgive
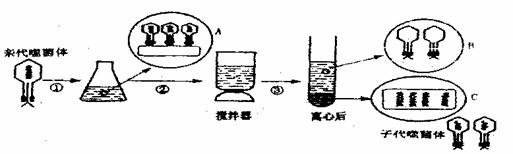
34ЃЎ(12Зж)ЯТЭМЮЊгУКЌ32PЕФT2ЪЩОњЬхЧжШОДѓГІИЫОњ(T2ЪЩОњЬхзЈадМФЩњдкДѓГІИЫОњЯИАћФк)ЕФЪЕбщЃЌОнЭМЛиД№ЯТСаЮЪЬтЃК
 ЁЁ
ЁЁ
ЁЁ
ЁЁ
ЁЁ (1)ИљОнЩЯЪіЪЕбщЖдЯТСаЮЪЬтНјааЗжЮіЃКЭМжазЖаЮЦПЕФХрбјвКЪЧгУРДХрбјЁЁЁЁЁЁЁЁ ЃЌЦфФкЕФгЊбјГЩЗжжаЪЧЗёКЌга32PЁЁЁЁЁЁЁЁ ЃП
ЁЁ (2)ЖдЯТСаПЩФмГіЯжЕФЪЕбщЮѓВюНјааЗжЮіЃК
ЁЁЁЁЁЁЁЁ ЂйВтЖЈЗЂЯждкНСАшРыаФКѓЕФЩЯЧхвКжаКЌга0.8%ЕФЗХЩфадЃЌзюПЩФмЕФдвђЪЧ
ЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЂкЕБНгжжЪЩОњЬхКѓХрбјЕФЪБМфЙ§ГЄЃЌЗЂЯждкНСАшРыаФКѓЕФЩЯЧхвКжавВгаНЯЧПЗХЩфадЃЌЦфзюПЩФмЕФдвђЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (3)ЧыФуЩшМЦвЛИіИјT2ЪЩОњЬхБъМЧЩЯ32PЕФЪЕбщЃК
ЁЁЁЁЁЁЁЁ ЂйЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЂкЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁЁЁ ЂлЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
33ЃЎ(7Зж)ШЫЬхЮЌГжФкЛЗОГЕФЯрЖдЮШЖЈЃЌЖдЯИАће§ГЃЩњУќЛюЖЏЗЧГЃживЊЁЃЧыЛиД№ЯТСаЮЪЬтЁЃ
ЁЁ (1)ШЫЬхФкЛЗОГЭЈЙ§ЁЁЁЁЁЁЁЁ ЕїНкКЭЁЁЁЁЁЁЁЁЁЁ ЕїНкЪЕЯжЯрЖдЮШЖЈЁЃ
ЁЁ (2)ШЫЬхФкЛЗОГжївЊАќРЈЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (3)ЬхЮТЯрЖдКуЖЈЪЧБЃжЄФкЛЗОГЮШЖЈЕФвЛИіживЊЧАЬсЁЃЬхЮТЕїНкжаЪрЮЛгкЁЁЁЁЁЁЁЁ ЃЌЮТЖШИаЪмЦїЮЛгкЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЩЯЁЃгыЬхЮТЕїНкжБНгЯрЙиЕФСНжжМЄЫиЪЧЁЁЁЁЁЁЁЁЁЁ КЭЁЁЁЁЁЁЁЁЁЁ ЁЃ
32ЃЎ(8Зж)ЧыЛиД№ЯТСагаЙивХДЋаХЯЂДЋЕнЕФЮЪЬтЁЃ
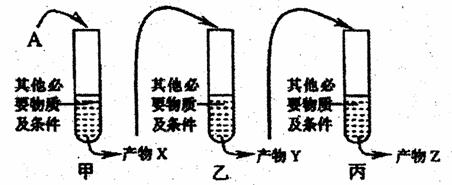
ЁЁ (1)ЮЊбаОПФГВЁЖОЕФжТВЁЙ§ГЬЃЌдкЪЕбщЪвжазіСЫШчЯТЭМЫљЪОЕФФЃФтЪЕбщЁЃ
 ЁЁ
ЁЁ
ЁЁ
ЁЁ
ЂйДгВЁЖОжаЗжРыЕУЕНЮяжЪAЁЃвбжЊAЪЧЕЅСДЕФЩњЮяДѓЗжзгЃЌЦфВПЗжМюЛљађСаЮЊ-GAACAUGUU-ЁЃНЋЮяжЪAМгШыЪдЙмМзжаЃЌЗДгІКѓЕУЕНВњЮяXЁЃОВтЖЈВњЮяXЕФВПЗжМюЛљађСаЪЧ-CTTGTACAA-ЃЌдђЪдЙмМзжаФЃФтЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁ Й§ГЬЁЃ
ЂкНЋЬсДПЕФВњЮяXМгШыЪдЙмввЃЌЗДгІКѓЕУЕНВњЮяYЁЃВњЮяYЪЧФмгыКЫЬЧЬхНсКЯЕФЕЅСДДѓЗжзгЃЌдђВњЮяYЪЧЁЁЁЁЁЁЁЁ ЃЌЪдЙмввжаФЃФтЕФЪЧЁЁЁЁЁЁЁЁЁЁ Й§ГЬЁЃ
ЂлНЋЬсДПЕФВњЮяYМгШыЪдЙмБћжаЃЌЗДгІКѓЕУЕНВњЮяZЁЃВњЮяZЪЧзщГЩИУВЁЖОЭтПЧЕФЛЏКЯЮяЃЌдђВњЮяZЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (2)ШєИУВЁЖОИаШОСЫаЁЪѓЩЯЦЄЯИАћЃЌдђзщГЩзгДњВЁЖОЭтПЧЕФЛЏКЯЮяЕФдСЯРДздЁЁЁЁЁЁ ЃЌЖјОіЖЈИУЛЏКЯЮяКЯГЩЕФвХДЋаХЯЂРДздЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃИУВЁЖОБэУцЕФвТПЧЕФзїгУЪЧ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
30ЃЎ(15Зж)2009Фъ12дТ7ШежС18ШедкИчБОЙўИљейПЊЕФЪРНчЦјКђДѓЛсЃЌСљЪЎЖрИіЙњМвЕФСьЕМШЫГіЯЏСЫЛсвщЃЌЬхЯжСЫЦјКђБфЛЏдНРДдНв§Ц№ШЫУЧЕФжиЪгЁЃдкетДЮЛсвщжаЃЌШчКЮНЕЕЭДѓЦјжаCO2ЕФКЌСПМАгааЇЕиПЊЗЂРћгУCO2ЃЌГЩЮЊСЫЦфжавЛИіживЊЕФвщЬтЁЃ
 ЁЁ
ЁЁ
ЁЁ
ЁЁ
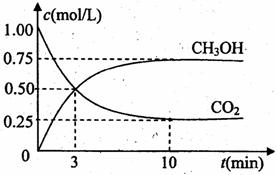
ЁЁ (1)ФПЧАЙЄвЕЩЯгавЛжжЗНЗЈЪЧгУCO2РДЩњВњШМСЯМзДМЁЃЮЊЬНОПЗДгІдРэЃЌЯжНјааШчЯТЪЕбщЃЌдкЬхЛ§ЮЊ1LЕФУмБеШнЦїжаЃЌГфШы1molCO2КЭ3molH2ЃЌвЛЖЈЬѕМўЯТЗЂЩњЗДгІЃК
 ЁЁЁЁЁЁЁЁ CO2(g)+3H2(g)ЁЁЁЁЁЁ CH3OH(g)+H2O(g)ЃЛЁїH=-49.0kJ/mol
ЁЁЁЁЁЁЁЁ CO2(g)+3H2(g)ЁЁЁЁЁЁ CH3OH(g)+H2O(g)ЃЛЁїH=-49.0kJ/mol
ЁЁЁЁЁЁЁЁ ВтЕУCO2КЭCH3OH(g)ЕФХЈЖШЫцЪБМфБфЛЏШчЭМЫљЪОЁЃ
ЁЁЁЁЁЁЁЁ ЂйДгЗДгІПЊЪМЕНЦНКтЃЌЧтЦјЕФЦНОљЗДгІЫйТЪv(H2)=ЁЁЁЁ mol/(LЁЄmin)
ЂкФГвЛЪБПЬЃЌВтЕУЗДгІЗХГіЕФШШСПЮЊ24.5kJЃЌдђДЫЪБCO2ЕФзЊЛЏТЪЮЊЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЂлЯТСаДыЪЉжаФмЪЙn(CH3OH)/n(CO2)діДѓЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
AЃЎЩ§ИпЮТЖШЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎГфШыHe(g)ЃЌЪЙЬхЯЕбЙЧПдіДѓ
CЃЎНЋH2O(g)ДгЬхЯЕжаЗжРыЁЁЁЁЁЁЁЁЁЁ DЃЎдйГфШы1mol CO2КЭ3molH2
ЁЁ (2)дкдиШыКНЬьЦїЕФЩњЬЌЯЕЭГжаЃЌВЛНівЊЧѓЗжРыШЅГ§CO2ЃЌЛЙвЊЧѓЬсЙЉГфзуЕФO2ЁЃФГжжЕчЛЏбЇзАжУПЩЪЕЯжШчЯТзЊЛЏЃК2CO2=2CO+O2ЃЌCOПЩгУзїШМСЯЁЃ
ЁЁЁЁЁЁЁЁ вбжЊИУЗДгІЕФбєМЋЗДгІЮЊЃК4OH--4e-=O2Ёќ+2H2O
ЁЁЁЁЁЁЁЁ дђвѕМЋЗДгІЪНЮЊЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (3)ШчЙћЗДгІБидквЛИіЬхЛ§ПЩБфЕФУмБеШнЦїжаНјааЃЌЦфгрЬѕМўВЛБфЃЌдђДяЕНЦНКтЪБCO2зЊЛЏТЪгы(1)жаЯрБШЁЁЁЁЁЁЁЁЁЁЁЁ (ЬюЁАдіДѓЁБЁЂЁАМѕаЁЁБЁЂЁАВЛБфЁБЛђЁАЮоЗЈШЗЖЈЁБ)
 ЁЁ
31ЃЎ(15Зж)ЙШАБЫсЪЧЩњЮяЬхФкЕФвЛжжживЊЕФгаЛњ
ЁЁ
31ЃЎ(15Зж)ЙШАБЫсЪЧЩњЮяЬхФкЕФвЛжжживЊЕФгаЛњ
аЁЗжзгЃЌЙШАБЫсФЦЪЧЫќЕФФЦбЮЃЌЪЧЮЖОЋЕШЕї
ЮЖЦЗЕФжївЊГЩЗжЃЌФПЧАРћгУЮЂЩњЮяЗЂНЭЩњВњЕФ
АБЛљЫсжаЃЌЙШАБЫсЪЧВњСПзюДѓЕФжжРржЎвЛЁЃ
ЁЁ (1)ЙШАБЫсRЛљЮЊ-CH2-CH2-COOHЃЌ
дђЙШАБЫсЕФЗжзгЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (2)ЙШАБЫсЗЂНЭЕФХрбјЛљГЩЗжЃЌжївЊгаЦЯЬбЬЧЁЂ
АБЫЎЁЂСзЫсбЮЁЂЩњЮяЫиЕШЃЌЗЂНЭзАжУШчгв
ЩЯЭМЫљЪОЃЌПЩвдХаЖЯЙШАБЫсАєзДИЫОњЕФаТ
ГТДњаЛРраЭЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁ аЭЁЃФГГЇгУАБЫсАєзДИЫОњЩњВњЙШАБЫсЃЌНсЙћДњаЛВњЮяжаГіЯжСЫДѓСПШщЫсЃЌЦфдвђПЩФмЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (3)ЙШАБЫсЗЂНЭЩњВњЙ§ГЬжаЃЌашвЊЬэМгАБЫЎЃЌЪдЗжЮіЬэМгАБЫЎЕФзїгУПЩФмЪЧЪВУДЃП
ЁЁЁЁЁЁЁЁ ЂйЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЂкЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁ (4)ФГГЇЕФЗЂНЭвКдјВЛЩїБЛЪЩОњЬхЮлШОЃЌОњЬхДѓСПЫРЭіЃЌЕЋШЫУЧШДНФавДгжаЛёЕУСЫВЛЩйПЩЕжПЙЪЩОњЬхЕФаТОњжгЃЌЯИОњетжжаТадзДЕФВњЩњРДздгкЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃвЊЪЙгХСМОњжжгУгкДѓЙцФЃЩњВњЃЌаыбЁгУЁЁЁЁЁЁЁЁЁЁ ЦкЕФОњжжНјааРЉДѓХрбјЁЃ
ЁЁ (5)ЕБЙШАБЫсЕФКЯГЩЙ§СПЪБЃЌОЭЛсвжжЦЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЕФЛюадЃЛДгЖјЕМжТКЯГЩЭООЖжаЖЯЃЌЕБЙШАБЫсвђЯћКФЖјХЈЖШЯТНЕЪБЃЌвжжЦзїгУОЭБЛНтГ§ЃЌИУКЯГЩЗДгІгжжиаТПЊЪМЃЌетжжЕїНкЗНЪННаЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃЮЊСЫНтГ§етжжЕїНкЖдЩњВњЕФгАЯьЃЌдкЩњВњжаВЩгУЕФЪжЖЮЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЃ
ЁЁ (6)СЌајХрбјЪБЃЌвдвЛЖЈЕФЫйЖШВЛЖЯЬэМгаТЕФХрбјЛљЃЌЭЌЪБвдЯрЭЌЕФЫйЖШЗХГіОЩЕФХрбјЛљЃЌДЫЙЄвеСїГЬПЩвдДѓДѓЬсИпЩњВњаЇТЪЃЌЦфдвђЪЧЃК
ЁЁЁЁЁЁЁЁ ЂйЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЂкЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
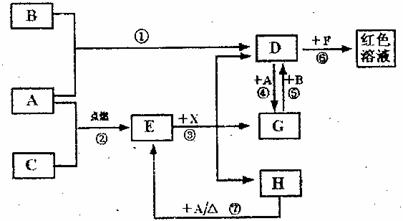
28ЃЎ(19Зж)AЁЂBЁЂCЮЊжабЇГЃМћЕЅжЪЃЌЦфжавЛжжЮЊН№ЪєЃЛЭЈГЃЧщПіЯТAЮЊЙЬЬхЁЂBЮЊЙЬЬхЁЂCЮЊЦјЬхЁЃDЁЂEЁЂFЁЂGЁЂHЁЂXОљЮЊЛЏКЯЮяЃЌЦфжаXЪЧвЛжжЮобѕЧПЫсЁЂEЮЊКкЩЋЙЬЬхЃЌHдкГЃЮТЯТЮЊвКЬхЁЃЫќУЧжЎМфЕФзЊЛЏЙиЯЕШчЭМЫљЪО(ЦфжаФГаЉЗДгІЬѕМўКЭВПЗжЗДгІВњЮявбТдШЅ)ЁЃ
 ЁЁ
ЁЁ
ЁЁ
ЁЁ
ЁЁ (1)аДГіЯТСаЮяжЪЕФЛЏбЇЪНЃКDЁЁЁЁЁЁЁЁ ЃЛXЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (2)дкЗДгІЂй~ЂпжаЃЌВЛЪєгкбѕЛЏЛЙдЗДгІЕФЪЧЁЁЁЁЁЁЁЁЁЁ (ЬюБрКХ)ЁЃ
ЁЁ (3)ЗДгІЂмЕФРызгЗНГЬЪНЮЊЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (4)ЭљGШмвКжаМгШыNaOHШмвКЙлВьЕНЕФЯжЯѓЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (5)ЗДгІЂпЕФЛЏбЇЗНГЬЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
ЁЁЁЁЁЁЁЁ ИУЗДгІжаУПЯћКФ0.3molЕФAЃЌПЩзЊвЦЕчзгЁЁЁЁЁЁЁЁЁЁ molЁЃ
ЁЁ (6)аДГіDЕФШмвКгыаЁЫеДђШмвКЗДгІЕФРызгЗНГЬЪНЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
 ЁЁ
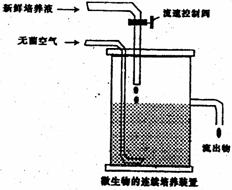
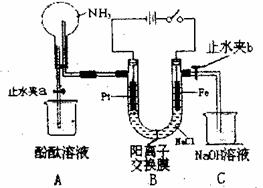
29ЃЎ(16Зж)ФГПЮЭтЛюЖЏаЁзщЩшМЦСЫШчЭМЫљЪОЕФзАжУЃЌгУгкНјааЛКТ§ЕчНтNaClШмвКМАЯрЙиЪЕбщ(ДЫЪБевПЊжЙЫЎМаaЃЌЙиБежЙЫЎМаb)ЁЃгЩгкФГаЉдвђЃЌЪЕбщПЊЪМВЂУЛгаДяЕНдЄЦкЕФФПЕФЃЌЕЋвВПДЕНСЫСюШЫИпаЫЕФЯжЯѓ(бєРызгНЛЛЛФЄжЛдЪаэбєРызгКЭЫЎЕФЭЈЙ§)ЁЃЧыАяЫћУЧЗжЮідвђЃЌШЛКѓЛиД№ЮЪЬтЃК
ЁЁ
29ЃЎ(16Зж)ФГПЮЭтЛюЖЏаЁзщЩшМЦСЫШчЭМЫљЪОЕФзАжУЃЌгУгкНјааЛКТ§ЕчНтNaClШмвКМАЯрЙиЪЕбщ(ДЫЪБевПЊжЙЫЎМаaЃЌЙиБежЙЫЎМаb)ЁЃгЩгкФГаЉдвђЃЌЪЕбщПЊЪМВЂУЛгаДяЕНдЄЦкЕФФПЕФЃЌЕЋвВПДЕНСЫСюШЫИпаЫЕФЯжЯѓ(бєРызгНЛЛЛФЄжЛдЪаэбєРызгКЭЫЎЕФЭЈЙ§)ЁЃЧыАяЫћУЧЗжЮідвђЃЌШЛКѓЛиД№ЮЪЬтЃК
ЁЁ (1)аДГіBзАжУжаЕФЕчМЋЗДгІЃК
ЁЁЁЁЁЁЁЁ вѕМЋЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁЁЁ бєМЋЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁ (2)вЛЖЮЪБМфФквРДЮЙлВьЕНAжаЕФЯжЯѓЮЊЃК
ЁЁЁЁЁЁЁЁ ЂйЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЂкЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЂлЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁ (3)ЕБЙлВьЭъAжаЕФЯжЯѓКѓЃЌДђПЊЫЎжЙ
МаbЁЃдйЙлВьCзАжУЃЌгаЮоУїЯдЯжЯѓЁЁЁЁЁЁ (ЬюЁАгаЁБЛђЁАУЛгаЁБ)ЃЌШєЮоУїЯдЯжЯѓЫЕУїРэгЩЃЌШєгаЯжЯѓЧыаДГігаЙиЗДгІЕФЛЏбЇЗНГЬЪН
ЁЁ (4)ШєЯыДяЕНЕчНтNaClШмвКЕФФПЕФЃЌЧыЖдИУзАжУНјаазюМђЕЅЕФИФНјЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛВЂаДГіЕчНтБЅКЭNaClШмвКЕФРызгЗНГЬЪНЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
27ЃЎ(10Зж)вбжЊ2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10ЁЁЁЁЁЁ ЁЃ
ЁЁЁЁ дкИпУЬЫсМиЫсадШмвККЭВнЫс(H2C2O4ЃЌШѕЫс)ШмвКЗДгІЪБЃЌЗЂЯжПЊЪМвЛЖЮЪБМфЃЌЗДгІЫйТЪНЯТ§ЃЌШмвКЭЪЩЋВЛУїЯдЃЌЕЋВЛОУЭЛШЛЭЪЩЋЃЌЗДгІЫйТЪУїЯдМгПьЁЃ
ЁЁ (1)ЧыаДГіКсЯпЩЯЫљЬюЮяжЪЕФЕчзгЪНЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌИУЗДгІжабѕЛЏМСЪЧ(ЬюУћГЦ)ЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌаДГіВнЫсгызуСПNaOHШмвКЗДгІЕФРызгЗНГЬЪНЃКЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (2)еыЖдЩЯЪіЪЕбщЯжЯѓЃЌФГЭЌбЇШЯЮЊKMnO4гыH2C2O4ЗДгІЪЧЗХШШЗДгІЃЌЕМжТШмвКЮТЖШЩ§ИпЃЌЗДгІЫйТЪМгПьЁЃДггАЯьЛЏбЇЗДгІЫйТЪЕФвђЫиПДЃЌФуЕФВТЯыЛЙПЩФмЪЧЁЁЁЁЁЁ ЕФгАЯьЁЃ
ЁЁ (3)ШєгУвбжЊХЈЖШЕФЫсадKMnO4ШмвКЕЮЖЈЮДжЊХЈЖШЕФH2C2O4ШмвКЃЌдђKMnO4ШмвКгІзАдкЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЬювЧЦїУћГЦ)жаЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com