
7.如图所示,一列简谐横波在x轴上传播,图甲和图乙分别为x轴上a、b两质点的振动图象,且 xab=6m。下列判断正确的是 ( )
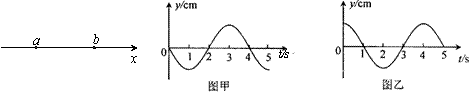
A.波一定沿x轴正方向传播 B.波长可能是8 m
C.波速一定是2 m/s D.波速可能是6 m/s
6.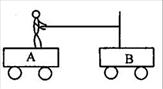 如图所示,光滑的水平面上停放着A、B两辆小车,质量分别为M和m,M>m,两车相距为L,人的质量也是m,另有不计质量的一根硬杆和一根细绳。第一次人站在A车上,杆插在B车上;第二次人站在B车上,杆插在A车上。两种情况下,人用同样大小的力拉绳子,使两车相遇。两次小车从开始运动到相遇的时间分别为t1和t2,则: ( )
如图所示,光滑的水平面上停放着A、B两辆小车,质量分别为M和m,M>m,两车相距为L,人的质量也是m,另有不计质量的一根硬杆和一根细绳。第一次人站在A车上,杆插在B车上;第二次人站在B车上,杆插在A车上。两种情况下,人用同样大小的力拉绳子,使两车相遇。两次小车从开始运动到相遇的时间分别为t1和t2,则: ( )
A. t1=t2 B. t1<t2 C. t1>t2 D.条件不足,无法判断
5.太阳围绕银河系中心的运动可视为匀速圆周运动,其运动速度约为地球公转速度的7倍,轨道半径约为地球公转半径的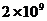 倍,为了粗略估算银河系恒星的数目,可认为银河系中所有恒星的质量都集中在银河系中心,且银河系中恒星的平均质量约等于太阳质量,则银河系中恒星数目约为
( )
倍,为了粗略估算银河系恒星的数目,可认为银河系中所有恒星的质量都集中在银河系中心,且银河系中恒星的平均质量约等于太阳质量,则银河系中恒星数目约为
( )
A. 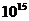 B.
B. 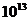 C.
C. 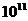 D.
D. 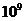
4.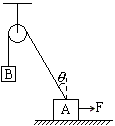 如图所示,AB两物体用跨过光滑定滑轮的轻绳相连,A的质量大于B的质量,A放置在水平地板上,在水平向右的外力F作用下沿地板一直向右运动,与地板的动摩擦因数是常数,B物体匀减速上升。设A受绳的拉力为T,受地面的弹力为N,受摩擦力为f。以下判断正确的是( )
如图所示,AB两物体用跨过光滑定滑轮的轻绳相连,A的质量大于B的质量,A放置在水平地板上,在水平向右的外力F作用下沿地板一直向右运动,与地板的动摩擦因数是常数,B物体匀减速上升。设A受绳的拉力为T,受地面的弹力为N,受摩擦力为f。以下判断正确的是( )
A.T不变,f逐渐增大; B.T逐渐减小,N逐渐增大;
C.N逐渐减小,T不变; D.f逐渐减小,T逐渐减小。
3.在2008北京奥运会上,俄罗斯著名撑杆跳运动员伊辛巴耶娃以5.07m的成绩第24次打破世界纪录。图为她在比赛中的几个画面。下列说法中正确的是 ( )
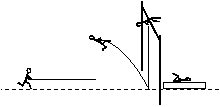 A.运动员过最高点时的速度为零
A.运动员过最高点时的速度为零
B.撑杆恢复形变时,弹性势能完全转化为动能
C.运动员要成功跃过横杆,其重心必须高于横杆
D.运动员在上升过程中对杆先做正功后做负功
2.作匀变速直线运动的物体,依次通过A、B、C三点,位移SAB=SBC ,已知物体在AB段的平均速度为3 m/s,在BC段的平均速度大小为6 m/s,那么物体经过B点的瞬时速度大小为( )
A.4 m/s B.4.5 m/s C.5 m/s D.5.5 m/s。
1.下列有关物体内能和分子势能的说法正确的是 ( )
A.对质量一定的某种气体,若体积发生变化,则它的内能一定改变
B.质量相等、温度相同的氢气和氧气,若不考虑分子间的势能,则它们的内能相等
C.当两个分子间的距离r等于它们平衡位置时的距离r0时,两分子间的势能最小
D.当两个分子间的距离r小于它们平衡位置时的距离r0时,将r逐渐增大到10 r0的过程中,两分子间的势能先增大后减小
23.常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
|
实验编号 |
HA物质的量 浓度(mol·L-1) |
NaOH物质的量 浓度(mol·L-1) |
混合溶液的pH |
|
甲 |
0.2 |
0.2 |
pH=a |
|
乙 |
C1 |
0.2 |
pH=7 |
|
丙 |
0.2 |
0.1 |
pH>7 |
|
丁 |
0.1 |
0.1 |
pH=9 |
请回答:
(1) 不考虑其它组的实验结果,单从甲组情况分析,
若a 7(填>、<或=),则HA为强酸;
若a 7(填>、<或=),则HA为弱酸。
(2)在乙组中混合溶液中离子浓度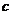 (A-)与
(A-)与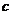 (Na+)的大小关系是
。
(Na+)的大小关系是
。
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,HA是 酸(选填“强”或“弱”)。
该混合溶液中离子浓度由大到小的顺序是
。
(4)丁组实验所得混合溶液中由水电离出的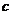
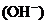 =
mol·L-1。
=
mol·L-1。
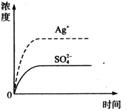 24.已知Ag2SO4的KSP为2.0×10-5,将适量Ag2SO4固体溶于100mL水中至刚好饱和,该过程中Ag+和
24.已知Ag2SO4的KSP为2.0×10-5,将适量Ag2SO4固体溶于100mL水中至刚好饱和,该过程中Ag+和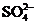 浓度随时间变化关系如右图(饱和Ag2SO4溶液中
浓度随时间变化关系如右图(饱和Ag2SO4溶液中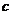 (Ag+)=0.034mol·L-1)。若
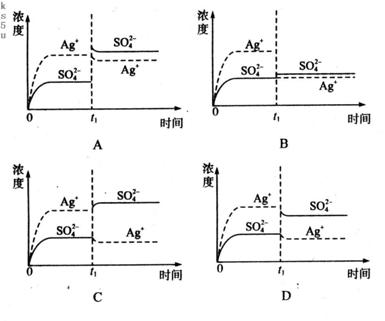
(Ag+)=0.034mol·L-1)。若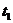 时刻在上述体系中加入100mL
0.020mol·L-1 Na2SO4溶液,下列示意图中,能正确表示
时刻在上述体系中加入100mL
0.020mol·L-1 Na2SO4溶液,下列示意图中,能正确表示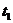 时刻后Ag+和
时刻后Ag+和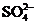 浓度随时间变化关系的是
。
浓度随时间变化关系的是
。
山东师范大学附中高三年级第二次模拟练习
22.(1)将等质量的锌粉分别投入10mL 0.1mol•L-1 HCl和10mL 0.1mol•L-1的CH3COOH的溶液中。
①若锌不足量,反应快的是 ;
②若锌过量,产生氢气的量的关系为 。
(2)将等量的锌粉分别投入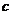 (H+)均为1mol·L-1、体积均为10mL的盐酸和醋酸溶液中。
(H+)均为1mol·L-1、体积均为10mL的盐酸和醋酸溶液中。
①若锌不足量,反应快的是 ;
②若锌过量,产生氢气的量的关系为 。
21.关于酸碱中和滴定
(1)准确量取25.00ml高锰酸钾溶液,选用的仪器是 (酸式或碱式)滴定管。
(2)一只规格为a mL的滴定管,其尖嘴部分充满溶液,管内液面在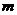 mL处,当液面降到
mL处,当液面降到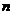 mL处时,流出液体的体积为
ml。
mL处时,流出液体的体积为
ml。
(3)用已知浓度的NaOH溶液测定某H2SO4溶液的浓度,参考下图,从下表中选出正确选项 。
|
|
锥形 瓶中 溶液 |
滴定 管中 溶液 |
选用 指示剂 |
 选用 选用滴定管 |
|
A |
碱 |
酸 |
石蕊 |
(甲) |
|
B |
酸 |
碱 |
酚酞 |
(甲) |
|
C |
碱 |
酸 |
甲基橙 |
(甲) |
|
D |
酸 |
碱 |
酚酞 |
(乙) |
 (4)某学生用0.1mol·L-1的KOH标准溶液滴定未知浓度的盐酸,其操作分解为如下几步:
(4)某学生用0.1mol·L-1的KOH标准溶液滴定未知浓度的盐酸,其操作分解为如下几步:
A.量取20mL待测盐酸注入洁净的锥形瓶,并加入2~3滴酚酞
B.用标准溶液润洗滴定管2~3次
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液
D.取标准KOH溶液注入碱式滴定管至“0”刻度以上1~2cm
E.调节液面至“0”或“0”以下刻度,记下读数
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点并记下滴定管液面的刻度
就此实验完成填写:
①正确操作步骤的顺序是(用序号字母填写) ;
②判断到达滴定终点的实验现象是 ;
③滴定过程中眼睛 ,左手 ,右手 ;
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com