
3.“―÷ΣIΈΣ Β ΐΦ·Θ§M={x|x2 -2xΘΦ0}Θ§N={x|y=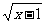 }Θ§‘ρ
}Θ§‘ρ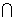 (
(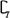 Θ§N)=
Θ§N)=
ΓΓ (A){x|0ΘΦxΘΦ1}ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (B){x|0ΘΦxΘΦ2}
ΓΓ (C){x|xΘΦ1}ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (D)Π’
2.ΓΑa = 2Γ± «ΓΑ÷±œΏax+2y=0”κ÷±œΏx+y=1ΤΫ––Γ±ΒΡ
ΓΓ (A)≥δΖ÷≤Μ±Ί“ΣΧθΦΰΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (B)±Ί“Σ≤Μ≥δΖ÷ΧθΦΰ
ΓΓ (C)≥δ“ΣΧθΦΰΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ (D)Φ»≤Μ≥δΖ÷“≤≤Μ±Ί“ΣΧθΦΰ
1.»τp: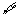 xΓ R,sinx
xΓ R,sinx 1,‘ρ
1,‘ρ
(A)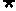 p:
p: 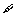 xΓ R,sinxΘΨ1ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
(B)
xΓ R,sinxΘΨ1ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
(B) 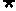 p:
p: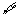 xΓ R,sinxΘΨ1
xΓ R,sinxΘΨ1
(C)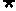 p:
p: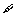 xΓ R,sinx
xΓ R,sinx 1ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
(D)
1ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
(D) 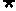 p:
p: 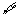 xΓ R,sinx
xΓ R,sinx 1
1
6Θ°(3Ζ÷)ΫΪœ¬Ν–Έο ÷ Ϋχ–– Ζ÷άύΘΚ
Ζ÷άύΘΚ
ΔΌΓΓΓΓ 
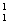 H”κ
H”κ 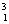 H ΓΓΔΎ O2 ”κO3 ΓΓΔέ““¥Φ”κΦΉΟ―(CH3Θ≠OΘ≠CH3) Δή
H2O ”κ D2OΓΓ
H ΓΓΔΎ O2 ”κO3 ΓΓΔέ““¥Φ”κΦΉΟ―(CH3Θ≠OΘ≠CH3) Δή
H2O ”κ D2OΓΓ
Δί CH3CH2CH2CH3 ”κCH3Θ≠CH(CH3)Θ≠CH3ΓΓ Δό C60 ”κC70ΓΓΔΏ
Δ≈ ΜΞΈΣΆ§ΈΜΥΊΒΡ « ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ(Χν±ύΚ≈Θ§œ¬Ά§)ΘΜ
ΔΤ ΜΞΈΣΆ§ΥΊ“λ–ΈΧεΒΡ «ΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓ
Δ« ΜΞΈΣΆ§Ζ÷“λΙΙΧεΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓ
5Θ°(10Ζ÷)Ϋώ”–“ΜΜλΚœΈοΒΡΥ°»ή“ΚΘ§÷ΜΩ…ΡήΚ§”–“‘œ¬άκΉ”÷–ΒΡ»τΗ…÷÷ΘΚK+ΓΔNH4+ΓΔCl-ΓΔMg2+ΓΔBa2+ΓΔCO32-ΓΔSO42-Θ§œ÷»Γ»ΐΖίΗς100mL»ή“Κ Ϋχ––»γœ¬ Β―ιΘΚ
Ϋχ––»γœ¬ Β―ιΘΚ
ΒΎ“ΜΖίΦ”»κAgNO3»ή“Κ”–≥ΝΒμ≤ζ…ζΓΘ
ΒΎΕΰΖίΦ”ΉψΝΩNaOH»ή“ΚΦ”»»ΚσΘ§ ’Φ·ΒΫ0.08 molΤχΧεΓΘ
ΒΎ»ΐΖίΦ”ΉψΝΩBaCl2»ή“ΚΚσΘ§ΒΟΒΫΗ…‘ο≥ΝΒμ12.54 g,Ψ≠ΉψΝΩ―ΈΥαœ¥Β”ΓΔΗ…‘οΚσΘ§≥ΝΒμ÷ ΝΩΈΣ4.66 g.ΓΘ
ΗυΨί…œ ω Β―ιΘ§ΜΊ¥π“‘œ¬Έ ΧβΘΚ
Β―ιΘ§ΜΊ¥π“‘œ¬Έ ΧβΘΚ
(1)ΓΓΓΓΓΓ ”…ΒΎ“ΜΖίΫχ––ΒΡ Β―ιΆΤΕœΗΟΜλΚœΈο «Ζώ“ΜΕ®Κ§”–Cl-Θ§≤ΔΥΒΟςάμ”…ΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΘ
(2)ΓΓΓΓΓΓ ”…ΒΎΕΰΖίΫχ––ΒΡ Β―ιΒΟ÷ΣΜλΚœΈο÷–”ΠΚ§”–ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ άκΉ”Θ§ΤδΈο÷ ΒΡΝΩ≈®Ε»ΈΣΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
(3)ΓΓΓΓΓΓ ”…ΒΎ»ΐΖίΫχ––ΒΡ Β―ιΩ…÷Σ12.54g≥ΝΒμΒΡ≥…Ζ÷ΈΣΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
«κΦΤΥψ–Έ≥…ΗΟ≥ΝΒμΒΡ‘≠ΜλΚœΈο÷–ΗςάκΉ”ΒΡΈο÷ ΒΡΝΩΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
(4)ΓΓΓΓΓΓ ΉέΚœ…œ ω Β―ιΘ§Ρψ»œΈΣ“‘œ¬Ϋα¬έ’ΐ»ΖΒΡ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
A. ΗΟΜλΚœ“Κ÷–“ΜΕ®Κ§”–ΘΚK+ΓΔNH4+ΓΔCO32-ΓΔSO42-Θ§Ω…ΡήΚ§Cl-
B. ΗΟΜλΚœ“Κ÷–“ΜΕ®Κ§”–ΘΚNH4+ΓΔCO32-ΓΔSO42-Θ§Ω…ΡήΚ§K+ΓΔCl-
C. ΗΟΜλΚœ“Κ÷–“ΜΕ®Κ§”–ΘΚNH4+ΓΔCO32-ΓΔSO42-Θ§ Ω…ΡήΚ§Mg2+ΓΔK+ΓΔCl-
Ω…ΡήΚ§Mg2+ΓΔK+ΓΔCl-
D. ΗΟΜλΚœ“Κ÷–“ΜΕ®Κ§”–ΘΚNH4+ΓΔSO42-Θ§Ω…ΡήΚ§Mg2+ΓΔK+ΓΔCl-
4Θ°(6Ζ÷)‘Ύœ¬ΆΦΥυ ΨΒΡ Β―ιΉΑ÷Ο÷–Θ§A÷– Δ”–ΤΖΚλ»ή“ΚΘ§B  ÷– Δ”–NaOH»ή“ΚΓΘ
÷– Δ”–NaOH»ή“ΚΓΘ
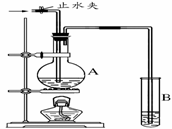
«κΜΊ¥πœ¬Ν–Έ ΧβΘΚ
(1) »τœρA÷–Ά®»κΉψΝΩΒΡΕΰ―θΜ·ΝρΤχΧεΘ§A÷–ΒΡœ÷œσ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
(2) »τœρA÷–Ά®»κΉψΝΩΒΡ¬»ΤχΚσΘ§‘ΌΦ”»»AΘ§A÷–ΒΡ»ή“ΚΓΓΓΓΓΓ (ΧνΓΑΡήΓ±ΜρΓΑ≤ΜΡήΓ±)Μ÷Η¥ΒΫ‘≠ά¥ΒΡ―’…ΪΓΘ
(3) »γΙϊA÷– ΔΒΡ «Α±Υ°Θ§B÷– ΔΒΡ «Έό…ΪΖ”ΧΣ»ή“ΚΘ§ΈΔ»»Θ§B÷–»ή“ΚΜα±δΈΣΚλ…ΪΘ§‘ρ¥Υ ±±μœ÷Α±Υ°ΒΡΜ·―ß–‘÷ ”–Φν–‘ΚΆΓΓΓΓΓΓ –‘ΓΘ
(4) »γΙϊA÷– ΔΒΡ «≈®ΝρΥαΘ§Φ”»κΆ≠Θ§Φ”»»Ζ¥”ΠΘ§¥Υ Ζ¥”Π÷–±μœ÷≈®ΝρΥαΒΡΥα–‘ΚΆΓΓΓΓΓΓ –‘ΓΘ
Ζ¥”Π÷–±μœ÷≈®ΝρΥαΒΡΥα–‘ΚΆΓΓΓΓΓΓ –‘ΓΘ
(5) »γΙϊA÷– ΔΒΡ «―ΈΥαΘ§Φ”»κΆ≠ΖέΘ§ΈΣΝΥ»ΟΆ≠Ζέ»ήΫβΘ§Ω…“‘Φ”»κNaNO3Θ§Ζ¥”ΠάκΉ”ΖΫ≥Χ ΫΈΣΘΚΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
3Θ°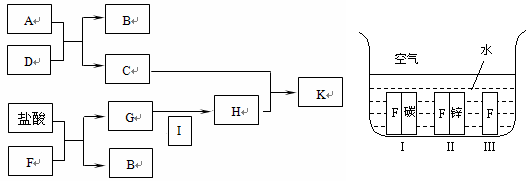 (8Ζ÷)œ¬ΖΫΉσΆΦ÷–A~KΨυΈΣ÷–―ßΜ·―ß÷–≥ΘΦϊΒΡΈο÷ Θ§Τδ÷–AΚΆF «Ϋπ τΒΞ÷ Θ§D «Ήν≥ΘΦϊΒΡ»ήΦΝΓΘIΈΣΜΤ¬Χ…ΪΤχΧεΘ§CΒΡ―φ…ΪΖ¥”Π≥ ΜΤ…ΪΘ§K «ΚλΚ÷…ΪΙΧΧεΓΘ
(8Ζ÷)œ¬ΖΫΉσΆΦ÷–A~KΨυΈΣ÷–―ßΜ·―ß÷–≥ΘΦϊΒΡΈο÷ Θ§Τδ÷–AΚΆF «Ϋπ τΒΞ÷ Θ§D «Ήν≥ΘΦϊΒΡ»ήΦΝΓΘIΈΣΜΤ¬Χ…ΪΤχΧεΘ§CΒΡ―φ…ΪΖ¥”Π≥ ΜΤ…ΪΘ§K «ΚλΚ÷…ΪΙΧΧεΓΘ
(1)FΒΡ‘ΣΥΊ‘Ύ÷ήΤΎ±μ÷–ΈΜ”ΎΒΎΓΓΓΓΓΓ ÷ήΤΎ ΓΓΓΓΓΓΓΓΉεΓΓ ΓΘ
(2)A+DΓζB+CΒΡάκΉ”ΖΫ≥Χ ΫΈΣΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
ΓΓ G+IΓζHΒΡάκΉ”ΖΫ≥Χ ΫΈΣΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
(3) Β―ι “≥Θ”ΟKSCN»ή“ΚΦλ―ιH÷–ΒΡΫπ τάκΉ”Θ§œ÷œσ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
(4)»γ…œΖΫ”“ΆΦΥυ ΨΘ§F¥Π”ΎΔώΓΔΔρΓΔΔσ»ΐ÷÷≤ΜΆ§ΒΡΜΖΨ≥÷–Θ§ΗΟΫπ τ±ΜΗ· ¥ΒΡΥΌ¬ ”…ΩλΒΫ¬ΐΒΡΥ≥–ρ «(Χν–ρΚ≈)_______________ΓΘ
2ΓΔ(8Ζ÷)Μ·ΚœΈοA «“Μ÷÷θΞΘ§ΥϋΒΡΖ÷Ή” ΫΈΣC4H8O2Θ§”–œ¬ΆΦΉΣΜ·ΙΊœΒΓΘ ‘ΜΊ¥πœ¬Ν–Έ ΧβΓΘ
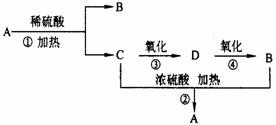 (1)AΒΡΟϊ≥Τ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΘ
(1)AΒΡΟϊ≥Τ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
ΓΘ
(2)BΒΡΫαΙΙΦρ Ϋ «ΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘ
(3)D÷–Κ§”–ΒΡΙΌΡήΆ≈(ΧνΟϊ≥Τ)ΓΓ ΓΓΓΓΓΓΓΘ
(4)–¥≥ωBΚΆC…ζ≥…AΒΡΜ·―ßΖΫ≥ΧΓΓ ΫΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΓΘΓΓ
1Θ°(8Ζ÷)”–AΓΔBΓΔCΓΔDΥΡ÷÷ΕΧ÷ήΤΎ‘ΣΥΊΘ§Τδ÷–AΓΔDΆ§÷ςΉεΘΜ”÷“―÷ΣBΚΆA–Έ≥…ΒΡΜ·ΚœΈοBA÷–Θ§AΒΡΜ·ΚœΦέΈΣ-1Θ§BΚΆC–Έ≥…ΒΡΜ·ΚœΈοB2CΘ§AΓΔBΓΔCάκΉ”ΒΡΚΥΆβΒγΉ”Ήή ΐœύΆ§
(1)–¥≥ωΗς‘ΣΥΊΒΡΟϊ≥ΤΘΚAΓΓΓΓΓΓΓΓΓΓ BΓΓΓΓΓΓΓΓΓΓ CΓΓΓΓΓΓΓΓΓΓ DΓΓΓΓΓΓΓΓΓΓ ΘΜ
(2)‘ΣΥΊC‘Ύ÷ήΤΎ±μ÷–ΒΡΈΜ÷ΟΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ ΘΜ
(3)–¥≥ωDΒΞ÷ ”κBΒΡΉνΗΏΦέ―θΜ·ΈοΕ‘”ΠΥ°Μ·ΈοΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΘ
19Θ° Β―ι «―–ΨΩΜ·―ßΒΡΜυ¥ΓΘ§œ¬ΆΦ÷–Υυ ΨΒΡ Β―ιΖΫΖ®ΓΔΉΑ÷ΟΜρ≤ΌΉςΆξ»Ϊ’ΐ»ΖΒΡ «(ΓΓΓΓ )
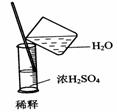
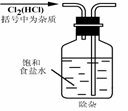 AΘ°ΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
BΘ°
AΘ°ΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ
BΘ°
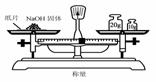
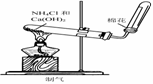
CΘ°ΓΓΓΓ ΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓΓ DΘ°
ΒΎIIΨμ
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com