
5.下列有关实验的说法正确的是
A.除去铁粉中混有的少量铝粉,可加入过量的氢氧化钠溶液,完全反应后过滤
B.为测定熔融氢氧化钠的导电性,可在瓷坩埚中溶化氢氧化钠固体后进行测量
C.制备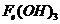 胶体,通常是将
胶体,通常是将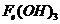 固体溶于热水中
固体溶于热水中
D.某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液中一定含有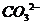
4.下列说法正确的是
A.原子晶体中只存在非极性共价键
B.稀有气体中形成的晶体属于分子晶体
C.干冰升华时,分子内共价键会发生断裂
D.金属元素和非金属元素形成的化合物一定是离子化合物
3.三聚氰酸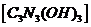 可用于消除汽车尾气中的
可用于消除汽车尾气中的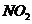 。其反应原理为:
。其反应原理为:
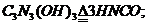
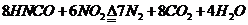
下列说法正确的是
A.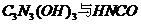 为同一物质 B.
为同一物质 B.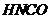 是一种很强的氧化剂
是一种很强的氧化剂
C.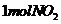 在反应中转移的电子为
在反应中转移的电子为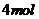 D.反应中
D.反应中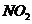 是还原剂
是还原剂
2.下列叙述正确的是
A.聚丙烯的结构简式为: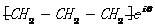
B.石英的化学式为: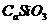
C.在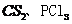 中各原子最外层均能达到8电子的稳定机构
中各原子最外层均能达到8电子的稳定机构
D.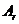 原子的结构示意图为:
原子的结构示意图为: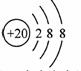
1.据估计,地球上的绿色植物通过光合作用每年能结合来自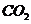 中的碳1500亿吨和来自水中的氢250亿吨,并释放4000亿吨氧气。光合作用的过程一般可用下式表示:
中的碳1500亿吨和来自水中的氢250亿吨,并释放4000亿吨氧气。光合作用的过程一般可用下式表示:
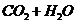 +微量元素(P、N等)
+微量元素(P、N等)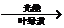 (蛋白质、碳水化合物、脂肪等)+
(蛋白质、碳水化合物、脂肪等)+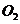
下列说法不正确的是
A.某些无机物通过光合作用可转化为有机物
B.碳水化合物就是碳和水组成的化合物
C.叶绿素是光合作用的催化剂
D.增加植被,保护环境是人类生存的需要
39.(化学-物质结构与性质)(15分)
今有位于元素周期表短周期中X、Y、Z三种元素。已知:
①三者原子序数之和为25;
②元素Y的原子价电子排布为ns2npn+2
③X和Y在不同条件下可形成X2Y和X2Y2两种固体化合物,Y和Z在不同条件下可形成ZY和ZY2两种气态化合物;
④元素Z的硫化物与元素Z的氯化物,常温下均为液态,且二者的相对分子质量之比38:77
据此填写下列空白:
(1)写出元素X的基态原子的电子排布式_____________________。
(2)X2Y2属于________晶体,构成晶体的微粒是_____________________(填微粒符号)。
(3)Z的硫化物的分子空间构形是________________,根据原子轨道重叠方式的不同,Z的氯化物分子中含有的共价键种类及数目是______________________________。
38.(化学-有机化学基础)(15分)
有机物A有如下变化,其中只有B1既能使溴水褪色,又能和Na2CO3溶液反应生成CO2
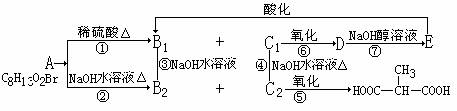
(1)C1中含有的官能团有__________________________
(2)已知CH2=CH-OH不稳定,写出B1既可以发生银镜反应,又可以与金属钠反应的所有链状同分异构体的结构简式:___________________________
(3)写出A与C2两种物质的结构简式: A _______________ C2 ________________
(4)写出反应①③ 的反应类型:①________________ ③_________________
(5)写出反应②的化学方程式__________________________________________________
37.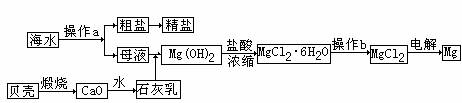 (化学-化学与技术)(15分)
(化学-化学与技术)(15分)
海水是一种丰富的资源,工业上从海水中可提取很多种物质,广泛应用于生活、生产、科技等方面。上图是某工厂对海水资源进行综合利用的示意图。
请回答下列问题:
(1)海水制盐可采取的操作a的方法,则操作a的名称为________________________。作为海水晒盐的海岸必须符合_________________________________________________
___________________________________________________________________________
等条件才能作为盐田(至少填两条)。
(2)若要验证所得精盐中不含KCl,进行最简单的实验操作所需要的实验用品有(试剂除外)______________________________________________________________。
(3)工业从海水中提取的NaCl,可用来制取纯碱,其简要过程如下:向饱和食盐水中先通入气体A,后通入气体B,充分反应后过滤得到晶体NaHCO3 ,将NaHCO3灼烧得纯碱。气体A、B是CO2或NH3,则气体A应是______________________________(填化学式),为什么?___________________________________________________________________
(4)操作b是在____________氛围中进行,其目的是________________________________
(5)镁是一种用途很广泛的金属材料,目前世界上60%的镁从海水中提取。已知有关物质的熔沸点数据如下:
|
|
MgO |
MgCl2 |
|
熔点(°C) |
2850 |
714 |
|
沸点(°C) |
3600 |
1412 |
工业上用电解法生产镁,结合表中数据和实际生产情况,说明通常采用电解MgCl2而不是电解MgO的理由:______________________________________________________________
27.(15分)
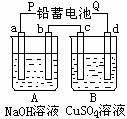 如图装置实验,A、B两烧杯分别放200g 10% NaOH溶液和
如图装置实验,A、B两烧杯分别放200g 10% NaOH溶液和
足量CuSO4溶液。通电一段时间后,c极上有Cu析出,又测
得A杯中溶液的质量少4.5g(不考虑谁的蒸发)。
请回答下列问题:
(1) 电源P极为:___________极 ;
请分别写出b极和c极上发生的电极反应式:
b: ____________________________ c:__________________________
(2)c极上析出固体铜的质量为_____________g。
(3)若装置用铅蓄电池作电源,已知铅蓄电池放电时发生如下的反应:
负极:Pb+SO42-=PbSO4 +2e-
正极:PbO2+4H++SO42-+2e-=PbSO4+2H2O
假设在a极制得气体0.050mol,这时电池内消耗的H2SO4的物质的量至少是________mol。
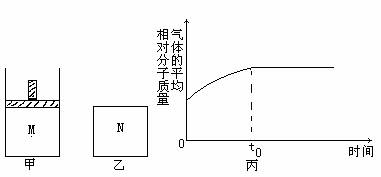
 28.如甲图,在恒压密闭容器M中加入2mol A和2mol B,起始时容器体积为VL,发生如下反应并达到化学平衡状态:2A(?)+B(?) xC(g);△H<0。
28.如甲图,在恒压密闭容器M中加入2mol A和2mol B,起始时容器体积为VL,发生如下反应并达到化学平衡状态:2A(?)+B(?) xC(g);△H<0。
平衡时,A、B、C的物质的量之比为1:3:4,C的物质的量为ymol。
(1)根据题中数据计算,x=____________、y=____________
(2)如乙图,在体积为VL的恒容密闭容器N中发生上述反应(其它条件相同),测得反应过程中气体的平均分子质量随时间的变化如丙图(t0时达平衡),平衡时容器中C的物质的量为zmol。由于反应物A、B的状态未知,则z、y的大小也不确定,请在下表中填入A、B的状态与z、y的大小之间的关系(仿照情形①、可不填满):
|
可能的情形 |
A、B是否为气体 |
z与y的大小关系 |
M(B)与M(C)的大小关系 (M表示摩尔质量) |
|
|
A |
B |
|||
|
① |
是 |
不是 |
z=y |
无法确定 |
|
② |
|
|
|
|
|
③ |
|
|
|
|
0.1mol/L的该化合物水溶液中的离子浓度由大到小的顺序为:_______________________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com