
30ЃЎ(16Зж)
вбжЊЃК
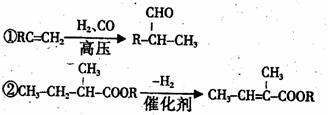
 ЁЁ
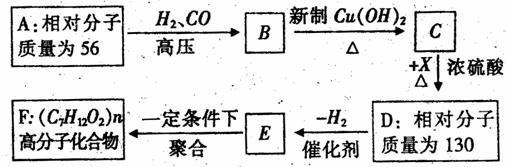
гаЛњЮяA ~FжаЃЌAЪЧСДЬўЃЌAгыH2МгГЩЕУЕНЭщЬўЃЌОВтЖЈЃЌИУЭщЬўЗжзгжажЛгаСНИі-CH3ЃЌЦфвЛТБДњЮягаСНжжЭЌЗжвьЙЙЬхЃЌCгыXЗДгІЩњГЩDЁЃИїЮяжЪжЎЪЧЕФзЊЛЏЙиЯЕШчЯТЭМЫљЪОЃК
ЁЁ
гаЛњЮяA ~FжаЃЌAЪЧСДЬўЃЌAгыH2МгГЩЕУЕНЭщЬўЃЌОВтЖЈЃЌИУЭщЬўЗжзгжажЛгаСНИі-CH3ЃЌЦфвЛТБДњЮягаСНжжЭЌЗжвьЙЙЬхЃЌCгыXЗДгІЩњГЩDЁЃИїЮяжЪжЎЪЧЕФзЊЛЏЙиЯЕШчЯТЭМЫљЪОЃК
ЁЁ (1)аДГіXЕФУћГЦЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (2)аДГіЛЏКЯЮяAЁЂEЕФНсЙЙМђЪНЃКAЁЁЁЁЁЁЁЁЁЁ ЃЌEЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (3)жИГіЯТСаЗДгІЕФРраЭЃКCЁњDЁЁЁЁЁЁЁЁ ЃЌEЁњFЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (4)аДГіBгызуСПаТжЦЧтбѕЛЏЭаќзЧвКЙВШШЪБЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЃКЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (5)гаЛњЮяGЪЧгаЛњЮяCВЛЭЌРраЭЕФЭЌЗжвьЙЙЬхЃЌВЂЧвGФмгыН№ЪєФЦЗЂЩњЗДгІЗХГіЮоЩЋЦјЬхЃЌгжФмЗЂЩњвјОЕЗДгІЃЛгжжЊGЕФЭЌвЛРраЭЕФЭЌЗжвьЙЙЬхЙВгаЖржжЃЌдђЦфжажЛКЌгавЛИіМзЛљЕФЭЌЗжвьЙЙЬхЕФНсЙЙМђЪНгаЁЁЁЁЁЁЁЁЁЁ ЁЂЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ(ШЮаДСНжж)
29ЃЎ(17Зж)
ЁЁЁЁЁЁ ЯТЭМЮЊГЃМћЦјЬхжЦБИЁЂЗжРыЁЂИЩдяКЭаджЪбщжЄЕФВПЗжвЧЦїзАжУ(МгШШЩшБИМАМаГжЙЬЖЈзАжУОљТдШЅЃЌвбжЊввДМЕФЗаЕуЮЊ78.5Ёц)ЃЌЧыИљОнвЊЧѓЭъГЩЯТСаЮЪЬт(вЧЦїзАжУПЩШЮвтбЁгУЃЌБивЊЪБПЩжиИДбЁдёЃЌaЁЂbЮЊа§ХЅ)ЁЃ
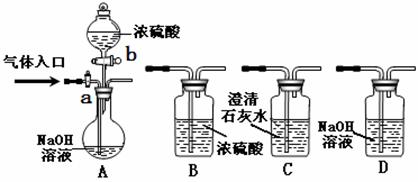
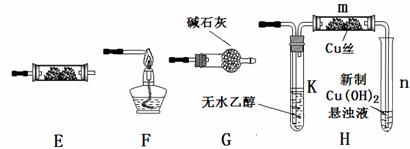
ЁЁ (1)ШєAжаЦјЬхШыПкЭЈШыCOКЭCO2ЕФЛьКЯЦјЬхЃЌEФкЗХжУCuOЃЌгћЕУЕНДПОЛИЩдяЕФCOЃЌВЂбщжЄЦфЛЙдадМАбѕЛЏВњЮяЃЌЫљбЁзАжУЕФСЌНгЫГађЮЊ___ЁЁЁЁЁЁЁЁЁЁ ___ (ЬюаДзАжУДњКХ)ЁЃФмбщжЄCOбѕЛЏВњЮяЕФЪЕбщЯжЯѓЪЧ____________ЁЁЁЁ ____ЁЃ
ЁЁ (2)ЭъГЩ(1)ЪЕбщКѓЃЌНЋAжаaа§ХЅЙиБеЃЌВЂдкEФкЗХжУNa2O2ЃЌАДAЁњEЁњDЁњBЁњHзАжУЫГађЃЌжЦШЁДПОЛИЩдяЕФO2ЃЌВЂгУO2бѕЛЏввДМЁЃ
ЂйЮЊЛёЕУбѕЦјЃЌЙиБеaа§ХЅКѓЃЌЪзЯШашНјааЕФВйзїЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЂкЮЊЕУЕНЦНЮШЕФввДМеєЦјСї,ЬсИпЗДгІаЇТЪЃЌПЩВЩШЁЕФДыЪЉЪЧ(гУЮФзжМђЪі)ЁЁЁЁЁЁ
__________ЃЛmжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЪЧ____________________________ЁЃ
ЂлШєЯыЙлВьЕНЪдЙмnжагаКьЩЋГСЕэГіЯжЃЌЛЙашвЊНјааЕФВйзїЪЧ________ЁЁ __ЁЃ
28ЃЎ(15Зж)
 ЁЁ
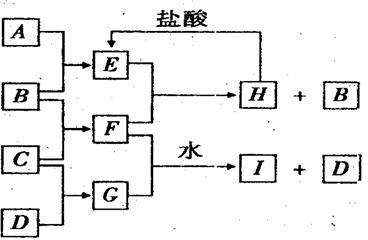
AЁЂBЁЂCЁЂDЪЧАДдзгађЪ§гЩаЁЕНДѓХХСаЕФЕкЖўЁЂШ§жмЦкдЊЫиЕФЕЅжЪЁЃBЁЂEОљЮЊзщГЩПеЦјЕФГЩЗжЁЃFЕФбцЩЋЗДгІГЪЛЦЩЋЁЃдкGжаЃЌЗЧН№ЪєдЊЫигыН№ЪєдЊЫиЕФдзгИіЪ§БШЮЊ1ЃК2ЁЃдквЛЖЈЬѕМўЯТЃЌИїЮяжЪжЎМфЕФЯрЛЅзЊЛЏЙиЯЕШчЭМ(ЭМжаВПЗжВњЮяЮДСаГі)ЃК
ЁЁ
AЁЂBЁЂCЁЂDЪЧАДдзгађЪ§гЩаЁЕНДѓХХСаЕФЕкЖўЁЂШ§жмЦкдЊЫиЕФЕЅжЪЁЃBЁЂEОљЮЊзщГЩПеЦјЕФГЩЗжЁЃFЕФбцЩЋЗДгІГЪЛЦЩЋЁЃдкGжаЃЌЗЧН№ЪєдЊЫигыН№ЪєдЊЫиЕФдзгИіЪ§БШЮЊ1ЃК2ЁЃдквЛЖЈЬѕМўЯТЃЌИїЮяжЪжЎМфЕФЯрЛЅзЊЛЏЙиЯЕШчЭМ(ЭМжаВПЗжВњЮяЮДСаГі)ЃК
ЁЁЁЁ ЧыЬюаДЯТСаПеАз
ЁЁ (1)AЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌFЕФЕчзгЪНЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (2)HгыбЮЫсЗДгІЩњГЩEЕФЛЏбЇЗНГЬЪНЪЧ
ЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЁЁ (3)EгыFЗДгІЕФЛЏбЇЗНГЬЪНЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (4)FгыGЕФЫЎШмвКЗДгІЩњГЩIКЭDЕФРызгЗНГЬЪНЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЃ
56.1KJЕФШШСПЃЌЪдаДГіСђЛЏЧтЗжНтЕФШШЛЏбЇЗН
ГЬЪНЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЃ
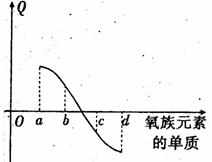
ЁЁ (5)гвЭМЫљЪОЮЊбѕзхдЊЫиЕЅжЪгыH2ЗДгІЙ§ГЬжаЕФ
ФмСПБфЛЏЪОвтЭМЃЌЦфжаaЁЂbЁЂcЁЂdЗжСэБэЪО
бѕзхжаФГвЛдЊЫиЕФЕЅжЪЃЌQЮЊЯрЭЌЮяжЪЕФСП
ЕФЕЅжЪгыH2ЗДгІЗХГіЕФШШСПЁЃдђЃК
aДњБэЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌcДњБэЁЁЁЁЁЁЁЁЁЁЁЁ
(ОљПЩЕЅжЪУћГЦ)
27ЃЎ(12Зж)ЯТБэЪЧбѕзхдЊЫиЕФЯрЙиаджЪ
|
аджЪ\дЊЫи |
8O |
16S |
34Se |
52Te |
|
ЕЅжЪШлЕу(Ёц) |
-218.4 |
113 |
ЁЁ |
450 |
|
ЕЅжЪЗаЕу(Ёц) |
-183 |
444.6 |
685 |
1390 |
|
жївЊЛЏКЯМл |
-2 |
-2ЃЌ+4ЃЌ+6 |
-2ЃЌ+4ЃЌ+6 |
ЁЁ |
|
дзгАыОЖ |
ж№НЅдіДѓ |
|||
|
ЕЅжЪгыH2ЗДгІЧщПі |
ЕуШМЪБвзЛЏКЯ |
МгШШЛЏКЯ |
МгШШФбЛЏКЯ |
ВЛФмжБНгЛЏКЯ |
ЁЁЁЁ ЧыИљОнБэЛиД№ЯТСаЮЪЬтЃК
ЁЁ (1)ЮјЕФШлЕуЗЖЮЇПЩФмЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁ
ЁЁ (2)ЧтЮјЫсгаНЯЧПЕФЁЁЁЁЁЁЁЁЁЁ (ЬюЁАбѕЛЏадЁБЛђЁАЛЙдадЁБ)ЃЌвђДЫЗХдкПеЦјжаГЄЦкБЃДцвзБфжЪЃЌЦфПЩФмЗЂЩњдкЛЏбЇЗДгІЗНГЬЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
 ЁЁ
ЁЁ
(3)ЙЄвЕЩЯAl2Te3ПЩгУРДжЦБИH2TeЃЌЭъГЩЯТСаЛЏбЇЗНГЬЪНЃК
ЁЁ
ЁЁ
(3)ЙЄвЕЩЯAl2Te3ПЩгУРДжЦБИH2TeЃЌЭъГЩЯТСаЛЏбЇЗНГЬЪНЃК
ЁЁЁЁЁЁЁЁ ЁѕAl2Te3+ЁѕЁЁЁЁЁЁ ===Al(OH)3Ё§+ЁѕH2TeЁќ
ЁЁ (4)вбжЊдкГЃЮТЯТЃЌH2КЭSЗДгІЩњГЩ17gH2SЗХГі
26ЃЎ(20Зж)
ЛЗзДПеаФЕФЯИН№ЪєЙмЕРжЪСПЮЊMЃЌВЛМЦвЛЧаФІВСЁЃ
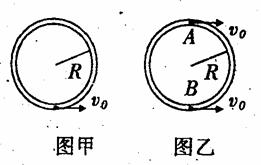
ЁЁ (1)НЋЙмЕРЪњжБЙЬЖЈЃЌЙмФкЕзВПгавЛПЩЪгЮЊжЪЕуЕФаЁЧђ(ШчЭММз)ЃЌШєаЁЧђГѕЫйЖШЮЊv0ЃЌаЁЧђЧЁФмЭЈЙ§зюИпЕуЃЌДЫЪБЧђЪмЕНЙмЕРБкЕФЕЏСІДѓаЁЮЊMg/2ЃЌаЁЧђЕФжЪСПДѓаЁЮЊЖрЩйЃПЛЗЕФАыОЖRЮЊЖрЩй(гыЛЗЕФАыОЖЯрБШЃЌЙмЕФДжЯИПЩВЛМЦ)ЃП
ЁЁ (2)ЯжНЋЙмЕРЫЎЦНЗХжУдкЙтЛЌЫЎЦНУцЩЯЃЌЙмжБОЖСНЖЫAЁЂBДІгаСНИігыЕквЛЮЪЭъШЋЯрЭЌЕФаЁЧђ(ШчЭМвв)ЃЌГѕЫйЖШШдОљЮЊv0ЃЌЕБСНЧђЯргіЪБЃЌаЁЧђЫйЖШДѓаЁЮЊЖрЩйЃП
ЁЁ (3)НєНгЩЯЮЪЃЌШєСНЧђЗЂЩњЭъШЋЕЏадХізВЃЌдђЕБСНаЁЧђЗжБ№ЛиЕНABДІЪБЃЌЙмЕРЕФЫйЖШДѓаЁЮЊЖрЩйЃП
 ЁЁ
ЁЁ
ЁЁ
ЁЁ
25ЃЎ(18Зж)
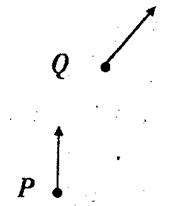
ПеМфжаДцдкЫЎЦНЯђгвЕФдШЧПЕчГЁЃЌГЁЧПДѓаЁЮЊEЃЌвЛДјЕчСПЮЊ+qЁЂжЪСПЮЊmЕФСЃзгЃЌдкPЕувдЯђЩЯГѕЫйЖШv0ПЊЪМдЫЖЏЃЌИУСЃзгдЫЖЏЕНЭМжаQЕуЪБЫйЖШЗНЯђгыPЕуЪБЕФЗНЯђЦЋзЊСЫ45ЁуЃЌШєБЃГжСЃзгдкPЕуЪБЕФЫйЖШВЛБфЃЌЖјНЋдШЧПЕчГЁЛЛГЩЗНЯђДЙжБгкжНУцЯђЭтЕФдШЧПДХГЁЃЌдкДЫДХГЁСІЕФзїгУЯТСЃзгвВгЩPЕудЫЖЏЕНQЕуЃЌВЛМЦжиСІЁЃЧѓЃК
 ЁЁ
ЁЁ
(1)PЁЂQМфЕФОрРыlЮЊЖрЩйЃП
ЁЁ
ЁЁ
(1)PЁЂQМфЕФОрРыlЮЊЖрЩйЃП
ЁЁ (2)дШЧПДХГЁЕФДХИагІЧПЖШЮЊЖрЩйЃП
24ЃЎ(14Зж)
Н№ЪєАєдкЮТЖШЩ§ИпЃЌЦфГЄЖШвВЛсдіГЄЃЌЮвУЧАбЮТЖШЩ§Ип1ЁцЫљв§Ц№ГЄЖШЕФдіМггыЫќдк0ЁцЪБГЄЖШжЎБШГЦЮЊЯпХђеЭЯЕЪ§ІСЁЃФЧУДЃЌН№ЪєАєtЁцЪБЕФГЄЖШl1гыЦфдк0ЁцЕФГЄЖШ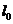 гаЯТСаЙиЯЕЃК
гаЯТСаЙиЯЕЃК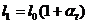 ЁЃ
ЁЃ
ЁЁЁЁЁЁЁЁ ЯждкСНИљН№ЪєАєЃЌЯпХђеЭЯЕЪ§ЗжБ№ЮЊ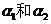 ЃЌдк0ЁцЕФГЄЖШЗжБ№ЮЊL10КЭL20ЃЌШєЗЂЯжетСНИљН№ЪєАєдкШЮКЮЮТЖШЯТГЄЖШжЎВюОљКуЖЈЃЌЧѓ
ЃЌдк0ЁцЕФГЄЖШЗжБ№ЮЊL10КЭL20ЃЌШєЗЂЯжетСНИљН№ЪєАєдкШЮКЮЮТЖШЯТГЄЖШжЎВюОљКуЖЈЃЌЧѓ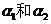 жЎБШЮЊЖрЩйЃП
жЎБШЮЊЖрЩйЃП
23ЃЎ(ЙВ12ЗжЃЌУППе2Зж)
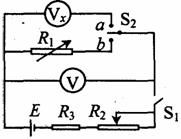 ЮЊСЫВтЖЈЕчбЙБэVxЕФФкзшЃЌВЩгУСЫШчЭМЫљЪОЕФЕчТЗЁЃЦфжаЃКVxЪЧД§ВтЕчбЙБэЃЌСПГЬ3VЃЌФкзшдМ3kІИЃЛVЪЧБъзМЕчбЙБэЃЌСПГЬ2VЃЌФкзшдМ2kІИЃЛR1ЪЧЕчзшЯфЃЌзшжЕЗЖЮЇЪЧ0-9999.9ІИЃЛR2ЪЧЛЌЖЏБфзшЦїЃЛR3ЪЧБЃЛЄЕчзшЃЛEЪЧЕчГизщЃЌЕчЖЏЪЦ6VЃЌФкзшВЛМЦЃЛS1ЪЧЕЅЕЖЕЅжРПЊЙиЃЌS2ЪЧЕЅЕЖЫЋжРПЊЙиЃЎ
ЮЊСЫВтЖЈЕчбЙБэVxЕФФкзшЃЌВЩгУСЫШчЭМЫљЪОЕФЕчТЗЁЃЦфжаЃКVxЪЧД§ВтЕчбЙБэЃЌСПГЬ3VЃЌФкзшдМ3kІИЃЛVЪЧБъзМЕчбЙБэЃЌСПГЬ2VЃЌФкзшдМ2kІИЃЛR1ЪЧЕчзшЯфЃЌзшжЕЗЖЮЇЪЧ0-9999.9ІИЃЛR2ЪЧЛЌЖЏБфзшЦїЃЛR3ЪЧБЃЛЄЕчзшЃЛEЪЧЕчГизщЃЌЕчЖЏЪЦ6VЃЌФкзшВЛМЦЃЛS1ЪЧЕЅЕЖЕЅжРПЊЙиЃЌS2ЪЧЕЅЕЖЫЋжРПЊЙиЃЎ
ЁЁ (1)ЪЕбщВНжшШчЯТЃКЁЁЁЁ
ЁЁ (a)ИљОнЕчТЗЭМЃЌНЋЦїВФе§ШЗЕиСЌНгГЩЪЕбщЕчТЗЃЎ
ЁЁ (b)НЋПЊЙиS2АтЕНСЌНгЕуaДІЃЌНгЭЈПЊЙиS1ЃЌЕїНкЛЌЖЏ
БфзшЦїR2ЃЌЪЙЕчбЙБэVЕФЖСЪ§ЪЧ1.50VЁЁЁЁ
ЁЁ (c)ЖЯПЊПЊЙиS1ЃЌНЋПЊЙиS2АтЕНСЌНгЕуbДІЃЌНгЭЈПЊЙи
S1ЃЌБЃГж____ЁЁ ______ВЛБфЃЌЕїНк_______________
 ЪЙЕчбЙБэVЕФЖСЪ§ЪЧ______________VЃЌдђПЩвдШЯЮЊ
ЪЙЕчбЙБэVЕФЖСЪ§ЪЧ______________VЃЌдђПЩвдШЯЮЊ
ЕчзшЯфR1ЕФзшжЕОЭЕШгкЕчбЙБэVxЕФФкзшЃЎ
ЁЁ (d)ШєДЫЪБЕчзшЯфR1Иїа§ХЅЕФЮЛжУШчЭМЫљЪОЃЌдђЕчзшЯфR1ЕФ
зшжЕЪЧ__________ІИЃЌМДЮЊД§ВтЕчбЙБэVxЕФФкзшЃЎ
ЁЁ (2)гУБОЪЕбщЗНЗЈВтЕУЕФЕчбЙБэVxЕФФкзшжЕгыЕчбЙБэVxФкзш
ЕФецЪЕжЕЯрБШНЯЃЌВтСПжЕ_________(ЬюађКХ)ЃЎ
ЁЁЁЁЁЁЁЁ AЃЎТдДѓгкЁЁЁЁ BЃЎТдаЁгкЁЁЁЁ CЃЎЕШгк
ЁЁ (3)ЩЯЪіЪЕбщжаЃЌБеКЯПЊЙиS1КЭS2Кѓ(ЯШБеКЯS2КѓБеКЯS1)ЃЌ
ЮоТлдѕбљЕїНкЕчзшЯфR1КЭЛЌЖЏБфзшЦїR2ЃЌЖМвЊБЃжЄСНИі
ЕчбЙБэЕФАВШЋЃЎдкЯТУцЬсЙЉЕФЫФИіЕчзшжаЃЌБЃЛЄЕчзшR3
гІбЁгУ____________(ЬюађКХ)ЁЃЁЁЁЁЁЁЁЁ
AЃЎ4kІИЁЁЁЁЁЁЁЁ BЃЎ3.33kІИЁЁЁЁ ЁЁЁЁ CЃЎ2.4kІИЁЁЁЁ ЁЁЁЁЁЁЁЁ DЃЎ1 kІИ
22ЃЎ(ЙВ8ЗжЃЌУПИіХаЖЯ2Зж)ЧыХаЖЯЯТСагаЙиИпжаЮяРэбЇЩњЪЕбщЕФУшЪіЪЧЗёе§ШЗЃЌе§ШЗЕФД№ЬтПЈЖдгІЬтКХЕФЮЛжУЩЯДђЩЯЁАЁЬЁБЃЌДэЮѓЕФдкД№ЬтПЈЖдгІЬтКХЕФЮЛжУЩЯДђЩЯЁАЁСЁБЁЃ
ЁЁЁЁЁЁЁЁ AЃЎЁАбщжЄЛњаЕФмЪиКуЖЈТЩЁБЪЕбщжаЃЌВЛашвЊгУЬьЦНВтГіЯТТфДЙДИЕФжЪСП
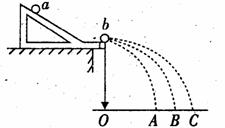
BЃЎЁАбаОПЦНХзЮяЬхдЫЖЏЁБЕФЪЕбщжаЃЌШчЙћвбОУшЛцКУдЫЖЏЙьМЃЃЌМДЪЙЭќМЧМЧТМХзГіЕуЕФЮЛжУКЭЪњжБЗНЯђЃЌвВФмЭЈЙ§ЪЪЕБбЁШЁЙьМЃЩЯЕФШ§ИіЕуРДЧѓЦНХздЫЖЏЕФГѕЫйЖШЁЃ
 ЁЁ
CЃЎЁАгУЕЅАкВтЖЈжиСІМгЫйЖШЁБЪЕбщжаЃЌШєНЋ49
ЁЁ
CЃЎЁАгУЕЅАкВтЖЈжиСІМгЫйЖШЁБЪЕбщжаЃЌШєНЋ49
ДЮШЋеёЖЏЮѓМЧТМГЩ50ДЮШЋеёЖЏЃЌНЋЕМжТжи
СІМгЫйЖШЕФВтСПжЕБШЪЕМЪжЕЦЋДѓЁЃ
DЃЎЁАбщжЄЖЏСПЪиКуЖЈТЩЁБЪЕбщжаЃЌдкАзжНЩЯМЧЯТ
жиДЙЯпЫљжИЕФЮЛжУOКѓЃЌВЛаЁаФНЋАзжНКЭ
ИДаДжНЭЌЪБЯђгввЦЖЏСЫЩйаэЃЌМЬајЪЕбщЃЌ
ЕУЕНаЁЧђдкАзжНЩЯТфЕуЕФЦНОљЮЛжУAЁЂBЁЂ
C(ШчЭМ)ЃЌАзжНЕФвЦЖЏЖдЪЕбщНсЙћУЛгагАЯьЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com