
20.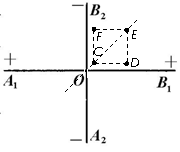 理论研究表明,无限大的均匀带电平面在周围空间会形成与平面垂直的匀强电场。现有两块无限大的均匀绝缘带电平板,正交放置如图所示,A1B1两面正电,A2B2两面负电,且单位面积所带电荷量相等(设电荷不发生移动)。图中直线A1B1和A2B2分别为带正电平面和带负电平面与纸面正交的交线,O为两交线的交点,C、D、E、F恰好位于纸面内正方形的四个顶点上,且CE的连线过O点。则下列说法中正确的是
理论研究表明,无限大的均匀带电平面在周围空间会形成与平面垂直的匀强电场。现有两块无限大的均匀绝缘带电平板,正交放置如图所示,A1B1两面正电,A2B2两面负电,且单位面积所带电荷量相等(设电荷不发生移动)。图中直线A1B1和A2B2分别为带正电平面和带负电平面与纸面正交的交线,O为两交线的交点,C、D、E、F恰好位于纸面内正方形的四个顶点上,且CE的连线过O点。则下列说法中正确的是
A. C、E两点场强相同
B. D、F两点电势相同
C.电子从C点移到D点电场力做正功
D.在C、D、E、F四个点中电子在F点具有的电势能最大
第II卷
19.1798年英国物理学家卡文迪许测出万有引力常量G,因此卡文迪许被人们称为能称出地球质量的人,若已知万有引力常量G,地球表面处的重力加速度g,地球半径为R,地球上一个昼夜的时间为T1(地球自转周期),一年的时间T2(地球公转的周期),地球中心到月球中心的距离L1,地球中心到太阳中心的距离为L2。则
A.地球的质量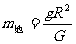
B.太阳的质量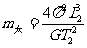
C.月球的质量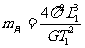
D.利用上面给出的已知量可求月球、地球及太阳的密度
18.如图所示,理想变压器,原副线圈的匝数比为n。原线圈接正弦交流电压U,输出端A、A1、A2、A3为理想的交流电流表,R为三个完全相同的电阻,L为电感,C为电容,当输入端接通电源后,电流表A读数为I。下列判断正确的是
A.副线圈两端的电压为nU
B.通过副线圈的最大电流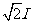
C.电流表A1的读数I1大于电流表A2的读数I2
D.电流表A3的读数I3=0
16.质量为1kg的物体静止在水平面上,物体与水平面之间的动摩擦因数为0.2。对物体施加一个大小变化、方向不变的水平拉力F,使物体在水平面上运动了3t0的时间。为使物体在3t0时间内发生的位移最大,力F随时间的变化情况应该为下面四个图中的
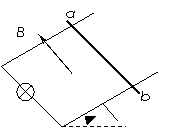
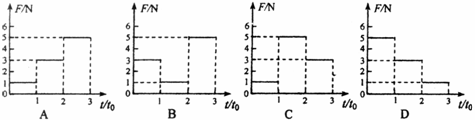 17.如图所示,光滑导轨倾斜放置,其下端连接一个灯泡,匀强磁场垂直于导轨所在平面,当ab棒下滑到稳定状态时,小灯泡获得的功率为P0。除灯泡外,其它电阻不计,要使灯泡的功率变为2P0(仍在灯泡额定功率范围内),下列措施正确的是
17.如图所示,光滑导轨倾斜放置,其下端连接一个灯泡,匀强磁场垂直于导轨所在平面,当ab棒下滑到稳定状态时,小灯泡获得的功率为P0。除灯泡外,其它电阻不计,要使灯泡的功率变为2P0(仍在灯泡额定功率范围内),下列措施正确的是
A.换一个电阻为原来一半的灯泡
B.磁感应强度增为原来的2倍
C.换一根质量为原来的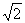 倍的金属棒
倍的金属棒
D.把导轨间的距离增大为原来的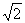 倍
倍
15.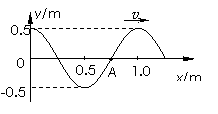 有一列简谐横波在弹性介质中沿x轴正方向以速率v=5.0m/s传播,t=0时刻的波形如图所示,下列说法中正确的是
有一列简谐横波在弹性介质中沿x轴正方向以速率v=5.0m/s传播,t=0时刻的波形如图所示,下列说法中正确的是
A.该列波的波长为0.5m,频率为5Hz
B.t=0.1s时,波形沿x轴正方向移动0.5m
C.t=0.1s时,质点A的位置坐标为(1.25m,0)
D.t=0.1s时,质点A的速度为零
14.下列说法正确的是
A.爱因斯坦提出了光子学说,成功解释了光电效应现象
B.核反应方程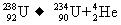 属于裂变
属于裂变
C.β衰变中产生的β射线是原子核外电子挣脱原子核束缚后形成的
D.升高放射性物质的温度,可缩短其半衰期
13.下列溶液中各微粒的浓度关系或说法正确的是
A.0.1 mol•L-1 pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-)
B.等物质的量浓度的下列溶液中,①NH4Al(SO4)2、②NH4Cl、③CH3COONH4、
④NH3·H2O;c(NH4+) 由大到小的顺序是:①>②>③>④
C.a mol·L-1HCN溶液与b mol·L-1NaOH溶液等体积混合后,所得溶液中c(Na+)>c(CN-),则a一定大于b
D.0.1mol·L-1的醋酸的pH=a,0.01mol·L-1的醋酸的pH=b,则a+1=b
12.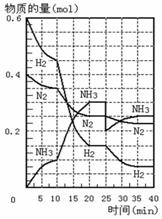 500℃、20MPa时,将H2和N2置于一容积为2L的密闭容器中发生反应:3H2+N2
500℃、20MPa时,将H2和N2置于一容积为2L的密闭容器中发生反应:3H2+N2 2NH3 △H<0。反应过程中H2、N2和NH3物质的量变化如右图所示,据图判断下列叙述不正确的是
2NH3 △H<0。反应过程中H2、N2和NH3物质的量变化如右图所示,据图判断下列叙述不正确的是
A.反应开始到第一次平衡时,N2的平均反应速率为0.0625 mol·(L·min)-1 ,H2的转化率为75%
B.反应达到第一次平衡时,反应的平衡常数表达式可写作:K=c2(NH3)/[ c3(H2) ·c(N2)]=(0.15 mol·L-1) 2/[ (0.075 mol·L-1) 3 ·(0.125 mol·L-1)]
C.从曲线变化可以看出,反应进行到10min至20min时可能采取的措施是使用了催化剂。
D.从曲线变化可以看出,反应进行至25min时,采取的措施是分离出0.1mol的氨气,平衡正向移动。
11.原子数相同、电子总数相同的粒子,互称为等电子体。硼元素可形成三个等电子体阴离子:BO2-、BC25-和BN2n-,则BN2n-中的n值为
A.1 B.2 C.3 D.4
10.下列判断或实验预期正确的是
A.对于反应N2H4(l)=N2(g)+2H2(g) △H=-50.6kJ·mol-1,它在任何温度下都是自发的。
B.用升华法分离碘和氯化铵的混合物,用乙醇萃取碘水中的碘
C.纯碱溶液或石灰水存放在配有磨口塞的棕色玻璃瓶中
D.淀粉用酸催化水解后的溶液加入新制银氨溶液,水浴加热,可看到有银镜出现
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com