
21.(8分)在一定体积的密闭容器中,进行如下化学反应:
CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
|
t |
K |
|
700 |
0.6 |
|
800 |
0.9 |
|
830 |
1.0 |
|
1000 |
1.7 |
|
1200 |
2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K= 。
(2)该反应为 反应(填“吸热”或“放热”)。
(3)能判断该反应是否达到化学平衡状态的依据是 。
a.容器中压强不变 b.混合气体中c(CO)不变
c.v正(H2)=v逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为 ℃。
20.下列各图中表示正反应是吸热反应的图是 ( )
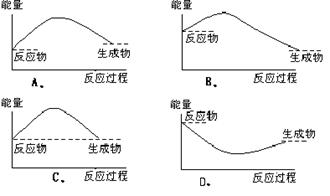
第Ⅱ卷(非选择题,共50分)
19.一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如右图,下列描述正确的是( )
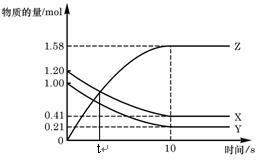
A.t秒时该反应达到化学平衡状态
B.反应开始到10 s,X的物质的量浓度减少了0.79mol/L
C.反应开始到10s时,Y的转化率为79.0%
D.反应的化学方程式为:X(g) +
Y(g) 2Z(g)
2Z(g)
18.某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中P表示压强,T表示温度,n表示物质的量):
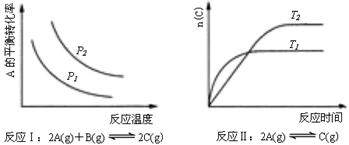
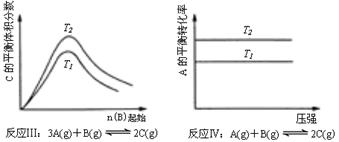
根据以上规律判断,下列结论正确的是( )
A.反应Ⅰ:△H>0,P2>P1
B.反应Ⅱ:△H<0,T1>T2
C.反应Ⅲ:△H﹤0,T2>T1
D.反应Ⅳ:△H<0,T2>T1
17.已知450℃时,反应H2(g)+I2(g) 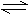 2HI(g)的K=50,由此推测在450℃时,反应2HI(g)
2HI(g)的K=50,由此推测在450℃时,反应2HI(g) 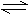 H2(g)+I2(g)的化学平衡常数为(
)
H2(g)+I2(g)的化学平衡常数为(
)
A.50 B.0.02 C.100 D.无法确定
16.在一密闭容器中,反应aA(g)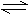 bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则( )
bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则( )
A.物质A的转化率小了 B.平衡向正反应方向移动了
C.物质B的质量分数减小了 D.b>a
15.一定条件下,可逆反应N2 +3H2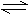 2NH3(正反应为放热反应)达到平衡,当单独改变下述条件后,有关叙述错误的是(
)
2NH3(正反应为放热反应)达到平衡,当单独改变下述条件后,有关叙述错误的是(
)
A、加催化剂,V正、V逆 都发生变化,且变化的倍数相等
B、加压,V正、V逆 都增大,且V正 增大的倍数小于V逆 增大的倍数
C、降温,V正、V逆 都减小,且V正 减小的倍数大于V逆 减小的倍数
D、增大氮气的浓度,V正、V逆 都增大,且V正 增大倍数大于V逆 增大倍数
14.有如下反应:mA(g)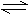 nB(g),当加压后,反应速率如图所示,推断系数m和n的关系是( )
nB(g),当加压后,反应速率如图所示,推断系数m和n的关系是( )
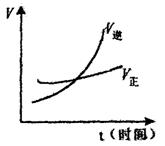
A.m>n B.m<n C.m=n D.无法确定
13.在36 g 碳不完全燃烧所得气体中,CO占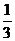 体积,CO2占
体积,CO2占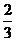 体积,且
体积,且
C(s) + O2(g) = CO(g) △H = -110.5 kJ/mol
CO(g) + O2(g) = CO2(g) △H = -283 kJ/mol
与这些碳完全燃烧相比,损失的热量是( )
A.172.5 kJ B. 1149 kJ
C.283kJ D. 517.5 kJ
12.已知Zn(s)+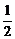 O2(g)===ZnO(s);ΔH1=-351、1kJ/mol
O2(g)===ZnO(s);ΔH1=-351、1kJ/mol
Hg(s)+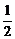 O2(g)===
Hg O(s);ΔH2=-90、7kJ/mol
O2(g)===
Hg O(s);ΔH2=-90、7kJ/mol
Zn(s)+Hg O(s)=== Hg(s)+ZnO(s);ΔH3
则ΔH3是 ( )
A.-441、8kJ/mol B.-254、6kJ/mol C.-438、9kJ/mol D.-260、4kJ/mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com