
3ЃЎ
|
ЁЁ |
е§МЋЗДгІ |
ИКМЋЗДгІ |
ЕчГизмЗДгІ |
pHБфЛЏ |
|
(1) |
2H2O+O2+4eЃ=4OHЃ |
H2+2OHЃЃ2eЃ=2H2O |
2H2+ O2=2H2O |
БфаЁ |
|
(2) |
H2S+8OHЃЃ6eЃ=SO32Ѓ+5H2O |
O2 ЁЁ |
БфаЁ |
|
|
(3) |
CO+4OHЃ Ѓ2eЃ=CO32Ѓ+2H2O |
2CO+O2+4OHЃ=2CO32Ѓ+2H2O |
БфаЁ |
|
|
(4) |
CH4+10OHЃ -8eЃ= CO32Ѓ+7H2O |
CH4+2O2+2OHЃ=CO32Ѓ+3H2O |
БфаЁ |
|
|
(5) |
C2H4+16OHЃ -12eЃ= 2CO32Ѓ+ 10H2O |
C2H4+3O2+4OHЃ=2CO32Ѓ+4H2O |
БфаЁ |
|
|
(6) |
C2H2+14OHЃ -10eЃ=2CO32Ѓ+8H2O |
2C2H2+5O2+8OHЃ=4CO32Ѓ+6H2O |
БфаЁ |
МьВтЬсИп
2.(1) ЂкЁЁ (2)ЂйЂлЁЁ (3) ЂйЂлЁЁ (4) ЂкЂл
1.ACЁЁ НВЮіЃКЭЈЙ§ДЫЬтЕФбЕСЗПЩвдДяЕНШЋУцеЦЮегаЙидЕчГиЙЄзїдРэЁЂЕчМЋЗДгІЁЂЕчзгСїЯђЕШжЊЪЖЕуЃЌЭЌЪБИУЬтвВЪЧвЛИіНЋПЮБОжЊЪЖгыЪЕМЪНсКЯЕФМЋКУР§згЁЃ
ЁЁЁЁ ХаЖЯдЕчГиЕФе§ИКМЋЃЌПЩвдДгСНИіЗНУцЃКЂйЮЂЙлЃКЕчзгСїГіЕФвЛМЋЪЧИКМЋЃЌЕчзгСїШыЕФвЛМЋЪЧе§МЋЁЃЂкКъЙл:ЛюЦУЕФЕчМЋЪЧИКМЋЃЌВЛЛюЦУЕФвЛМЋЪЧе§МЋЃЌЕчзгЪЧДгИКМЋбиЕМ
12ЃЎ(1)дЕчГиЁЃZnЃ2e = Zn2+ЃЛ2H++2e = H2
(2)O2ЃЌЕчНтГиЁЃ2Cu2++4e = 2CuЃЌ4OHЃЃ4e =2H2O+O2ЃЌНЕЕЭЁЃ
ЁЁЁЁ зАжУСЌНгШчЭМЃК
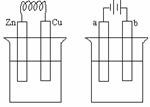
ЁЁЕк17ПЮЪБ(BОэ)
ОРДэбЕСЗ
11ЃЎ(1)дЕчГижаЕФбѕЛЏЗДгІ
(2)ЬМЗлЃКЙЙГЩдЕчГиЕФе§МЋЃЛNaClЃКЦ№ЕчНтжЪШмвКЕФзїгУ
(3)ИКМЋЃК2FeЃ4eЃ=2Fe2+
е§МЋЃК2H2O+O2+4eЃ=4OHЃ
4Fe(OH)2+O2+2H2O=4Fe(OH)3
10ЃЎAЁЂCБжаЗЂЩњЮќбѕИЏЪДЃЌНЯТ§ЁЃ
ЁЁЁЁ BБжаЗЂЩњЮіЧтИЏЪДЃЌНЯПьЁЃ
ЁЁЁЁ вђЮЊдке§МЋЖсЕчзгЕФЮЂСЃКЭХЈЖШЖМВЛЯрЭЌ,BБжа[H+]ДѓЃЌЫљвдЗДгІПьЁЃЖјAЁЂCБжа[O2]дЖаЁгк[H+]ЃЌЫљвдЗДгІТ§ЁЃ
1ЁЂDЁЁЁЁ 2ЁЂC 3ЁЂDЁЁЁЁЁЁЁЁ 4ЁЂAЁЁЁЁ 5ЁЂBЁЁЁЁ 6ЁЂDЁЁЁЁЁЁ 7ЁЂDЁЁЁЁЁЁЁЁ 8ЁЂB ЁЁ 9ЁЂA
4ЃЎ DBACE
аТЛюЬтЭјеО
3ЃЎ(1)D (2) вђдЕчГиЗДгІЃЌЭНЋдквјАє(е§МЋ)ЩЯЮіГіЖјВЛЪЧдкЬњАєЩЯЃЌЫљвдгІИУЪЧвјАєЯТГСЬњАєЩЯЩ§.
НВЮіЃКДэЮѓЕФШЯЪЖЪЧЃКЭРызггыЬњЗЂЩњжУЛЛЗДгІЃЌЬњАєдіжиЯђЯТГС.ЪЕМЪЩЯгІИУПМТЧдЕчГиЗДгІЃЌЭНЋдквјАєЩЯЮіГіЖјВЛЪЧдкЬњАєЩЯЃЌЫљвдгІИУЪЧвјАєЯТГСЬњАєЩЯЩ§.
2ЃЎCDЁЁНВЮіЃКЪзЯШЪЧЧјБ№ГіГфЕчдЫгУЕФЪЧЕчНтдРэЃЌЗХЕчдђЪЧдЫгУСЫдЕчГидРэЁЃзЅзЁЕчНтГиЁЂдЕчГиИїМЋЗЂЩњбѕЛЏЛЙдЗДгІЕФЬиЕуЃЌНсКЯЬтИјЕФаХЯЂНјааЗжЮіХаЖЯЃК
AЃКдЕчГиИКМЋЗДгІЪНЮЊЃК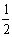 H2+OH-+e-
H2+OH-+e- Ni(OH)2ЃЌpHЯТНЕЁЃЙЪAВЛе§ШЗЁЃ
Ni(OH)2ЃЌpHЯТНЕЁЃЙЪAВЛе§ШЗЁЃ
BЃКдЕчГиЃЌNiO(OH)ЁњNi(OH)2ЃЌФјБЛЛЙдЁЃЙЪBвВВЛе§ШЗЁЃЭЌРэПЩХаЖЯЕУЃКе§ШЗД№АИЮЊCDЁЃ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com