
1ЃЎACЁЁ2.CЁЁ 3.BЁЁ 4.DЁЁ 5.CЁЁ 6.BDЁЁ 7.D
НВЮіЃК1ЃЎГ§дгдРэЪЧГ§ШЅдгжЪЃЌЕЋжївЊЮяжЪВЛВЮгыЗДгІЃЌВЛв§ШыаТдгжЪЁЃжївЊЮяжЪгыЦфЫћЮяжЪШнвзЗжРыЃЌNO2гыЫЎЗДгІзЊЛЏГЩNOЁЃNH4ClгыЙ§СПЕФNaOHШмвКЗДгІЃЌГ§ШЅСЫNH4ClЃЌЕЋгЩгкNaOHЙ§СПЃЌв§ШыСЫаТдгжЪЁЃбѕЦјгыМгШШЕФCuЗДгІЩњГЩCuOЙЬЬхЁЃАзСзШМЩеЗХШШЪЙКьСзШМЩеЁЃЁЁ2ЃЎгЩЗДгІNO2+NO+2NaOH 2NaNO2+H2OЁЁ ПЩжЊV(NO2)ЁЂV(NO)ЬхЛ§БШЮЊ1ЃК1ЪБЃЌЭъШЋБЛМюШмвКЮќЪеЃЌЕБNO2Й§СПЪБЃЌМЬајЗЂЩњЗДгІ2NO2+2NaOH
2NaNO2+H2OЁЁ ПЩжЊV(NO2)ЁЂV(NO)ЬхЛ§БШЮЊ1ЃК1ЪБЃЌЭъШЋБЛМюШмвКЮќЪеЃЌЕБNO2Й§СПЪБЃЌМЬајЗЂЩњЗДгІ2NO2+2NaOH NaNO3+NaNO2+H2OЃЌФмБЛМюШмвКЮќЪеЁЃЕБNOЙ§СПЪБОЭВЛФмБЛМюШмвКЮќЪеСЫЁЃЁЁ3ЃЎбѕЛЏЛЙдЗДгІжаЛЏКЯМлЕФЩ§НЕзмЪ§гІЯрЕШЁЃЕЊдЊЫиЙВЩ§Ип8МлЃЌбѕдЊЫиЙВЩ§Ип4МлЃЌЫљвдН№ЪєдЊЫигІИУЩњИп4МлЁЃД№АИЃКBЁЃ4ЃЎH2SКЭSO2ЗДгІЩњГЩSКЭH2O(l)ЃЌЦјЬхЕФЮяжЪЕФСПМѕЩйЁЃNOКЭO2ЗДгІЦјЬхЮяжЪЕФСПМѕЩйЁЃCl2КЭHIЗДгІЩњГЩHClКЭI2ЙЬЬхЃЌЦјЬхЮяжЪЕФСПМѕЩйЁЃCl2КЭH2SЗДгІЩњГЩHClКЭSЙЬЬхЃЌЦјЬхЮяжЪЕФСПВЛБфЁЃЁЁ7ЃЎ 22.4mLNOКЭ11.2 mlO2ЧЁКУЭъШЋЗДгІЩњГЩNO2ЃЌВПЗжNO2МЬајЗДгІЩњГЩN2O4ЃЌЦјЬхгЩNO2КЭN2O4зщГЩЁЃБъПіЯТЃЌd(NO2)=2.054g/LЁЁ d(N2O4)=4.108g/L
NaNO3+NaNO2+H2OЃЌФмБЛМюШмвКЮќЪеЁЃЕБNOЙ§СПЪБОЭВЛФмБЛМюШмвКЮќЪеСЫЁЃЁЁ3ЃЎбѕЛЏЛЙдЗДгІжаЛЏКЯМлЕФЩ§НЕзмЪ§гІЯрЕШЁЃЕЊдЊЫиЙВЩ§Ип8МлЃЌбѕдЊЫиЙВЩ§Ип4МлЃЌЫљвдН№ЪєдЊЫигІИУЩњИп4МлЁЃД№АИЃКBЁЃ4ЃЎH2SКЭSO2ЗДгІЩњГЩSКЭH2O(l)ЃЌЦјЬхЕФЮяжЪЕФСПМѕЩйЁЃNOКЭO2ЗДгІЦјЬхЮяжЪЕФСПМѕЩйЁЃCl2КЭHIЗДгІЩњГЩHClКЭI2ЙЬЬхЃЌЦјЬхЮяжЪЕФСПМѕЩйЁЃCl2КЭH2SЗДгІЩњГЩHClКЭSЙЬЬхЃЌЦјЬхЮяжЪЕФСПВЛБфЁЃЁЁ7ЃЎ 22.4mLNOКЭ11.2 mlO2ЧЁКУЭъШЋЗДгІЩњГЩNO2ЃЌВПЗжNO2МЬајЗДгІЩњГЩN2O4ЃЌЦјЬхгЩNO2КЭN2O4зщГЩЁЃБъПіЯТЃЌd(NO2)=2.054g/LЁЁ d(N2O4)=4.108g/L
ЫљвдЃЌЦјЬхЕФУмЖШдк2.054g/L~4.108g/L.Д№АИЃКDЁЃ
6ЃЎАзСзЁЂP4ЁЃЮхбѕЛЏЖўСзЁЂP2O5ЃЌЦЋСзЫсЁЂHPO3ЃЌ
СзЫсЁЂH3PO4ЁЃ
аТЛюЬтЭјеО
5ЃЎ(1)ШѕМюадЁЃ(2)взШМЩеЁЃ(3)H3AsO4ЃЌAsH3ЃЌ74.9ЃЌТдЁЃНВЮіЃКЭЌжмЦкЕФдЊЫиДгзѓЭљгвЃЌдЊЫиЕФН№Ъєадж№НЅМѕШѕЃЌЗЧН№Ъєадж№НЅдіЧПЃЌЗЧН№ЪєдЊЫиЕФЧтЛЏЮяЕФЫсаддіЧПЃЌМюадМѕШѕЁЃАБЫЎГЪМюадЁЃSiЕФЗЧН№ЪєадБШPШѕЃЌЫљвдЧтЛЏЮяЮШЖЈадВюЃЌвзШМЩеЁЃ
1.CЁЁ 2.BЁЁ 3.AЁЁ 4.C
НВЮіЃК1.ЕЊЗжзггЩгкдзгжЎМфгаШ§ИіЙВМлМќЃЌМќФмКмДѓЃЌЫљвдЕЊЗжзгКмЮШЖЈЃЌЕЋЕЊдЊЫиЗЧН№ЪєадКмЧПЃЌдкЕЊзхдЊЫижаЗЧН№ЪєадзюЧПЁЃдкЛЏбЇЗДгІжаСзЕЅжЪБШЕЊЦјЛюЦУЁЃЕЊЦјаджЪЮШЖЈЃЌПЩвдзіБЃЛЄЦјЃЌвКЕЊПЩзіРфЖГМСЁЃЁЁ2ЃЎгЩвЛжждЊЫиаЮГЩЕФВЛЭЌжжЕЅжЪ,ЛЅГЦЮЊЭЌЫивьаЮЬх.жЪзгЪ§ЯрЭЌ,жазгЪ§ВЛЭЌЕФдзг,ЛЅГЦЮЊЭЌЮЛЫи.AЮЊЭЌЮЛЫи,BЮЊЭЌЫивьаЮЬх.CЁЂDЪЧгЩЭЌжждЊЫизщГЩЕФВЛЭЌжжЮяжЪЁЃ3ЃЎБОЬтЪЧИљОнЗжзгЪНЕФМЦЫуЃЌгЩдЊЫиЕФжЪСПБШСаЪНМЦЫуГіЛЏКЯМлЁЃ
17ЃЎ (2002ФъИпПМзлКЯЬт)вбжЊМЙзЕЖЏЮяЕФЙЧїРжаКЌгаСзЁЃвдЯТЪЧВтЖЈЖЏЮяЙЧЛвжаСздЊЫиКЌСПЕФЪЕбщЗНЗЈЁЃГЦШЁФГЖЏЮяЙЧЛвбљЦЗ0.103 gЃЌгУЯѕЫсДІРэЃЌЪЙСззЊЛЏГЩСзЫсИљЁЃдйМгШыФГЪдМСЃЌЪЙСзЫсИљгжзЊЛЏГЩГСЕэЁЃГСЕэОзЦЩеКѓЕУЕНзщГЩЮЊP2Mo24O77ЕФЙЬЬх(ЦфЪНСПвд3.60 ЁС103МЦ)0.504 gЁЃЪдгЩЩЯЪіЪ§ОнМЦЫуИУЙЧЛвбљЦЗжаСзЕФжЪСПЗжЪ§ЁЃ(СзЕФЯрЖддзгжЪСПвд31.0 )ЁЁ
16ЃЎНЋVКСЩ§NOКЭNO2ЕФЛьКЯЦјЬхЭЈЙ§ЫЎЮќЪеКѓЃЌЕУЕНaКСЩ§ЮоЩЋЦјЬхAЃЌНЋДЫЮоЩЋЦјЬхAгыЕШЬхЛ§ЕФO2ЛьКЯЃЌдйЭЈЙ§ЫЎГфЗжЮќЪеКѓЪеМЏЕН5КСЩ§ЮоЩЋЦјЬхBЁЃЪдЛиД№ЃКЂйAЁЂBЮЊКЮжжЦјЬхЃПЂкAЦјЬхЕФЬхЛ§ЪЧЖрЩйКСЩ§ЃПЂлVЕФШЁжЕЗЖЮЇЁЃ
15ЃЎЪЕбщЪвжавЊВтЖЈФГЮоЩЋЦјЬхЕФГЩЗнЃЌвбжЊДЫЦјЬхПЩФмгЩCO2ЁЂNH3ЁЂNO2ЁЂN2ЁЂNOжаЕФвЛжжЛђМИжжЛьКЯЖјГЩЁЃНЋДЫЮоЩЋЦјЬхНјаавдЯТЪЕбщЃКЂйЯШЭЈЙ§ЪЂгаХЈСђЫсЕФЯДЦјЦПЃЌЗЂЯжЦјЬхМѕЩйвЛВПЗжЬхЛ§ЃЛЂкМЬајЭЈЙ§зАгаNa2O2ЙЬЬхЕФИЩдяЙмЃЌЗЂЯжДгИЩдяЙмГіРДЕФЦјЬхбеЩЋГЪКьзиЩЋЃЛЂлдйМЬајНЋЦјЬхЭЈШыЪЂТњЫЎЕЙСЂгкЫЎВлжаЕФЪдЙмФкЃЌзюКѓЦјЬхЭъШЋБЛЮќЪеЃЌЪдЙмФкШдЮЊвЛТњЪдЙмвКЬхЁЃгЩДЫПЩХаЖЯЃК
(1)дЦјЬхжавЛЖЈКЌгаЁЁЁЁЁЁ ЃЌвЛЖЈВЛКЌгаЁЁЁЁЁЁ ЁЃ
(2)аДГіЂкжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(3)гЩзюжеНсЙћПЩжЊдЦјЬхжаЁЁЁЁЁЁ КЭ ЁЁЁЁЁЁЁЁЕФЬхЛ§БШЮЊЁЁЁЁЁЁЁЁ ЁЃ
14ЃЎНЋХ№ЩА(Na2B4O7)гыNH4ClЙВШШЃЌдйгУбЮЫсЃЌШШЫЎДІРэЃЌПЩЕУЕНАзЩЋЙЬЬхЕЊЛЏХ№(BN)ЁЃ
(1)ХфЦНЗДгІЗНГЬЪНЃК
ЁЁЁЁ ЁѕNa2B4O7+ЁѕNH4Cl = ЁѕNaCl+ЁѕB2O3+2BN+ЁѕH2O
(2)BNЪЧвЛжжаТаЭЮоЛњВФСЯЃЌЫќгаСНжжОЇЬхНсЙЙЃЌН№ИеЪЏаЭЕФBNПЩзїФЭФЅВФСЯЃЌЫќгІОпгаЕФаджЪЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛЪЏФЋаЭBNПЩзїШѓЛЌВФСЯЃЌЫќгІОпгаЕФОЇЬхНсЙЙЮЊ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
13ЃЎШчЭМЫљЪОзЊЛЏЙиЯЕЃЌХаЖЯAЁЂBЁЂCЁЂDИїЪЧЪВУДЮяжЪЃЌаДГігаЙиЕФЛЏбЇЗНГЬЪНЁЃ
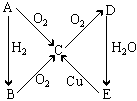
(1)ЕБAЮЊЦјЬхЕЅжЪЪБЃЌAЪЧЁЁЁЁЁЁ ЃЌBЪЧЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁ ЃЌ
ЁЁCЪЧЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌ
DЪЧЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌ
EЪЧЁЁЁЁЁЁЁЁ
ЁЁEЁњCЛЏбЇЗНГЬЪНЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(2)ЕБAЮЊЙЬЬхЕЅжЪЪБЃЌAЪЧЁЁЁЁЁЁ ЃЌBЪЧЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁ ЃЌЁЁ CЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌDЪЧЁЁЁЁ ЁЁЁЁЁЁЁЁ ЃЌEЪЧЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
EЁњCЛЏбЇЗНГЬЪНЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
12ЃЎНЋ20ml NO2КЭNH3ЕФЛьКЯЦјЬхдквЛЖЈЬѕМўЯТГфЗжЗДгІЃЌЛЏбЇЗНГЬЪНЪЧ6NO2+8NH3==7N2+12H2OЃЌвбжЊВЮМгЗДгІЕФNO2БШNH3Щй2ml(ЦјЬхЬхЛ§ОљдкЯрЭЌЬѕМўЯТВтЖЈ)ЁЃдђдЛьКЯЦјЬхжаNO2КЭNH3ЕФЮяжЪЕФСПжЎБШЪЧ
AЃЎ3ЁУ2 ЁЁЁЁBЃЎ2ЁУ3 ЁЁ
ЁЁCЃЎ3ЁУ7ЁЁЁЁ DЃЎ3ЁУ4
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com