
1.文化现象无处不在,下列属于文化现象的有
①我市南山公园保质快速推进
②2010年9月20日“南昌--九江”城际列车正式开通
③九江一中召开第39届运动会,运动场上同学们青春勃发
④观看中央电视台“唱响九江,相约九银”大型文艺晚会
A.①② B.②③ C.③④ D. ①④
8. 如下图所示的装置,C、D、E、F、X、Y都是惰性电极。将电源接通后,向(乙)中滴入酚酞溶液,在F极附近显红色。则以下说法正确的是

A.电源B极是正极
B.(甲)、(乙)装置的C、D、E、F电极均有单质生成,其物质的量之比为1 : 2 : 2 : 1
C.欲用(丙)装置给铜镀银,H应该是Ag,电镀液是AgNO3溶液
D.装置(丁)中Y极附近红褐色变深,说明氢氧化铁胶粒带正电荷
7.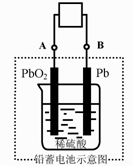 电瓶车所用电池一般为铅蓄电池,这是一种典型的可充电电池,
电池总反应式为:
电瓶车所用电池一般为铅蓄电池,这是一种典型的可充电电池,
电池总反应式为:
Pb+PbO2+4H++2SO42- 2PbSO4+2H2O,
2PbSO4+2H2O,
则下列说法正确的是:
A.放电时:电子流动方向由A到B
B.放电时:正极反应是Pb-2e-+SO42- PbSO4
PbSO4
C.充电时:铅蓄电池的负极应与充电器电源的正极相连
D.充电时:阳极反应是PbSO4-2e-+2H2O PbO2+SO42-+4H+
PbO2+SO42-+4H+
6. 今有室温下四种溶液,有关叙述不正确的是
|
|
① |
② |
③ |
④ |
|
pH |
11 |
11 |
3 |
3 |
|
溶液 |
氨水 |
氢氧化钠溶液 |
醋酸 |
盐酸 |
A.①、②中分别加入适量的氯化铵晶体后,两溶液的pH均减小
B.分别加水稀释10倍,四种溶液的pH: ①>②>④>③
C.①、④两溶液等体积混合,所得溶液中c(Cl-)>c(NH4+)>c(OH-)>c(H+)
D.VaL④与VbL②溶液混合后,若混合后溶液pH=4, 则Va : Vb= 11 : 9
5. 海底黑烟囱可在海底堆积硫化物的颗粒,形成多种金属矿产。若从海底黑烟囱附近的矿产物中分离出富铜矿CuFeS2,可用于冶炼铜,熔炼过程主要反应为:
2CuFeS2 = Cu2S+2FeS+S…………………………… ①
2Cu2S+3O2=2Cu2O+2SO2………………………………… ②
Cu2O+FeS = Cu2S+FeO……………………………… ③
2FeS+3O2+SiO2 = 2FeO·SiO2+2SO2………………… ④
2FeO+SiO2 = 2FeO·SiO2……………………………… ⑤
Cu2S+2Cu2O = 6Cu +SO2 ……………………………… ⑥
下列有关说法不正确的是
A.上述反应均属于氧化还原反应 B.该厂可同时建硫酸厂和炼铁厂
C.该厂的原料除富铜矿外,还需空气和硅石 D.反应④转移12e-
4. 从下列事实所得出的相应结论正确的是
|
|
实
验
事
实 |
结 论 |
|
① |
Cl2的水溶液可以导电 |
Cl2是电解质 |
|
② |
将CO2通入到Na2SiO3溶液中产生白色浑浊 |
酸性:H2CO3>H2SiO3 |
|
③ |
NaHCO3溶液与NaAlO2溶液混合产生白色沉淀 |
酸性:HCO3->Al(OH)3 |
|
④ |
常温下白磷可自燃而氮气须在放电时才与氧气反应 |
非金属性:P>N |
|
⑤ |
某无色溶液中加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝 |
该溶液一定有NH4+ |
A.③④⑤ B.②③⑤ C.①②③ D.全部
3. 下列操作或仪器的选用正确的是
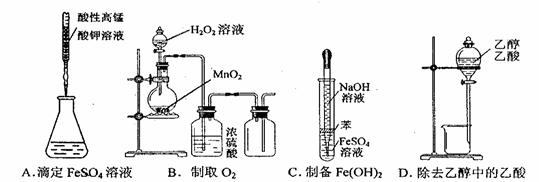
2. 下列叙述正确的是
A.用标准氢氧化钠溶液滴定含甲基橙的盐酸,终点时溶液由橙色变成黄色
B.将SO2通入BaCl2溶液中产生白色沉淀,再滴加稀硝酸沉淀不消失
C.将碘盐加入淀粉溶液中,充分搅拌后溶液呈蓝色
D.向葡萄糖溶液中加人新制氢氧化铜,加热至沸,静置后上层溶液显红色
1. 0.3 mol硼烷(B2H6)在氧气中完全燃烧生成B2O3固体和液态水,放出649.5 kJ热量。下列判断正确的是
A.该反应是非氧化还原反应
B.在理论上可以利用该反应的原理做成燃料电池
C.该反应的热化学方程式为:B2H6(g)+3O2(g) = B2O3(s)
+3H2O(l); H= +2165 kJ/mol
H= +2165 kJ/mol
D.每生成18 g水,该反应转移2 mol电子
30.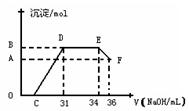 (16分)实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。某同学取一定量铁铝合金与100mL某浓度的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入4mol·L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示(C>0)。试回答下列问题:
(16分)实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。某同学取一定量铁铝合金与100mL某浓度的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入4mol·L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示(C>0)。试回答下列问题:
(1)写出反应过程中的离子反应方程式:OC段 ,
DE段 ,
EF段_____________________________________________ __________。
(2)硝酸溶液的物质的量浓度为 mol·L-1
(3)B的值为_________mol,C的值为 mL。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com