
氢键是除范德华力外的另一种 ,它是由已经与电负性很强的原子形成共价键的氢原子与 中电负性很强的原子之间的作用力;氢键不仅存在于分子与分子之间,也可存在于分子内。与化学键相比,氢键是一种较弱的作用力,但比范德华力大。
试题枚举
[例1]下列变化中,不存在化学键断裂的是
A.氯化氢气体溶于水
B.干冰气化
C.氯化钠固体溶于水
D.氢气在氯气中燃烧
解析:氯化氢气体溶于水,电离出H+和Cl-,原有的共价键被破坏;氯化钠固体溶于水,氯化钠固体中不能自由移动的Na+和Cl-变成能够自由移动,原有的离子键被破坏;干冰是由分子构成的,气化时只要克服分子间作用力,不要破坏分子内的化学键;氢气在氯气中燃烧是化学变化,必然有化学键的断裂。
答案: B
[例2]下列实验事实不能用氢键来解释的是
A.冰的密度比水小,能浮在水面上
B.接近沸点的水蒸气的相对分子质量测量值大于18
C.邻羟基苯甲醛的沸点低于对羟基苯甲醛
D.H2O比H2S稳定
解析:氢键使冰晶体中的水分子呈一定规则排列,空间利用率低,密度小;氢键使接近沸点的水蒸气中含有少量(H2O)2;邻羟基苯甲醛存在分子内氢键,而对羟基苯甲醛存在分子间氢键,增大了分子间作用力,沸点较高。H2O比H2S稳定是因为H-O比H-S稳定
答案:D。
[例3]下列物质中分子间能形成氢键的是
A.N2 B.HBr C.NH3 D.H2S
解析:A-H……B,A、B为N、O、F
答案:C
[例4]试从不同角度解释:乙醇(C2H5OH)和二甲醚(CH3OCH3)的化学组成均为C2H6O,但乙醇的沸点为78.5℃,而二甲醚的沸点为-23℃?
解析:乙醇(C2H5OH)和二甲醚(CH3OCH3)的化学组成相同,两者的相对分子质量也相同,不同的是二者的极性、对称性不同,且乙醇能满足氢键的形成条件,从不同点加以解释。
答案:①乙醇的极性强,分子间作用力大,沸腾时需要提供更多的能量去破坏分子间作用力②乙醇分子之间能形成氢键,使分子间产生了较强的结合力,沸腾时需要提供更多的能量去破坏分子间氢键,而二甲醚分子间没有氢键,上述两点使乙醇的沸点比二甲醚的高。
3.分子间作用力对物质性质的影响
分子间作用力主要影响物质的物理性质,如 、 等
2.影响分子间作用力大小的因素:
(1)组成与结构相似的物质,相对分子质量 ,分子间作用力越大
(2)分子的极性越大,分子间作用力
(3)分子的空间构型:一般来说,分子的空间型越对称,分子间作用力越小
1.概念:分子间作用力又称 ,是广泛存在于分子与分子之间的较弱的电性引力,只有分子间充分接近时才有分子间的相互作用存在。
22.(本题满分12分)
已知函数 (
(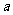 为实常数).
为实常数).
(1)若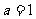 ,作函数
,作函数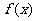 的图像;
的图像;
(2)设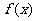 在区间
在区间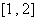 上的最小值为
上的最小值为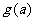 ,求
,求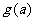 的表达式;
的表达式;
(3)设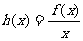 ,若函数
,若函数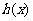 在区间
在区间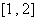 上是增函数,求实数
上是增函数,求实数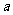 的取值范围.
的取值范围.




21. (本小题满分12分)
设函数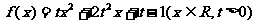
(I)求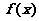 的最小值
的最小值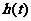 ;
;
(II)若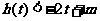 ,对
,对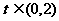 恒成立,求实数
恒成立,求实数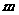 的取值范围.
的取值范围.
20. (本小题满分12分)设函数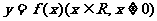 对于任意非零实数
对于任意非零实数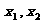 满足
满足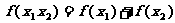 ,且
,且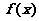 在
在 内为增函数
内为增函数
(1)求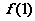 和
和 的值;
的值;
⑵判断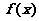 的奇偶性并证明
的奇偶性并证明
⑶若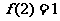 ,解不等式
,解不等式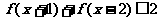
19.(本小题满分12分)已知函数 满足
满足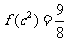
(1)求常数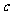 的值;
的值;
(2)解不等式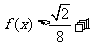
18.(本小题满分12分)
已知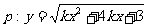 的定义域为
的定义域为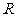 ;
;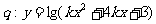 的值域为
的值域为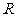 。若“
。若“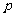 且
且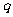 ”为假,“
”为假,“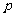 或
或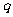 ”为真,求实数
”为真,求实数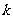 的取值范围。
的取值范围。
17.(本小题满分10分)
已知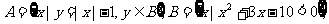 求
求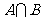 .
.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com