
6.(2010·上海虹口区模拟)已知NH4CuSO3与足量的2mol/L硫酸溶液混合微热,产生下列现象:①有红色金属生成 ②产生刺激性气味的气体 ③溶液呈现蓝色。据此判断下列说法正确的是( )。
A.反应中硫酸作氧化剂
B.NH4CuSO3中硫元素被氧化
C.1mol NH4CuSO3完全反应转移0.5mol电子
D.刺激性气味的气体是氨气
[解析]选C。红色金属是Cu,蓝色溶液中含Cu2+,NH3和SO2都是有刺激性气味的气体,但是NH3能溶于足量的硫酸溶液,所以该气体一定是SO2,由此可写出该反应的方程式:2NH4CuSO3+2H2SO4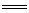 (NH4)2SO4+CuSO4+2SO2↑+Cu↓+2H2O,在该反应中铜元素的化合价由+1价变成0价和+2价,所以NH4CuSO3中铜元素既被氧化又被还原,反应转移1个电子,即1mol NH4CuSO3完全反应转移0.5mol电子。
(NH4)2SO4+CuSO4+2SO2↑+Cu↓+2H2O,在该反应中铜元素的化合价由+1价变成0价和+2价,所以NH4CuSO3中铜元素既被氧化又被还原,反应转移1个电子,即1mol NH4CuSO3完全反应转移0.5mol电子。
5.(2010·通辽模拟)某反应体系的物质有:NaOH、Au2O3、Na2S4O6、Na2S2O3、Au2O、H2O。下列选项正确的是( )。

A.Na2S4O6、H2O、Na2S2O3、Au2O、NaOH
B.Na2S2O3、NaOH、Na2S4O6、Au2O、H2O
C.Na2S2O3、H2O、Na2S4O6、Au2O、NaOH
D.当1mol Au2O3完全反应时,转移电子的物质的量为8mol
[解析]选C。Au2O3是反应物,则Au2O一定是生成物,其中Au元素化合价由+3价变成+1价,化合价降低,,则必然有化合价升高的,即Na2S2O3(硫元素为+2价)是反应物,Na2S4O6(硫元素为+2.5价)是生成物。根据反应前后硫元素守恒则有:2Na2S2O3→Na2S4O6,根据钠元素守恒,则生成物这边缺少钠元素,所以NaOH是生成物,再根据氢元素守恒,则水是反应物。由关系式:Au2O3~Au2O~4e-,所以当1mol Au2O3完全反应时,转移电子的物质的量为4mol。
4.(2010·南通模拟)科学家发现,食用虾类等水生甲壳类动物的同时服用维生素C容易中毒,这是因为对人体无害的+5价砷类物质在维生素C的作用下,能够转化为有毒的+3价含砷化合物。下列说法中不正确的是( )。
A.维生素C具有还原性
B.上述过程中砷元素发生还原反应
C.上述过程中+5价砷类物质作氧化剂
D.1mol +5价砷完全转化为+3价砷,共失去2mol电子
[解析]选D。由题意知,维生素C能够将+5价的砷变成+3价的砷,所以砷元素发生还原反应,+5价的砷作氧化剂,维生素C发生氧化反应,作还原剂,失去2个电子。
3.(2010·安庆模拟)如图所示,两圆圈相交的阴影部分表示圆圈内物质相互发生的反应,其中属于氧化还原反应,但水既不作氧化剂也不作还原剂的是( )。
A.甲 B.乙 C.丙 D.丁
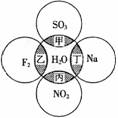
[解析]选C。水中氢元素处于最高价,具有氧化性,氧元素处于最低价,具有还原性,水作还原剂的反应是-2价的氧元素被氧化成O2的反应。水作氧化剂的反应是+1价的氢元素被还原成H2的反应,水既不作氧化剂也不作还原剂的反应是既没有O2产生又没有H2产生的反应。各个反应的方程式及水的作用分析如下表:
|
|
化学方程式 |
是否为氧化还原反应 |
水的作用 |
|
甲 |
SO3+H2O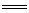 H2SO4 H2SO4 |
不是 |
非氧化剂,非还原剂 |
|
乙 |
2F2+2H2O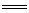 4HF+O2 4HF+O2 |
是 |
还原剂 |
|
丙 |
3NO2+H2O 2HNO3+NO 2HNO3+NO |
是 |
非氧化剂,非还原剂 |
|
丁 |
2Na+2H2O 2NaOH+H2↑ 2NaOH+H2↑ |
是 |
氧化剂 |
2.(2010·宿迁模拟)我国“四大发明”在人类发展史上起到了非常重要的作用,其中黑火药的爆炸反应为:2KNO3+S+3C K2S+N2↑+3CO2↑。该反应中被氧化的元素是( )。
K2S+N2↑+3CO2↑。该反应中被氧化的元素是( )。
A.C B.N C.N和S D.N和C
[解析]选A。在该反应中,氮元素由+5价变成0价,硫元素由0价变成-2价,化合价降低,被还原;碳元素由0价变成+4价,化合价升高,被氧化。
1.(2010·商丘模拟)下列物质久置于空气中会发生相应的变化,其中发生了氧化还原反应的是( )。
A.浓硫酸的体积增大 B.铝的表面生成致密的薄膜
C.澄清的石灰水变浑浊 D.氢氧化钠的表面发生潮解
[解析]选B。浓硫酸和氢氧化钠固体都有吸水性,可以吸收空气中的水蒸气而使体积增大或发生潮解,发生物理变化;铝是一种活泼金属,极易被空气中的氧气在表面氧化生成一层致密的氧化物薄膜而具有抗腐蚀性能;澄清的石灰水可以吸收空气中的二氧化碳生成白色的CaCO3沉淀,为非氧化还原反应。
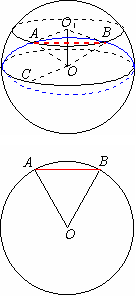
4.设地球的半径为R,在北纬45°圈上有A、B两点,它们的经度相差90°,那么这两点间的纬线的长为_________,两点间的球面距离是_________.
分析:求A、B两点间的球面距离,就是求过球心和点A、B的大圆的劣弧长,因而应先求出弦AB的长,所以要先求出A、B两点所在纬度圈的半径.
解:连结AB.设地球球心为O,北纬45°圈中心为O1,则
O1O⊥O1A,O1O⊥O1B.
 ∴
∴ 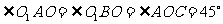 .
.
∴ O1A=O1B=O1O=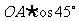 =
=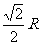 .
.
∴ 两点间的纬线的长为: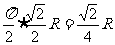 .
.
∵ A、B两点的经度相差90°,
∴ 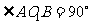 .
.
在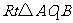 中,
中,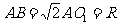 ,
,
∴ 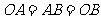 ,
,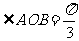 .
.
∴ 两点间的球面距离是: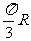 .
.
说明:半径为R的圆弧长的公式: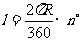 或
或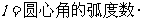 半径.
半径.
3.一个球夹在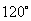 二面角内,两切点在球面上最短距离为
二面角内,两切点在球面上最短距离为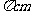 ,则球半径为 ;
,则球半径为 ;
答案: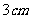
1 ?①过球面上任意两点,作球的大圆的个数是 .
?①过球面上任意两点,作球的大圆的个数是 .
②球半径为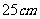 ,球心到截面距离为
,球心到截面距离为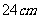 ,则截面面积为 .
,则截面面积为 .
③已知球的两个平行截面的面积分别是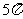 和
和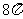 ,它们位于球心同一侧,且相距
,它们位于球心同一侧,且相距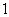 ,则球半径是 .
,则球半径是 .
④球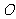 直径为
直径为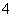 ,
,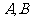 为球面上的两点且
为球面上的两点且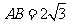 ,则
,则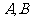 两点的球面距离为 .
两点的球面距离为 .
⑤北纬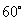 圈上
圈上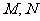 两地,它们在纬度圈上的弧长是
两地,它们在纬度圈上的弧长是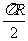 (
(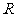 为地球半径),则这两地间的球面距离为 .
为地球半径),则这两地间的球面距离为 .
答案:①一个或无数个 ②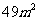 ③
③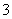 ④
④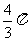 ⑤
⑤ 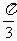
2.北纬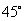 圈上有
圈上有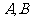 两地,
两地,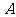 在东径
在东径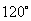 ,
,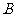 在西径
在西径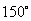 ,设地球半径为
,设地球半径为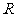 ,
,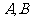 两地球面距离为 ;
两地球面距离为 ;
答案: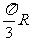
例1  我国首都靠近北纬
我国首都靠近北纬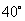 纬线,求北纬
纬线,求北纬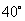 纬线的长度等于多少
纬线的长度等于多少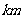 ?(地球半径大约为
?(地球半径大约为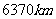 )
)
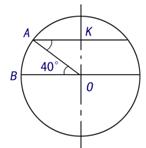 解:如图,
解:如图,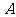 是北纬
是北纬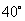 上一点,
上一点,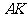 是它的半径,
是它的半径,
∴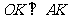 ,
,
设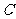 是北纬
是北纬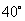 的纬线长,
的纬线长,
∵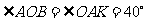 ,
,
∴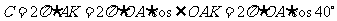
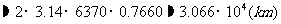
答:北纬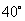 纬线长约等于
纬线长约等于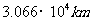 .
.
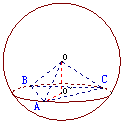 例2.在半径为
例2.在半径为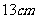 的球面上有
的球面上有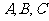 三点,
三点,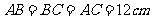 ,求球心到经过这三点的截面的距离
,求球心到经过这三点的截面的距离
解:设经过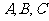 三点的截面为⊙
三点的截面为⊙ ,
,
设球心为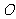 ,连结
,连结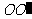 ,则
,则 平面
平面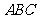 ,
,
∵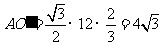 ,∴
,∴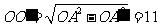 ,
,
所以,球心到截面距离为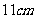 .
.
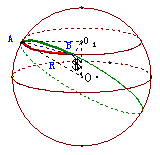
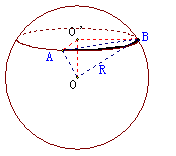 例3.在北纬
例3.在北纬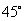 圈上有
圈上有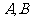 两点,设该纬度圈上
两点,设该纬度圈上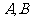 两点的劣弧长为
两点的劣弧长为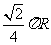 (
(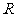 为地球半径),求
为地球半径),求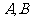 两点间的球面距离
两点间的球面距离
解:设北纬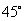 圈的半径为
圈的半径为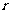 ,则
,则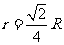 ,设
,设 为北纬
为北纬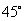 圈的圆心,
圈的圆心,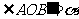 ,
,
 ∴
∴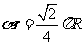 ,∴
,∴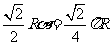 ,
,
∴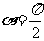 ,∴
,∴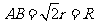 ,
,
∴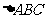 中,
中,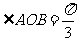 ,
,
所以,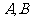 两点的球面距离等于
两点的球面距离等于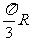 .
.
说明:要求两点的球面距离,必须先求出两点的直线距离,再求出这两点的球心角,进而求出这两点的球面距离
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com