
21(10分)Ⅰ.已知A、B、C、D四种分子所含原子的数目依次为1、3、6、6,且都含有18个电子,B、C是由两种元素的原子组成,且分子中两种原子的个数比均为1 :2。D是一种有毒的有机物。
(1)组成A分子的原子的元素符号是 ;
(2)从B分子的立体结构判断,该分子属于 分子(填“极性”或“非极性”);
(3)C分子中都包含_______个σ键,_______个π键。
(4)D的熔、沸点比CH4的熔、沸点高,其主要原因是(须指明D是何物质):
______________________________________________________。
Ⅱ.CO的结构可表示为C≡O,N2的结构可表示为N≡N。
(5)下表是两者的键能数据:(单位:kJ/mol)
A-B
A=B
A≡B
CO
②用移液管移取50.00mL滤液于250mL碘量瓶中,控制溶液的pH=3~4,加入过量KI溶液(生成CuI和I2)和指示剂,用0.01100mol×L-1Na2S2O3溶液滴定生成的I2至终点(反应:I2 + 2S2O32- = 2I- + S4O62-),消耗Na2S2O3溶液6.45mL。
(1)写出步骤①溶解Cu的离子方程式 。
(2)判断步骤②滴定终点的方法是 。
(3)计算合金中Cu的质量分数.
20(8分)锌铝合金的主要成分有Zn、Al、Cu、Si等元素。实验室测定其中Cu含量的步骤如下:①称取该合金样品

 (5)写出以
(5)写出以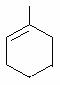 为原料(无机试剂任选)合成H [ OCH(CH3)(CH2)4CO ]nOH流程图。
为原料(无机试剂任选)合成H [ OCH(CH3)(CH2)4CO ]nOH流程图。
合成苯醚菊酯的菊酸部分一直是科学难题。M.Matsuda曾采用天然松节油成分中的蒈烯(Carene)E为原料,经过6步反应制得了菊酸,其合成步骤可表示为: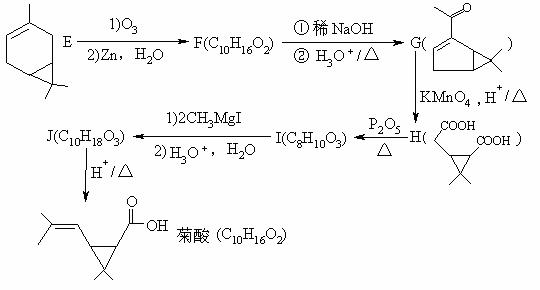
试回答下列问题:
(1) 写出F、I的结构简式。F I 。
(2)F→G包含的反应类型为: 、 。
(3)写出J→菊酸的反应方程式: 。菊酸分子中手性碳原子有 个。
(4)化合物G的一类同分异构体具有如下特点:遇FeCl3溶液现紫色,苯环上的一氯取代物有2种。化合物G的此类同分异构体共有 种
③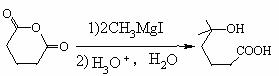
②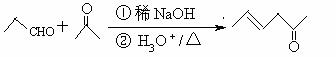
 19(12分)已高考资源网知:①CH3CH=C(CH3)2
CH3CHO+(CH3)
19(12分)已高考资源网知:①CH3CH=C(CH3)2
CH3CHO+(CH3)
|