
7.0
90.0
30.(18分)
正常成年人生成尿的过程中,部分液体若干成分的含量如下表所示。请参照图3中所提供的信息和表中数据,回答以下问题:
成分
水分
蛋白质
葡萄糖
尿素
K+
Na+
Cl―
血浆/g.dL-1
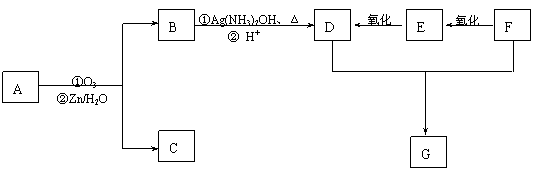

请回答:
(1)B中的官能团名称为 . 。
(2)E与足量的新制氢氧化铜悬浊液反应的化学方程式为
。
(3)D与F反应生成G的化学方程式为 ;分子中有2个羧基.且能使Br2的CCl4溶液褪色的G的同分异构体有 . (写结构简式)。
(4)A的结构简式为 ;A的加聚产物是一种功能高分子材料,其结构简式为 。
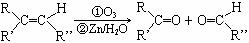
现有如下转化关系,其中A是蜂王浆中的有效成分,分子式为C10H18O3,具有酸性。B能被NaOH溶液中和。C中没有支链,也不含―CH3。G是六元环状化合物,分子式为C4H4O4。
29.(16分)
已知一定条件下,烯烃可发生下列反应:
28.(15分)
乙二酸(HOOC―COOH)俗称草酸。某校学生为探究乙二酸的部分化学性质,进行了下述实验:
(1)向盛有少量乙二酸饱和溶液的试管内滴入用硫酸酸化的KMnO4稀溶液,振荡,观察到的现象为 ,说明乙二酸具有 (填“氧化性”.“还原性”或“酸性”)。
(2)向图甲的A试管中加入乙二醇.浓硫酸和乙二酸,用酒精灯小火均匀加热试管3 ~ 5 min,在B试管中有油状液体产生,若反应中生成了六元环状化合物,该反应的化学方程式为 ,其中B试管中的导管不伸入液面下的原因是 ,饱和碳酸钠溶液的作用是
。
(3)已知:草酸在约
①从减少污染的角度看,应增加尾气处理装置,你如何进行尾气处理
。
②依据题给数据,请分析D试管中能否确定草酸分解产物中有CO2 (填“能确定”或“不能确定”),理由是
。
(3)将
(4)常温下,甲与乙的水溶液pH均为9,这两种溶液中由水电离出的OH- 的物质的量浓度c(OH-)甲: c(OH-)乙 = 。
(5)浓氨水与固体甲混合,可用于快速制取少量氨气,其原因是
(请用必要的方程式和简要的文字加以说明)。
27.(17分)
A.B.C.D四种短周期元素,原子序数依次递增,A原子形成的阳离子就是一个质子,B原子的最外层电子数是次外层的2倍,C原子的最外层电子数与B原子的核外电子总数相等,D在同周期元素中原子半径最大。A.C.D三种元素可形成化合物甲,B.C.D三种元素可形成化合物乙,甲与乙均为中学化学常见物质。
请回答:
(1)甲的电子式为 ,其中所含化学键类型为 。
(2)A的单质与C的单质在碱性条件下可以构成燃料电池,其正极反应式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com