
| A��25��ʱ��0.1mol/L�Ĵ�����Һ��0.01mol/L�Ĵ�����Һ��KֵС |
| B��25��ʱ�����ȵ���0.1mol/L�Ĵ�����Һ�У���Һ�ʻ�ɫ |
| C��������ˮ��̼�����Ʋ���Ӧ |
| D�������ʵ���Ũ�ȵ�̼������Һ����������Һ������������Һ��pH��pH��Na2CO3����pH��NaClO����pH��CH3COONa�� |
| 1.8��10 -5��0.1 |


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
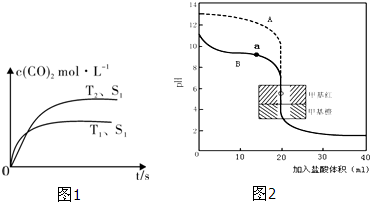
| ���� |
| �¶ȣ��棩 | 250 | 300 | 350 |
| K | 2.041 | 0.270 | 0.012 |
| ʱ�䣨min�� | 5 | 10 | 15 | 20 | 25 | 30 |
| ѹǿ�ȣ�P��/Pǰ�� | 0.98 | 0.90 | 0.80 | 0.70 | 0.70 | 0.70 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
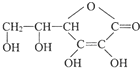
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������ˮ�м������NaOH��[Na+]=[Cl-]+[ClO-]+[OH-] |
| B��pH=8.3��NaHCO3��Һ��[Na+]��[HCO3-]��[CO32-]��[H2CO3] |
| C��pH=11�İ�ˮ��pH=3������������ϣ�[Cl-]=[NH4+]��[OH-]=[H+] |
| D��0.2mol?L-1CH3COOH��Һ��0.1mol?L-1NaOH��Һ�������ϣ�2[H+]-2[OH-]=[CH3COO-]-[CH3COOH] |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������10 s |
| B������12 s |
| C������12 s |
| D����12 s |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ʱ����������ڳ���ֽ�ϣ�����������ƽ�����̣��������������ƽ�������� |
| B����Һʱ����Һ©�����²�Һ����¿ڷų����ϲ�Һ����Ͽڵ��� |
| C�����Ȼ��ƹ����������ƿ�У�Ȼ���ˮϡ����ȡ�Ȼ�����Һ |
| D������ʱ��Ӧʹ�¶ȼ�ˮ����������ƿ֧�ܿ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
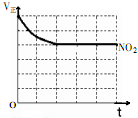 ���Ǵ����к����ḻ��һ��Ԫ�أ���ش����к����仯�����������⣺
���Ǵ����к����ḻ��һ��Ԫ�أ���ش����к����仯�����������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����п���ʴ��������Ϊ��������γ����ܵ�����Ĥ |
| B���ڸ��������ܽ��������е����û����� |
| C����������������ǿ�ᷴӦ������ǿ����Һ��Ӧ |
| D��������������������ʢ��Ũ�����Ũ���ᣬ����Ϊ���ڳ����²��������Ƿ�����Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com