
| A、等于10 s |
| B、等于12 s |
| C、大于12 s |
| D、小于12 s |
| △c |
| △t |
| 0.1mol/L-0.06mol/L |
| 20s |
| 0.024mol/L |
| 0.002mol/L?s |


科目:高中化学 来源: 题型:
| 阳离子 | K+ Al3+ Fe2+ Ba2+ |
| 阴离子 | OH- Cl- SO42- HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验序号 | 实验内容 | 实验结果 |
| 1 | 加AgNO3 溶液 | 有白色沉淀生成 |
| 2 | 加足量NaOH 溶液并加热 | 收集到气体1.12L(已折算成标准状况下的体积) |
| 3 | 加足量BaCl2 溶液,对所得沉淀进行洗涤、干燥、称量;再向沉淀中加足量稀盐酸,然后干燥、称量 | 第一次称量读数为6.27g,第二次称量读数为2.33g |
| 阴离子符号 | 物质的量浓度(mol?L-1) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,等浓度的醋酸比盐酸导电能力弱 |
| B、常温下,测得0.1 mol?L-1醋酸溶液的pH=4 |
| C、常温下,将pH=1的醋酸溶液稀释1000倍,测得pH<4 |
| D、常温下,将物质的量浓度相同的醋酸溶液与氢氧化钠溶液等体积混合后恰好中和 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、25℃时,0.1mol/L的醋酸溶液比0.01mol/L的醋酸溶液的K值小 |
| B、25℃时,甲基橙滴入0.1mol/L的醋酸溶液中,溶液呈黄色 |
| C、新制氯水与碳酸氢钠不反应 |
| D、等物质的量浓度的碳酸钠溶液、醋酸钠溶液、次氯酸钠溶液的pH:pH(Na2CO3)>pH(NaClO)>pH(CH3COONa) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若a+b<c+d,则反应一定能自发向右进行 |
| B、若从正反应开始,起始时A、B的物质的量之比为a:b,则平衡时A、B的转化率之比也为a:b |
| C、若a+b=c+d,在平衡体系中共有气体m mol,再向其中充入n mol B,则达到平衡时气体总物质的量小于(m+n)mol |
| D、若a+b=c+d,则对于体积不变的容器,升高温度,平衡向左移动,容器中气体的压强一定不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入Ba(NO3)2溶液产生白色的沉淀. |
| B、加入碘水变蓝 |
| C、加入Ba(NO3)2溶液没有白色沉淀 |
| D、加入碘水不变蓝 |
查看答案和解析>>
科目:高中化学 来源: 题型:
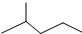 表示的分子式
表示的分子式查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com