
| 实验编号 | HA物质的量浓度 (mol?L-1) | NaOH物质的量浓度 (mol?L-1) | 混合溶液的pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH<7 |


 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、“夺命快递”事件中的有毒物质为氟乙酸甲酯 ,能发生消去、水解、氧化反应 ,能发生消去、水解、氧化反应 |
| B、用盐析的方法分离油脂皂化反应的产物 |
| C、利用丁达尔效应可以区别溶液和胶体 |
| D、用酒精清洗粘到皮肤上的苯酚 |
查看答案和解析>>
科目:高中化学 来源: 题型:
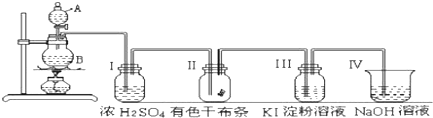
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,等浓度的醋酸比盐酸导电能力弱 |
| B、常温下,测得0.1 mol?L-1醋酸溶液的pH=4 |
| C、常温下,将pH=1的醋酸溶液稀释1000倍,测得pH<4 |
| D、常温下,将物质的量浓度相同的醋酸溶液与氢氧化钠溶液等体积混合后恰好中和 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 2SO2+O2?2SO3 的平衡体系中,加入由18O构成的氧气,则SO2中的18O的含量会增加 |  I2(g)+H2(g)2HI(g)加压后颜色加深 |
|
| ||||||||||||
| A | B | C | D |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com