
题目列表(包括答案和解析)
2.(09年四川卷)关于热力学定律,下列说法正确的是()
A.在一定条件下物体的温度可以降到0 K
B.物体从单一热源吸收的热量可全部用于做功
C.吸收了热量的物体,其内能一定增加
D.压缩气体总能使气体的温度升高
1.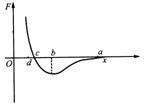 如图所示,甲分子固定在坐标原点
如图所示,甲分子固定在坐标原点 ,乙分子位于
,乙分子位于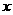 轴上,甲分子对乙分子的作用与两分子间距离的关系如图中曲线所示,
轴上,甲分子对乙分子的作用与两分子间距离的关系如图中曲线所示,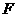 >0为斥力,
>0为斥力,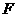 <0为引力,
<0为引力,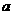 、
、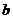 、
、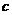 、
、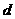 为
为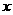 轴上4个特定的位置.现有乙分子从a处由静止释放,则( )
轴上4个特定的位置.现有乙分子从a处由静止释放,则( )
A.乙分子从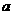 到
到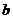 做加速运动,由
做加速运动,由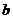 到
到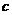 做减速运动
做减速运动
B.乙分子由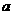 到c做加速运动,到达
到c做加速运动,到达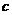 时速度最大
时速度最大
C.乙分子由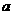 到
到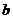 的过程中,两分子间的分子势能一直减少
的过程中,两分子间的分子势能一直减少
D.乙分子由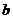 到
到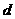 的过程中,两分子间的分子势能一直增加
的过程中,两分子间的分子势能一直增加
3.气体的压强与大气压的区别
气体的压强是由于气体分子频繁碰撞器壁而产生的.压强的大小跟两个因素有关:①气体分子的平均动能,②分子的密集程度.一般情况下不考虑气体本身的重量,所以同一容器内气体的压强处处相等.但大气压在宏观上可以看成是大气受地球吸引而产生的重力而引起的.(例如在估算地球大气的总重量时可以用标准大气压乘以地球表面积).
|

封闭气体压强的计算方法
(1)求解思路:选取与气体接触的液柱(或活塞、汽缸)为研究对象,进行受力分析;再根据运动状态列出相应的平衡方程或运用牛顿第二定律列式,从而求出压强.
(2)气体压强的计算常要用到以下知识
①若液面与外界大气相接触,液面下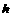 深处的压强
深处的压强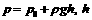 为竖直深度.
为竖直深度.
②与外界相通时,容器内的压强等于外界大气压;用细管相连通的两容器,平衡时两边气体的压强相等.
③连通器原理:在连通器中,同一种液体(中间不间断)的同一水平面上压强相等.
④帕斯卡定律:加在密闭、静止液体(或气体)上的压强,能够大小不变地由液体(或气体)向各个方面传递.
|

例1.甲、乙两个相同的密闭容器中分别装有等质量的同种气体,已知甲、乙容器中气体的压强分别为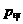 、
、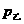 ,且
,且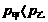 ,则
,则
A.甲容器中气体的温度高于乙容器中气体的温度
B.甲容器中气体的温度低于乙容器中气体的温度
C. 甲容器中气体分子的平均动能小于乙容器中气体分子的平均动能
D. 甲容器中气体分子的平均动能大于乙容器中气体分子的平均动能
解析:单位体积内的分子数越多,分子在单位时间内碰撞单位面积器壁的次数越多,压强就越大;温度升高,气体分子运动的平均动能越大,分子撞击器壁的作用力就会越大,气体的压强也就越大。甲、乙两个相同的密闭容器中分别装有等质量的同种气体,那么甲、乙容器中单位体积内的分子数相同,而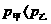 ,说明甲容器中气体的温度低于乙容器中气体的温度,所以BC正确
,说明甲容器中气体的温度低于乙容器中气体的温度,所以BC正确
变式训练1:对一定量的气体,若用N表示单位时间内与器壁单位面积碰撞的分子数,则( )
A.当体积减小时,N必定增加
B.当温度升高时,N必定增加
C.当压强不变而体积和温度变化时,N必定变化
D.当压强不变而体积和温度变化时,N可能不变
解析:因为单位时间内与与器壁单位面积碰撞的分子数与分子的密集程度和和分子的平均动能有关.即与气体的温度和体积有关, 当体积减小时,单位体积的分子数分子增加,但温度变化未知,所以N不一定增加,A项错;当温度升高时,分子的平均动能增大,但气体的体积可能增大,N不一定增大,B项错;当压强不变时,即单位时间内,器壁单位面积压力不变,体积和温度变化时,分子的平均动能变化,而压强不变,则N必定变化,所以C对而D错
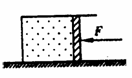 例2.如图8-3-1所示,一个壁厚可以不计、质量为M的气缸放在光滑的水平地面上,活塞的质量为m,面积为S,内部封有一定质量的气体.活塞不漏气,摩擦不计,外界大气压强为P0,若在活塞上加一水平向左的恒力F(不考虑气体温度的变化),求气缸和活塞以共同加速度运动时,缸内气体的压强多大?
图8-3-1
例2.如图8-3-1所示,一个壁厚可以不计、质量为M的气缸放在光滑的水平地面上,活塞的质量为m,面积为S,内部封有一定质量的气体.活塞不漏气,摩擦不计,外界大气压强为P0,若在活塞上加一水平向左的恒力F(不考虑气体温度的变化),求气缸和活塞以共同加速度运动时,缸内气体的压强多大?
图8-3-1
解析:设稳定时气体和活塞共同以加速度A向左做匀速运动,这 时缺内气体的压强为P,分析它们的受力情况,分别列出它们的运动方程为
气缸: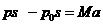 ①
①
活塞: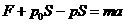 ②
②
将上述两式相加,可得系统加速度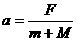
将其代入①式,化简即得封闭气体的压强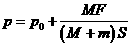
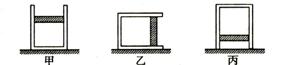
变式训练2:如图8-3-2所示,活塞封闭的容器中装有一定量的气体,活塞与容器内壁无摩擦,现先后将容器按甲、乙、丙三种方式放置,则稳定时,甲、乙、丙三种状态下被封闭气体的压强有( )
A.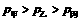 B.
B. 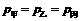 图8-3-2
图8-3-2
C. 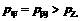 D.
D. 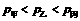
解析:A 取活塞为研究对象分别进行受力分析,由平衡条件得:
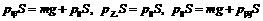 故
故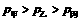 ,所以选项A正确
,所以选项A正确
热学单元测试题
2.决定压强的大小的因素:从微观上看,气体压强由分子的平均动能和单位体积的分子数(即气体分子的密集程度)决定.因为平均动能越大,分子撞击器壁时对器壁产生的作用力越大,气体的压强越大;气体分子越密集,每秒撞击器壁单位面积的分子数越多,气体的压强越大.从宏观是看,气体压强的大小由温度和体积决定:因为温度是分子平均动能的标志,气体压强在微观上与分子的平均动能有关,所以气体压强一定与温度有关;一定质量的气体,体积越小,分子越密集,所以气体压强与体积有关.
1.产生原因:气体的压强是大量分子频繁碰撞器壁产生的.
3.理想气体与实际气体
从宏观上讲,理想气体就是严格遵守气体三个实验定律的气体,从微观上讲,气体分子的大小与气体分子间的距离比较可以忽略不计;气体分子看成弹性小球,它们相撞或与器壁相撞时,遵守能量守恒和动量守恒;分子间除碰撞的瞬间外,分子间相互作用不考虑,分子所受重力也忽略不计.理想气体的内能只考虑分子平均动能,分子势能不考虑,一定质量的理想气体内能U只是温度的函数. 实际气体温度跟室温相比不太低,压强跟大气压相比不太大的情况下可视为理想气体.
2.每个气体分子的运动是杂乱无章的,但对大量分子的整体来说,分子的运动是有规律的.分子数表现出“中部多,两头少”的统计规律,所以研究的方法是统计方法.气体分子的速率分布规律遵从统计规律.在一定温度下,某种气体的分子速率分布是确定的,可以求出这个温度下该种气体分子的平均速率.
1.气体分子间的距离大约是分子直径的10倍,分子间的作用力十分微弱.通常认为,气体分子除了相互碰撞或碰撞器壁外,不受力的作用.
3. 一定质量的气体,在压强不变时,温度升高,体积增大.
|

2. 一定质量的气体,在体积不变时,温度升高,压强增大.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com