
题目列表(包括答案和解析)
17、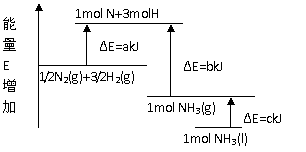 化学反应N2+3H2
=2NH3的能量变化如右图所示,该反应的热化学方程式可以写作( )
化学反应N2+3H2
=2NH3的能量变化如右图所示,该反应的热化学方程式可以写作( )
A. N2(g)+3H2(g) =2NH3(l)
ΔH =2(a-b-c) kJ·mol-1
B. N2(g)+3H2(g) =2NH3(g)
ΔH =2(b -a ) kJ·mol-1
C. 1/2N2(g)+3/2H2(g) =NH3(l)
ΔH =( b+c -a) kJ·mol-1
D. 1/2N2(g)+3/2H2(g) =NH3(g) ΔH =( a + b) kJ·mol-1
16、下列溶液中有关物质的量浓度关系正确的是( )
A.pH=2的HA溶液与pH=12的MOH溶液任意比混合:
c(H+) + c(M+) = c(OH-) + c(A-)
B.pH相等的CH3COONa、NaOH和Na2CO3三种溶液:
c(NaOH)<c(CH3COONa)<c(Na2CO3)
C.物质的量浓度相等CH3COOH和CH3COONa溶液等体积混合:
c(CH3COO-) + c(OH-) = 2c(H+) + c(CH3COOH)
D.0.1mol/L的NaHA溶液,其pH = 4:c(HA-)>c(H+)>c(H2A)>c(A2-)
15、 在250C时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表。下列说法错误的是
在250C时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表。下列说法错误的是 (
)
(
)
|
物质 |
X |
Y |
Z |
|
初始浓度/ mol•L-1 |
0.1 |
0.2 |
0 |
|
平衡浓度/ mol•L-1 |
0.05 |
0.05 |
0.1 |





 A.反应达到平衡时,X的转化率为50%
A.反应达到平衡时,X的转化率为50%
 B.反应可表示为X+3Y ⇋ 2Z,其平衡常数为1600
B.反应可表示为X+3Y ⇋ 2Z,其平衡常数为1600
 C.增大压强使平衡向生成Z的方向移动,平衡常数增大
C.增大压强使平衡向生成Z的方向移动,平衡常数增大
 D.改变温度可以改变此反应的平衡常数
D.改变温度可以改变此反应的平衡常数
14、对于难溶化合物AgCl来说,一定温度下,当其在水中达到溶解平衡时,银离子浓度与氯离子浓度之积是一个常数,叫做溶度积常数,用Ksp表示,即
Ksp=c(Ag+)·c(Cl-)。一定温度下,分别把 1 g AgCl 固体放于下列各不同溶液里,充分搅拌使其达到溶解平衡后,剩余固体质量最大的是( )
A.20 mL 0.1 mol/LKCl溶液 B.20 mL 0.1 mol /L MgCl2溶液
C.20 mL 0.2 mol /L CaCl2溶液 D.20 mL 0.15 mol /L AlCl3溶液
13、强酸与强碱的稀溶液发生中和反应生成1mol水热效应:
H+(aq)+ OH- (aq)= H2O(l) △H=-57.3kJ/mol。向1L0.5mol/L的NaOH溶液中加入下列物质:①稀醋酸 ②浓硫酸 ③稀硝酸,恰好完全反应时的热效应△H1、△H2、△H3的关系正确的是 ( )
A.△H1>△H2>△H3 B.△H1<△H3<△H2
C.△H1<△H2<△H3 D.△H1>△H3>△H2
12、若溶液中由水电离产生的c(OH-)=1×10-14 mol·L-1,满足此条件的溶液中一定可以大量共存的离子组是( )
A.Al3+、Na+、NO3-、Cl- B.K+、Na+、Cl-、NO3-
C.K+、Na+、Cl-、AlO2- D.K+、NH4+、SO42-、NO3
11、将①H+、②Cl-、③Al3+、④K+、⑤S2-、⑥OH-、⑦NO3-、⑧NH4+分别加入H2O中,基本上不影响水的电离平衡的是( )
A.①③⑤⑦⑧ B.②④⑦ C.①⑥ D.②④⑥⑧
10、下列事实中,不能用勒夏特列原理解释的是( )
A.溴水中存在如下平衡Br2+H2O ⇋ HBr +HBrO ,当加入NaOH溶液时颜色将变浅
B.增加压强时,平衡体系2HI ⇋ H2+ I2(g)的颜色将变深
C.升高温度时,可逆反应CO +NO2 ⇋ CO2 +NO (△H<0)的平衡将向逆方向移动
D.合成氨反应N2+3H2
 2NH3(△H<0),为使氨的产率提高,理论上应采取低温和高压的措施
2NH3(△H<0),为使氨的产率提高,理论上应采取低温和高压的措施
9、漂白剂亚氯酸钠(NaClO2)在常温与黑暗处可保存一年。亚氯酸不稳定可分解,反应的离子方程式为5HClO2=4ClO2↑+H++Cl-+2H2O。向NaClO2溶液中滴加H2SO4,开始反应缓慢,随后反应迅速,其原因是( )
A.在酸性条件下亚氯酸的氧化性增强 B.溶液中的H+起催化作用
C.ClO2逸出,使生成物的浓度降低 D.溶液中的Cl-起催化作用
8、在密闭容器中进行下列反应M(g)+N(g) ⇋ R(g)+2L,此反应符合下
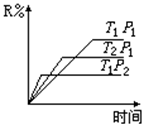 面图像,下列叙述正确的是( )
面图像,下列叙述正确的是( )
A.正反应吸热,L是气体
B.正反应吸热,L是固体
C.正反应放热,L是气体
D.正反应放热,L是固体或液体
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com