
题目列表(包括答案和解析)
23、用Pt电极电解KCl和CuSO4的混合溶液,当电路中通过0.4mol电子的电量时,阴阳两极都产生0.14mol的气体,若电解后溶液体积为40L,则电解后溶液的pH为( )
A、1 B、3 C、7 D、11
22、在1LK2SO4和CuSO4的混合溶液中,c(SO42-)=2.0 mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4L(标准状况)气体,则原溶液中K+的物质的量浓度为( )
A、2.0 mol·L-1 B、1.5 mol·L-1 C、1.0 mol·L-1 D、0.5 mol·L-1
21、一种新型燃料电池,一极通入空气,另一极通入丁烷气体,电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。下列对该燃料的说法正确的是
( )
A、在熔融电解质中,O2-由负极移向正极
B、电池的总反应是:C4H10 + 13O2 → 4CO2 + 5H2O
C、通入空气的一极是正极,电极反应为:O2 + 4e- =2O2-
D、通入丁烷的一极是正极,电极反应为:C4H10 + 26e- +13O2- =4CO2↑+ 5 H2O
20、将等物质的量的K2SO4、NaCl、Ba(NO3)2、AgNO3混合均匀后,置于指定容器中,加入足量的水,搅拌、静置、过滤。取滤液,用铂电极电解一段时间。则分别在两极区析出的氧化产物与还原产物的质量比约为( )
A、35.5:108 B、108:35.5 C、8:1 D、1:2
19、在一定体积pH=12的Ba(OH)2溶液中,逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液pH=11,若反应后溶液的体积等于Ba(OH)2溶液与NaHSO4溶液体积之和,则Ba(OH)2溶液与NaHSO4溶液体积之比是( )
A、1:9 B、1:1 C、1:2 D、1:4
18、高铁电池是一种新型可充电电池,与普通高能电池相比,该电池长时间保持稳定的放电电压。高铁电池的总反应为:3Zn +2K2FeO4 +8H2O 3Zn(OH)2
+2Fe(OH)3 + 4KOH,下列叙述不正确的是(
)
3Zn(OH)2
+2Fe(OH)3 + 4KOH,下列叙述不正确的是(
)
A、放电时负极反应为:Zn – 2e- + 2OH- = Zn(OH)2
B、充电时阳极反应为:Fe(OH)3 - 3e- + 5OH- = FeO42- + 4H2O
C、放电时每转移3mol电子,正极有1mol K2FeO4被氧化
D、放电时正极附近溶液的碱性增强
17、已知铅蓄电池放电时发生如下反应:负极:Pb+SO42- -2e- =PbSO4,
正极:PbO2 + 4H+ + SO42- + 2e- = PbSO4 + 2H2O。实验室用铅蓄电池作电源,用惰性电极电解CuSO4溶液,当阴极析出2.4g铜时,铅蓄电池内消耗H2SO4物质的量至少是
( )
A、0.050mol B、0.075mol C、0.20mol D、0.40mol
16、原电池的电极名称不仅与电极材料的性质有关,也与电解质溶液有关。下列说法中不正确的是( )
A、由Al、Cu、稀H2SO4组成原电池,其负极反应式为:Al - 3eˉ=Al3+
B、由Mg、Al、NaOH溶液组成原电池,其负极反应式为:
Al - 3eˉ+ 4OHˉ=AlO2ˉ+ 2H2O
C、由Fe、Cu、FeCl3溶液组成原电池,其负极反应式为:Cu - 2eˉ=Cu2+
D、由Al、Cu、浓硝酸组成原电池,其负极反应式为:Cu - 2eˉ=Cu2+
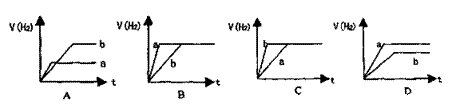
15、将等质量的两份锌粉a和b,分别加入两个盛过量的稀硫酸的烧杯中,并向加入a的烧杯中再加入少量CuO粉末。下列各图表示氢气体积V(H2)与反应时间t的关系,其中正确的是 ( A )
14、把Ca(OH)2固体放入一定量的蒸馏水中,一定温度下达到平衡:Ca(OH)2 
Ca2+(aq)+2OH-(aq)。当向悬浊液中加入少量生石灰后,若温度保持不变,下列判断正确的是( )
A、溶液的pH增大 B、溶液的pH不变
C、溶液中Ca2+数目增多 D、溶液中c(Ca2+)增大
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com