
题目列表(包括答案和解析)
10.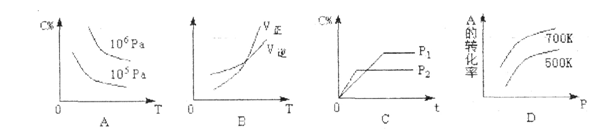
 对于2A(g)+B(g)
对于2A(g)+B(g) 2C(g)(正反应为放热反应),下列图象符合该反应的是 ( )
2C(g)(正反应为放热反应),下列图象符合该反应的是 ( )
9.在一定条件下,在容积为2L的密闭容器中,将2 mol M气体和3 mol N气体混合,发生如下反应:2M(g) + 3N (g) x Q (g) +3R(g),经过2分钟该反应达平衡,生成2.4mol R,并测得用Q表示的反应速率为0.2
mol/(L·min),下列有关叙述正确的是(
)
x Q (g) +3R(g),经过2分钟该反应达平衡,生成2.4mol R,并测得用Q表示的反应速率为0.2
mol/(L·min),下列有关叙述正确的是(
)
A.x值为2 B.混合气体的密度增大
C.平衡时N的浓度为0.3 mol/L D.N的转化率为60%
8.对于已达化学平衡的可逆反应,如果改变某种条件,结果某生成物的浓度增大,则( )
A.反应物的转化率一定增大 B.平衡一定向逆反应方向移动
C.反应物的浓度相应减小 D.平衡可能移动也可能没有移动
7.在一定温度下的固定容积的密闭容器中,当下列物理量不再变化时,表明反应:
A(s)+2B(g) C(g)+D(g) 已达平衡的是 ( )
C(g)+D(g) 已达平衡的是 ( )
A.混合气体的压强 B.混合气体的密度
C.生成l mol C的同时生成l mol D D.气体的总物质的量
6、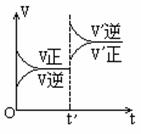 对达到平衡状态的可逆反应:X+Y
对达到平衡状态的可逆反应:X+Y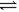 W+Z,在t'时增大压强,则正逆反应速率变化如下图所示(V代表速率,t代表时间。下列有关X、Y、Z、W的状态叙述正确的是( )
W+Z,在t'时增大压强,则正逆反应速率变化如下图所示(V代表速率,t代表时间。下列有关X、Y、Z、W的状态叙述正确的是( )
A.X、Y、W为气体,Z不是气体
B.X、Y为气体,W、Z中有一种是气体
C.W、Z为气体,X、Y中有一种是气体
D.W、Z中有一种为气体,X、Y都不是气体
5. 在一定温度下将l mol CO和3 mol水蒸气放在密闭的容器中发生下列反应:
CO(g) + H2O(g )  CO2(g) + H2(g), 达到平衡后,测得CO2为0.75mol ;再通入6mol水蒸气,达到新的平衡后,CO2和H2的物质的量之和可能为 ( )
CO2(g) + H2(g), 达到平衡后,测得CO2为0.75mol ;再通入6mol水蒸气,达到新的平衡后,CO2和H2的物质的量之和可能为 ( )
A.1.2mol B.1.5mol C.1.8mol D.2.5mol
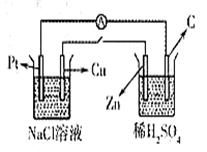
4.如图所示,将两烧杯用导线如图相连,Pt、Cu、Zn、C分别为四个电极,当闭合开关后,以下叙述正确的是( )
A.Cu极附近OH-浓度增大
B.Cu极为原电池负极
C.电子流向是由C极流向Pt极
D.当C极上有4mol电子转移时,Pt极上有1molO2生成
3.市场上经常见到的标记为Li-ion的电池称为“锂离子电池”。它的负极材料是金属锂和碳的复
 合材料(碳作为金属锂的载体),电解质为一种能传导Li
合材料(碳作为金属锂的载体),电解质为一种能传导Li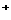 的高分子材料。这种锂离子电池的电池反应为: Li + 2 Li ,
下列说法不正确的是( )
的高分子材料。这种锂离子电池的电池反应为: Li + 2 Li ,
下列说法不正确的是( )
A.放电时,负极的电极反应式:Li → Li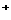 + e
+ e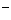
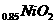 B.充电时,Li
既发生氧化反应又发生还原反应
B.充电时,Li
既发生氧化反应又发生还原反应
C.该电池不能用水溶液作为电解质
 D.放电过程中Li
D.放电过程中Li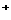 向负极移动
向负极移动
1.下列关于反应热的说法正确的是( )
A.当∆H为“-”时,表示该反应为吸热反应
B.反应热的大小与反应物所具有的能量和生成物所具有的能量无关
C.化学反应的反应热只与反应体系的始态和终点状态有关,而与反应的途径无关
D.由热化学方程式 H2(g)+F2(g) = 2HF(g) △H=-270 kJ/mol可知 2L氟化氢气体分解成1L的氢气和1L的氟气吸收270kJ热量
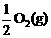 2.已知:2CO(g)+O2(g)=2CO2(g) ΔH=
-566 kJ/mol
2.已知:2CO(g)+O2(g)=2CO2(g) ΔH=
-566 kJ/mol
Na2O2(s) +CO2(g) = Na2CO3(s) + △H= -226 kJ/mol
根据以上热化学方程式判断,下列说法正确的是( )
A.CO的燃烧热为283 kJ
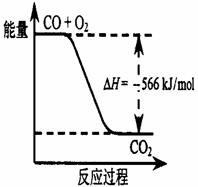
B.下图可表示由1molCO生成CO2的反应过程和能量关系
C.2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g)ΔH>- 452 kJ/mol
D. CO(g)与Na2O2 (s)反应放出509 kJ热量时,电子转移数为6.02×1023
35.(6分) 煤等化石燃料燃烧时产生的SO2会对大气造成污染。若某家庭取暖每天燃烧6 kg 煤,煤中硫元素的质量分数为1%。假设煤中的硫全部转化为SO2,试计算每天产生的SO2的物质的量是多少?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com