
题目列表(包括答案和解析)
20.25℃和1.01×10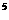 Pa时,反应
Pa时,反应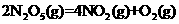 △H=+56.76kJ/mol能自发进行的原因是
△H=+56.76kJ/mol能自发进行的原因是
A.反应吸热 B.反应放热
C.反应的熵值减小 D.熵增大效应大于能量效应
19.将固体NH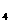 I置于密闭容器中,在一定温度下发生下列反应:①
I置于密闭容器中,在一定温度下发生下列反应:①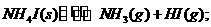 ②
②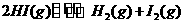 。达到平衡时,
。达到平衡时,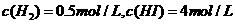 , 则此温度下反应①的平衡常数为
, 则此温度下反应①的平衡常数为
A.9 B.16 C.20 D.25
18.下列溶液混合后,常温下一定呈碱性的是
A.pH=12的氢氧化钡溶液与pH=2的盐酸等体积混合
B.0.01mol/L醋酸溶液与pH=12氢氧化钠溶液等体积混合
C.pH=2的醋酸溶液与pH=12的氢氧化钠溶液等体积混合
D.1×10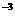 mol/L的盐酸和4×10
mol/L的盐酸和4×10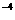 mol/L的氢氧化钡溶液等体积混合后再稀释100倍
mol/L的氢氧化钡溶液等体积混合后再稀释100倍
17.下列事实中不能用勒夏特列原理解释的是
A.溴水中有平衡: ,当加入
,当加入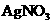 溶液后,溶液颜色变浅
溶液后,溶液颜色变浅
B.对 的平衡体系,增大压强可使颜色变深
的平衡体系,增大压强可使颜色变深
C.在电解含有酚酞的硫酸钠溶液时,阴极附近溶液的颜色变红
D.合成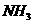 反应正反应放热,为提高NH3的产率,理论上应采用降温措施
反应正反应放热,为提高NH3的产率,理论上应采用降温措施
16.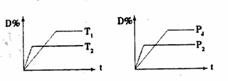 可逆反应
可逆反应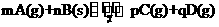 ,当其他条件不变时,D的百分含量与温度(T)和压强(P)的关系如图所示。下列叙述中不正确的是
,当其他条件不变时,D的百分含量与温度(T)和压强(P)的关系如图所示。下列叙述中不正确的是
A.达到平衡后,升高温度,平衡向逆反应方向移动
B.达到平衡后,若使用催化剂,D的物质的量分数不变
C.化学方程式中一定有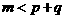
D.平衡后增大B的量,有利于平衡向正反应方向移动
15.已知反应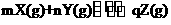 的△H<0,m+n>q。在一定温度一定体积的密闭容器中反应达到平衡时,下列说法正确的是
的△H<0,m+n>q。在一定温度一定体积的密闭容器中反应达到平衡时,下列说法正确的是
A.通入稀有气体使压强增大,平衡将正向移动
B.X的正反应速率是Y的逆反应速率的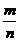 倍
倍
C.降低温度.混合气体的平均相对分子质量变小
D.若X、Y的转化率相等.说明反应开始时X、Y的物质的量之比为n:m
14.某温度下的密闭容器中,1 mol  l mol H2O(g)反应达平衡时生成
l mol H2O(g)反应达平衡时生成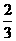 mol
mol 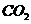 。若将
。若将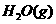 改为4 mol,在相同条件下反应生成
改为4 mol,在相同条件下反应生成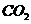 的物质的量为
的物质的量为
A.0.05.mol B.0.5 mol C.0.93 mol D.1 mol
13.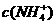 相同的下列各溶液中,物质的量浓度最大的是
相同的下列各溶液中,物质的量浓度最大的是
A.NH4AI(SO4)2 B.CH3COONK4
C.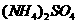 D.
D.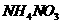
12.下列说法正确的是
A.增大反应物浓度,可增大单位体积内活化分子的百分数,反应速率加快
B.温度对吸热反应速率影响程度大
C.对于反应前后气体总体积不变的反应,压强对速率无影响
D.催化剂不影响反应活化能,对反应速率无影响
11.pH=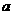 的某电解质溶液中,插入两支惰性电极通直流电一段时间后,溶液的pH>
的某电解质溶液中,插入两支惰性电极通直流电一段时间后,溶液的pH>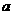 ,则
,则
该电解质可能是
A.NaOH B.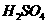 C.AgNO
C.AgNO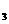 D.
D.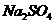
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com