
题目列表(包括答案和解析)
30.容积确定的密闭容器中发生反应: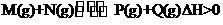 。请回答下列问题:
。请回答下列问题:
(1)在某温度下,反应物的起始浓度分别为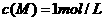 ,
,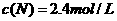 ;达到平衡后,M的转化率为60%,此时N的转化率为
。
;达到平衡后,M的转化率为60%,此时N的转化率为
。
(2)若反应温度不变,反应物的起始浓度分别为:c(M);1mol/L,c(N)=2.4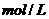 ;达到平衡后,
;达到平衡后,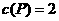
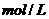 ,则
,则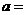 。
。
(3)下列能使M的转化率增大的方法有、
A.升高温度 B.增大M的起始浓度
C.增大N的起始浓度
D.反应物的起始浓度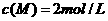 ,
,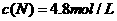
E.使用催化剂
(4)能说明该反应已达到平衡状态的是
A.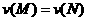 B.
B.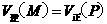 C.
C.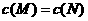
D.容器内压强保持不变 E.容器内密度保持不变
29.(1)将等体积等物质的量浓度的盐酸和氨水混合后,溶液呈
性,溶液中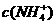
。c(Cl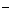 )(填“>”“<”或“=”);
)(填“>”“<”或“=”);
(2)将pH=3的盐酸和。pH=11的氨水等体积混合后,溶液呈 性,溶液中c(NH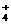 )
)
c(Cl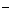 )(填“>”“<”或“=”);
)(填“>”“<”或“=”);
(3)将物质的量浓度相同的盐酸与氨水混合后,溶液中c( )与c(
)与c( )相等,则混合溶液呈
性,盐酸体积 氨水体积(填“>”“<”或“=”);
)相等,则混合溶液呈
性,盐酸体积 氨水体积(填“>”“<”或“=”);
(4)将m 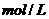 的盐酸和n
的盐酸和n  /L氨水等体积混合后,c(H
/L氨水等体积混合后,c(H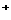 )>c(NH
)>c(NH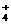 ),混合溶液呈
),混合溶液呈
性,此时溶液中的溶质是 。
28.DIS系统即数字化信息系统,它由传感器、数据采集器和计算机组成。某研究性学习小组用DIS系统测定食用白醋中醋酸的物质的量浓度,以溶液的导电能力来判断滴定终点。实验步骤如下:
(1)用 (填仪器名称)量取10.00mI。食用白醋,在 (填仪器名称)中用水稀
释后转移到100mL (填仪器名称)中定容,然后将稀释后的溶液倒入试剂瓶中。
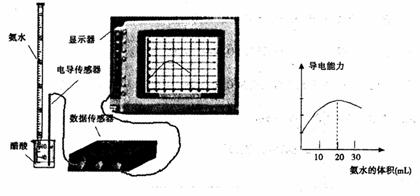
(2)量取20.00mL上述溶液倒入烧杯中,连接好DIS系统(见左下图),向烧杯中滴加浓度为0.1000mol/L.的氨水,计算机屏幕上显示出溶液导电能力随氨水体积变化的曲线(见右下图)。
①用水洗净的滴定管盛氨水前,还要进行的必要操作是 ,其目的是 。
②氨水与醋酸反应的离子方程式是 。
③食用白醋中醋酸的物质的量浓度是 。
④关于该实验的下列说法正确的是
A.不需使用酸碱指示剂
B.只需做一次实验即可,因为不会产生误差
C.只要显示器显示出了最高点后实验即可停止
27.1L0.2mol/L KOH溶液与1L0.1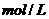
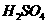 反应放出11.46 kJ的热量,请写出该反应的中和热的热化学方程式
。
反应放出11.46 kJ的热量,请写出该反应的中和热的热化学方程式
。
26.写出小苏打发生下列各变化的离子方程式
(1)电离: ;
(2)水解: ;
(3)与明矾溶液混合: ;
(4)与盐酸混合恰好反应 ;
所得溶液用惰性电极进行电解: 。
25.一种新型燃料电池,一极通入空气,另一极通入丁烷气体,电解质是掺杂氧化钇(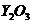 )的氧化锆(
)的氧化锆(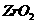 )晶体,在熔融状态下能传导
)晶体,在熔融状态下能传导 。下列对该燃料电池的说法正确的是
。下列对该燃料电池的说法正确的是
A.在熔融电解质中, 由负极移向正极
由负极移向正极
B.电池的总反应是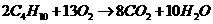
C.通入空气的一极是负极,电极反应为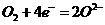
D.通入丁烷的一极是正极,电极反应为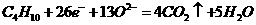
24.铅蓄电池放电时发生下列反应
负极: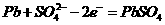
正极: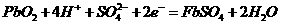
使用该电池电解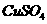 溶液。当有1.6g纯铜析出时,铅蓄电池内消耗硫酸的物质的量为
溶液。当有1.6g纯铜析出时,铅蓄电池内消耗硫酸的物质的量为
A.0.05 B.0.025mol
B.0.025mol
C.0.25 D.0.1mol
D.0.1mol
23.已知反应;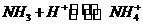 ②
②
③ ,反应生的容易程度①>②>③。下列事实或现象预测正确的是
,反应生的容易程度①>②>③。下列事实或现象预测正确的是
A.氯化银不溶于氨水
B.银氨溶液中加入少量氯化钠有白色沉淀
C.银氨溶液中加入盐酸有白色沉淀
D.银氨溶液可在酸性条件下稳定存在
22.下列各种说法中,都包含有前后两个数值,其中前者大于后者的是
A.在25℃和80℃时纯水中的c(H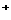 )
)
B.相同温度下,0.1mol/L醋酸和 醋酸中的c(OH
醋酸中的c(OH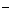 )
)
C.相同条件下,0.1 mol/L  0.1
0.1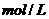
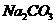 溶液的pH
溶液的pH
D.
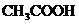 溶液中H
溶液中H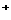 和
和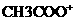 的个数
的个数
21.已知(1)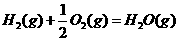
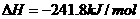
(2)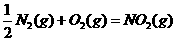
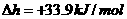
(3)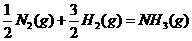
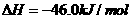
则1 mol 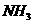
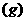 燃烧生成
燃烧生成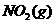 和
和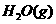 的反应热
的反应热 为
为
A.282.8kJ/mol B.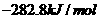
C.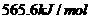 D.
D.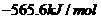
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com