
题目列表(包括答案和解析)
4、关于维生素的叙述中,不正确的是
A.维生素是参与生物发育和新陈代谢所必需的一类小分子
B.人体对维生素的需要量极小,但对人体的生长和健康至关重要
C.维生素在天然食品中含量丰富,所以加工后的食品维生素含量也高
D.习惯上把维生素分为脂溶性维生素和水溶性维生素
3、 垃圾处理无害化、减量化和资源化逐渐被人们所认识。垃圾的分类收集是实现上述理念的重要措施。某垃圾箱上贴有如右图所示的标志,向此垃圾箱中丢弃的垃圾是
垃圾处理无害化、减量化和资源化逐渐被人们所认识。垃圾的分类收集是实现上述理念的重要措施。某垃圾箱上贴有如右图所示的标志,向此垃圾箱中丢弃的垃圾是
A.危险垃圾 B.可回收物
C.有害垃圾 D.其他垃圾
2、 我国规定,所有销售的食品包装标签配料表上食品添加剂应使用规定的产品名称或种类名称,其中甜味剂、防腐剂、着色剂应注明。右图标签注明的添加剂中属于着色剂的是
我国规定,所有销售的食品包装标签配料表上食品添加剂应使用规定的产品名称或种类名称,其中甜味剂、防腐剂、着色剂应注明。右图标签注明的添加剂中属于着色剂的是
①柠檬酸 ②山梨酸钾 ③甜味素
④菠萝香精 ⑤柠檬黄 ⑥日落黄
A.①②⑤ B.②⑤⑥ C.⑤⑥ D.③④
1、下面是4位同学对“化学与健康”这一话题发表的见解中,正确的是








A B C D
31.(10分)25时,如果取0.1 mol·L-1HA溶液与0.1 mol·L-1NaOH溶液等体积混合(混合后溶液体积的变化不计),测得混合溶液的pH=8,试回答以下问题:
(1)混合溶液的pH=8的原因 (用离子方程式表示);
(2)混合溶液中由水电离出的c(H+)__ ___0.1 mol·L-1 NaOH溶液中由水电离出的c(H+);(填>、<、=)[
(3)求出混合液中下列算式的精确计算结果(填具体数字):
c (Na+)-c (A-)= mol·L-1;
(4)已知NH4A溶液为中性,又知将HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH 7 (填>、<、=);
(5)将相同温度下相同浓度的四种盐溶液:A.NH4HCO3 B.NH4A C.(NH4)2SO4 D.NH4Cl
按pH由大到小的顺序排列 (填序号)
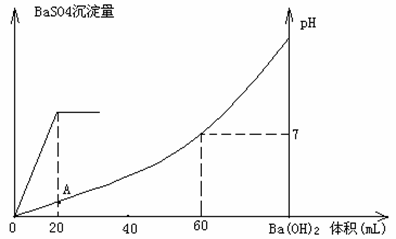
30.(12分).硫酸和盐酸混合溶液20mL,加入0.05mol/L的Ba(OH)2溶液时,生成BaSO4
沉淀量及溶液pH发生如下图所示的变化。
⑴开始时混合溶液中硫酸和盐酸的物质的量浓度各是多少?
⑵在A点溶液的pH是多少
29.(12分) 现有含FeCl2杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2固体,
首先将其制成水溶液,然后按下图所示步骤进行提纯:
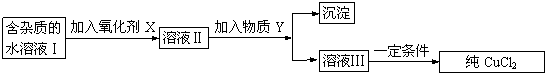
已知H2O2、KMnO4、NaClO、K2Cr2O7均具有强氧化性,要将溶液中的Cu2+、Fe2+、Fe3+沉淀为氢氧化物,需溶液的pH分别为6.4、6.4、3.7。
请回答下列问题:
(1)本实验最适合的氧化剂X是__________。
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4[
(2)加入氧化剂的目的是__________________________________________。
(3) 物质Y不可以是 ___________;
A.CuO B.CuCl2 C.Cu(OH)2 D.CuCO3
加入Y可以达到实验目的的理由是 .
(4)最后能不能直接蒸发结晶得到CuCl2? ______(填“能”或“不能”)。
如不能,应如何操作?(如能,此空不填)_________________________________________。
28、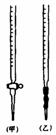 (10分) 乙二酸俗名草酸,某化学学习小组的同学欲探究测定草酸晶体(H2C2O4·xH2O)中x值。通过查阅资料该小组同学通过网络查询得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:2MnO4-+5H2C2O4+6H+
(10分) 乙二酸俗名草酸,某化学学习小组的同学欲探究测定草酸晶体(H2C2O4·xH2O)中x值。通过查阅资料该小组同学通过网络查询得,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:2MnO4-+5H2C2O4+6H+ 2Mn2++10CO2↑+8H2O
该组同学设计了滴定的方法测定x值。
① 称取1.260 g纯草酸晶体,将其酸制成100.00 mL水溶液为待测液。
② 取25.00 mL待测液放入锥形瓶中,再加入适量的稀H2SO4
③ 用浓度为0.1000 mol/L的KMnO4标准溶液进行滴定,达到终点时消耗10.00 mL;请回答:
⑴ 滴定时,将KMnO4标准液装在右图中的 (填“甲”或“乙”)滴定管中。[
⑵ 本实验滴定达到终点的标志可以是 。
⑶ 通过上述数据,计算出x= 。
讨论:①若滴定终点时俯视滴定管刻度,则由此测得的x值会 (填“偏大”、“偏小”或“不变”,下同)。
②若滴定时所用的KMnO4溶液因久置而导致浓度变小,则由此测得的x值会 。
27、(14分)
某二元酸(化学式用H2A表示)在水中的电离方程式是:H2A==H++HA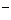 、
、
HA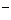
 H++A2-,回答下列问题:
H++A2-,回答下列问题:
(1)Na2A溶液呈 (填“酸性”、“中性”或“碱性”),理由是:
(用离子方程式说明)
NaHA溶液呈 (填“酸性”、“中性”或“碱性”),理由是:
。
(2)已知0.1mol/LNaHA溶液的pH=2,则0.1mol/L的H2A溶液中氢离子的物质的量浓
度 0.11mol/L(填“<”、“>”或“==”)理由是:
______ 。
(3)0.1mol/LNaHA溶液中各种离子浓度由大到小的顺序是: 。
26、(12分)
在25℃时,有pH为a的盐酸和pH为b的NaOH溶液,取Va L该盐酸,同该NaOH溶液完全中和,需Vb LNaOH溶液。填空:
(1)若a + b = 14,则Va∶Vb = (填数字)。
(2)若a + b = 13,则Va∶Vb = (填数字)。
(3)若a + b >15,则Va∶Vb = (填表达式),且Va Vb(填“>”、“<”或“=”)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com