
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
3ЁЂвбжЊC(ЪЏФЋ)ЁЂH2КЭCOЕФШМЩеШШЗжБ№ЮЊ393.5kJ/molЁЂ285.8kJ/molКЭ282.8kJ/molЁЃЯжгаH2КЭCOзщГЩЕФЛьКЯЦјЬх56.0L(БъзМзДПі)ЃЌОГфЗжШМЩеКѓЃЌЗХГізмШШСПЮЊ710.0kJЃЌВЂЩњГЩвКЬЌЫЎЁЃЯТСаШШЛЏбЇЗНГЬЪНЛђУшЪіжаЃЌе§ШЗЕФЪЧ(ЁЁЁЁ )
ЁЁ AЃЎ2CO(g) + O2(g) = 2CO2(g); ЁїH= +282.8kJ/mol
ЁЁ BЃЎ2H2(g) + O2(g) = 2H2O(g); ЁїH= -571.6kJ/mol
ЁЁ CЃЎC(ЪЏФЋ,s) + 1/2O2(g) = CO(g); ЁїH= -110.7kJ/mol
ЁЁ DЃЎШМЩеЧАЛьКЯЦјЬхжаЃЌH2ЕФЬхЛ§ЗжЪ§ЮЊ40%
2ЁЂЯТСаЙигкНКЬхЕФа№ЪіВЛе§ШЗЕФЪЧ(ЁЁЁЁ )
ЁЁ AЃЎВМРЪдЫЖЏЪЧНКЬхЮЂСЃЬигаЕФдЫЖЏЗНЪНЃЌПЩвдОнДЫАбНКЬхКЭШмвКЧјБ№ПЊРД
ЁЁ BЃЎЙтЯпЭИЙ§НКЬхЪБЃЌЛсЗЂЩњЖЁДяЖћаЇгІ
ЁЁ CЃЎгУЩјЮіЕФЗНЗЈОЛЛЏНКЬхЪБЃЌЪЙгУЕФАыЭИФЄжЛФмШУНЯаЁЕФЗжзгЁЂРызгЭЈЙ§
ЁЁ DЃЎНКЬхЮЂСЃФмЮќИНбєРызгЛђвѕРызгЃЌЙЪдкЕчГЁзїгУЯТЛсВњЩњЕчгОЯжЯѓ
1ЁЂ2007ФъХЕБДЖћЛЏбЇНБЪкгшЕТЙњПЦбЇМвИёЙўЕТЁЄАЃЬиЖћЁЃАЃЬиЖћдкБэУцЛЏбЇЗНУцЕФЙБЯзгажњгкШЫУЧРэНтЁАЬњЮЊЪВУДЛсЩњатЁБЁЂЁАШМСЯЕчГиКЭЦћГЕжаДІРэЮВЦјЕФДпЛЏМСШчКЮЙЄзїЁБЁЂЁАФЯМЋЩЯПеЕФГєбѕВуШчКЮБЛЦЦЛЕЁБЁЃЯТСагаЙиЫЕЗЈе§ШЗЕФЪЧЃК (ЁЁЁЁ )
AЃЎЮТЪваЇгІЕФМгОчЪЧЕМжТФЯМЋЩЯПеГєбѕПеЖДЕФжївЊдвђЁЁ
BЃЎЦћГЕЮВЦјДІРэЪЧдкИпЮТИпбЙДпЛЏМСЯТНјааЕФ
CЃЎЧтбѕШМСЯЕчГиЕФе§МЋЗДгІПЩБэЪОЮЊH2Ѓ2eЃ=2H+
DЃЎИжЬњдкПеЦјжаЕФИЏЪДжївЊЪЧЕчЛЏИЏЪД
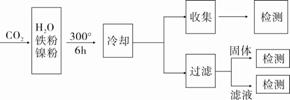
16ЁЂ(ЙВ18Зж)ЁАЮТЪваЇгІЁБЪЧШЋЧђЙизЂЕФЛЗОГЮЪЬтжЎвЛЁЃCO2ЪЧФПЧАДѓЦјжаКЌСПзюИпЕФвЛжжЮТЪвЦјЬхЃЌвђДЫЃЌПижЦКЭжЮРэCO2ЪЧНтОіЮТЪваЇгІЕФгааЇЭООЖЁЃ
(1)ЯТСаДыЪЉжаЃЌгаРћгкНЕЕЭДѓЦјжаCO2ХЈЖШЕФга--(ЬюзжФИ)
a.МѕЩйЛЏЪЏШМСЯЕФЪЙгУЁЁЁЁЁЁЁЁЁЁ b.жВЪїдьСжЃЌдіДѓжВБЛУцЛ§
c.ВЩгУНкФмММЪѕЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ d.РћгУЬЋбєФмЁЂЗчФм
(2)НЋCO2зЊЛЏГЩгаЛњЮяПЩгааЇЪЕЯжЬМбЛЗCO2зЊЛЏГЩгаЛњЮяЕФР§згКмЖрШчЃК
a.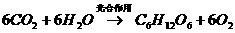
b.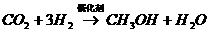
c.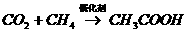
d. 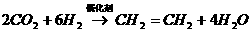
вдЩЯЗДгІжаЃЌзюНкФмЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌдзгРћгУТЪзюИпЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁ
(3)ЮФЯзБЈЕРФГПЮЬтзщРћгУCO2ДпЛЏМСЧтЛЏжЦМзЭщЕФбаОПЙ§ГЬШчЯТЃК
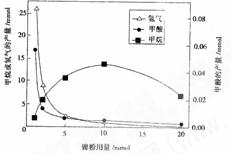 ЗДгІНсЪјКѓЃЌЦјЬхжаМьВтЕНCH4КЭH2ЃЌТЫвКжаМьВтЕНHCOOH(МзЫс)ЃЌЙЬЬхжаМьВтЕНФјЗлКЭFe3O4ЁЃCH4ЁЂHCOOHЁЂH2ЕФВњСПКЭФјЗлгУСПЕФЙиЯЕШчЭМЫљЪО(НіИФБфФјЗлгУСПЃЌЦфЫћЬѕМўВЛБф)ЃК
ЗДгІНсЪјКѓЃЌЦјЬхжаМьВтЕНCH4КЭH2ЃЌТЫвКжаМьВтЕНHCOOH(МзЫс)ЃЌЙЬЬхжаМьВтЕНФјЗлКЭFe3O4ЁЃCH4ЁЂHCOOHЁЂH2ЕФВњСПКЭФјЗлгУСПЕФЙиЯЕШчЭМЫљЪО(НіИФБфФјЗлгУСПЃЌЦфЫћЬѕМўВЛБф)ЃК
баОПШЫдБИљОнЪЕбщНсЙћЕУГіНсТлЃК
HCOOHЪЧCO2зЊЛЏЮЊCH4ЕФжаМфЬхМД 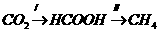
ЂйаДГіВњЩњH2ЕФЗДгІЗНГЬЪН
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЂкгЩЭМПЩжЊЃЌФјЗлЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ (ЬюзжФИ)
a.ЗДгІЂёЕФДпЛЏМСЁЁ b.ЗДгІЂђЕФДпЛЏМСЁЁ c.ЗДгІЂёЁЂЂђЕФДпЛЏМСЁЁ d.ВЛЪЧДпЛЏМС
ЂлЕБФјЗлгУСПДг1m molдіМгЕН10m molЃЌЗДгІ
ЫйТЪЕФБфЛЏЧщПіЪЧЁЁЁЁЁЁЁЁЁЁЁЁ (ЬюзжФИ)
a.ЗДгІЂёЕФЫйТЪдіМгЃЌЗДгІЂђЕФЫйТЪВЛБфЁЁ
b.ЗДгІЂёЕФЫйТЪВЛБфЃЌЗДгІЂђЕФЫйТЪдіМг
c.ЗДгІЂёЁЂЂђЕФЫйТЪОљВЛБф
d.ЗДгІЂёЁЂЂђЕФЫйТЪОљдіМгЃЌЧвЗДгІЂёЕФЫйТЪдіМгЕУПь
e.ЗДгІЂёЁЂЂђЕФЫйТЪОљдіМгЃЌЧвЗДгІЂђЕФЫйТЪдіМгЕУПь
15ЁЂ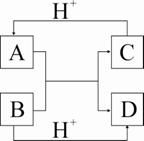 (ЙВ14Зж)вбжЊAЁЂBЁЂCЁЂDЪЧжабЇЛЏбЇжаГЃМћЕФЫФжжВЛЭЌСЃзгЃЌЫќУЧжЎМфДцдкШчЯТЫљЪОЕФЙиЯЕЃК
(ЙВ14Зж)вбжЊAЁЂBЁЂCЁЂDЪЧжабЇЛЏбЇжаГЃМћЕФЫФжжВЛЭЌСЃзгЃЌЫќУЧжЎМфДцдкШчЯТЫљЪОЕФЙиЯЕЃК
(1)ШчЙћAЁЂBЁЂCЁЂDОљЮЊ10ЕчзгЕФСЃзгЃЌ
ЧыаДГіЃКAЕФНсЙЙЪНЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛDЕФЕч
згЪНЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁ
(2)ШчЙћAКЭCЪЧ18ЕчзгЕФСЃзгЃЌBКЭ
DЪЧ10ЕчзгЕФСЃзгЃЌЧыаДГіAгыBдкШмвК
жаЗДгІЕФРызгЗНГЬЪНЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(3)вбжЊыТ(H2N-NH2)КЭМзАЗ(CH3-NH2)ЖМЪЧКЌга18ИіЕчзгЕФЗжзгЃЌЗжЮіыТКЭМзАЗЕФНсЙЙЬиЕуВЂДгжаЪмЕНЦєЗЂЃЌаДГігыЦфОпгаЯрЭЌЕчзгЪ§ЕФгаЛњЮяЕФНсЙЙМђЪН(аДСНИі)
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
14ЁЂ(ЙВ16Зж)гвЭМЪЧвЛЬзжЦШЁввЯЉВЂбщжЄввЯЉОпгаЛЙдадЕФЪЕбщзАжУЁЃ
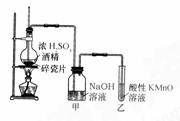 (1)ЪЕбщВНжшЃКЂйЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(1)ЪЕбщВНжшЃКЂйЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
ЂкдкИїзАжУжазЂШыЯргІЕФЪдМСЃЛЂлЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛЪЕбщЪБЃЌЩеЦПжавКЬхЛьКЯЮя
ж№НЅБфКкЁЃ
(2)аДГіДЫЪЕбщжЦШЁввЯЉЕФЛЏбЇЗНГЬЪН(зЂУїЗДгІЬѕМў)
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(3)ФмЙЛЫЕУїввЯЉОпгаЛЙдадЕФЯжЯѓЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛзАжУМзЕФзїгУЪЧЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃШєЮоДЫзАжУЃЌЪЧЗёвВФмМьбщввЯЉОпгаЛЙдадЃЌМђЪіЦфРэгЩЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
13ЁЂ(ЙВ12Зж)XЁЂYЁЂZЁЂWЮЊжабЇГЃМћЕФМИжжЕЅжЪЃЌЭЈГЃЧщПіЯТXЮЊвЛжжвзБЛДХЛЏЕФЃЌЙуЗКгУгкЙЄХЉвЕЩњВњЕФН№ЪєЃЌYЪЧвКЬхЕЅжЪЃЌZЪЧвЛжжЮоЩЋЦјЬхЃЌWЪЧвЛжжгаЩЋЦјЬхЁЃЛЏКЯЮяBЕФЫЎШмвКЮЊвЛдЊЧПЫс(ВЛКЌбѕдЊЫи)ЃЌИїЮяжЪЕФзЊЛЏЙиЯЕШчЯТЫљЪОЁЃ
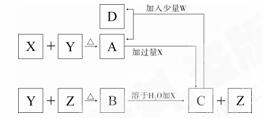
ЪдЛиД№ЃК
(1)XдЊЫидкжмЦкБэжаЕФЮЛжУЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃЛ
(2)YЕЅжЪЛЏбЇЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛZЕЅжЪЛЏбЇЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
(3)CШмвКгыЙ§СПWЕЅжЪЗДгІЕФРызгЗНГЬЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
(4)аТжЦWЫЎШмвКжаОпгаЧПбѕЛЏадЁЂЦЏАзадЕФЮяжЪЕФЛЏбЇЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
12ЁЂ120ЁцЪБ1ЬхЛ§ФГЬўКЭ4ЬхЛ§O2ЛьКЯЃЌЭъШЋШМЩеКѓЃЌЛжИДЕНдРДЕФЮТЖШКЭбЙЧПЃЌЬхЛ§ВЛБфЃЌИУЬўЗжзгжаЫљКЌЕФЬМдзгЪ§ВЛПЩФмЪЧ
AЁЂ1ЁЁЁЁЁЁЁЁЁЁ BЁЂ2ЁЁЁЁЁЁЁЁЁЁ CЁЂ3ЁЁЁЁЁЁЁЁЁЁ DЁЂ4
11ЁЂ24molХЈЖШЮЊ0.05molЁЄL-1ЕФNa2SO3ШмвКЧЁКУгы20mlХЈЖШЮЊ0.02molЁЄL-1ЕФK2Cr2O7ШмвКЭъШЋЗДгІЃЌдђдЊЫиCrдкЛЙдВњЮяжаЕФЛЏКЯМлЪЧ
AЁЂ+6ЁЁЁЁЁЁЁЁЁЁ BЁЂ+3ЁЁЁЁЁЁЁЁЁЁ CЁЂ+2ЁЁЁЁЁЁЁЁЁЁ DЁЂ0
10ЁЂИжЬњдкГБЪЊЕФПеЦјжаЛсБЛИЏЪДЃЌЗЂЩњЕФдЕчГиЗДгІЮЊ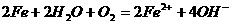 вдЯТЫЕЗЈе§ШЗЕФЪЧ
вдЯТЫЕЗЈе§ШЗЕФЪЧ
AЁЂИКМЋЗЂЩњЕФЗДгІЮЊ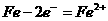
BЁЂе§МЋЗЂЩњЕФЗДгІЮЊ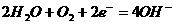
CЁЂдЕчГиЪЧНЋЕчФмзЊЛЏЮЊЛЏбЇФмЕФзАжУ
DЁЂИжжљдкЫЎЯТВПЗжБШдкПеЦјгыЫЎНЛНчДІИќШнвзБЛИЏЪД
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com