
ĢāÄæĮŠ±ķ(°üĄØ“š°øŗĶ½āĪö)
2£®ĻĀĮŠ¹ŲÓŚ·“Ó¦ĻŽ¶ČµÄŠšŹö²»ÕżČ·µÄŹĒ
A£®·“Ó¦ĻŽ¶ČŹĒŅ»ÖÖĘ½ŗāדĢ¬£¬“ĖŹ±·“Ó¦ŅŃ¾Ķ£Ö¹
B£®“ļµ½Ę½ŗāדĢ¬Ź±£¬Õż·“Ó¦ĖŁĀŹŗĶÄę·“Ó¦ĖŁĀŹĻąµČ
C£®“ļµ½Ę½ŗāדĢ¬Ź±£¬·“Ó¦ĪļŗĶÉś³ÉĪļÅØ¶Č¶¼²»ŌŁøıä
D£®²»ÉŁ·“Ó¦¶¼¾ß ÓŠæÉÄęŠŌ£¬Ö»ŹĒÓŠµÄ³Ģ¶ČŠ”£¬ÓŠµÄ³Ģ¶Č“ó
ÓŠæÉÄęŠŌ£¬Ö»ŹĒÓŠµÄ³Ģ¶ČŠ”£¬ÓŠµÄ³Ģ¶Č“ó
1£®·Ø¹śæĘѧ¼ŅĄļ°ŗ×ī½ü·¢ĻÖŅ»ÖÖÖ»ÓÉĖÄøöÖŠ×Ó¹¹³ÉµÄĮ£×Ó£¬ÕāÖÖĮ£×Ó³ĘĪŖ”°ĖÄÖŠ×Ó”±£¬Ņ²
ÓŠČĖ³ĘÖ®ĪŖ”°ĮćŗÅŌŖĖŲ”±”£ĻĀĮŠÓŠ¹Ų”°ĖÄÖŠ×Ó”±µÄĖµ·Ø²»ÕżČ·µÄŹĒ
A£®øĆĮ£×Ó²»ĻŌµēŠŌ”””””””””””””””””””””””””””””” B£®øĆĮ£×ÓµÄÖŹĮæŹżĪŖ4
C£®øĆŌŖĖŲŌŚŌŖĖŲÖÜĘŚ±ķÖŠÓėĒāŌŖĖŲÕ¼Ķ¬Ņ»Ī»ÖĆ”””””” D£®øĆĮ£×ÓµÄÖŹĮæ±ČĒāŌ×Ó“ó
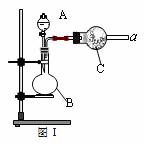
28£®(17·Ö)Ķ¼¢ńŹĒ»ÆѧŹµŃéŹŅÖŠ³£ÓĆÖʱø”¢øÉŌļĘųĢåµÄ²æ·ÖŅĒĘ÷×°ÖĆ”£Ä³Ń§Š£Ķ¬Ń§ĄūÓĆ֊ѧ³£ÓĆŹŌ¼Į¼°ŅĒĘ÷Éč¼ĘĻĀĮŠŹµŃ锣

 ””””
””””
(1)Ķ¼¢ńÖŠŅĒĘ÷BµÄĆū³Ę£ŗ_______________________”£
(2)¢ŁĶ¬Ń§¼×ĄūÓĆĶ¼¢ń×°ÖĆÖʱø²¢ŹÕ¼ÆøÉŌļµÄNO2ĘųĢ壬ĒėŌŚ·½æņÄŚ»³öÓĆ¼ÆĘųĘæŹÕ¼ÆNO2µÄ×°ÖĆĶ¼(ŗ¬Ī²Ęų“¦Ąķ×°ÖĆ)”£¢ŚBÖŠ·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ________________”£
(3)Ķ¬Ń§ŅŅĄūÓĆĶ¼¢ń×°ÖĆĶعż³ĘĮæ·“Ó¦Ē°ŗóCµÄÖŹĮæ£¬Č·¶ØNa2CO3ŗĶNaCl¹ĢĢå»ģŗĻĪļÖŠNa2CO3µÄÖŹĮ攣AÖŠ¼ÓČėĻ”ĮņĖį£¬BÖŠ¼ÓČėNa2CO3ŗĶNaCl¹ĢĢå»ģŗĻĪļ£¬CÖŠ¼ÓČė¼īŹÆ»Ņ”£øĆ×°ÖĆ“ęŌŚ½Ļ¶ąČ±ĻŻ£¬“Ó¶ųµ¼ÖĀŹµŃéĪó²ī½Ļ“ó£¬ĒėÄćĖµ³öĘäÖŠµÄĮ½µćȱĻŻ£ŗ
¢Ł______________________________________________________________________£»
¢Ś______________________________________________________________________”£
(4)Ķ¬Ń§±ūĄūÓĆĶ¼¢ń×°ÖĆÖĘČ”°±ĘųŗĶŃõĘųµÄ»ģŗĻĘųĢ壬²¢ĒŅĄūÓĆĶ¼¢ņ×°ÖĆŃéÖ¤°±µÄijŠ©ŠŌÖŹ”£AÖŠ¼ÓČėÅØ°±Ė®£¬CÖŠ¼ÓČė¼īŹÆ»Ņ£¬EÄŚ·ÅÖĆ“ß»Æ¼Į(²¬ŹÆĆŽ)£¬°“ĘųĮ÷·½Ļņa”śb”śc”śhĮ¬½Óø÷ŅĒĘ÷”£
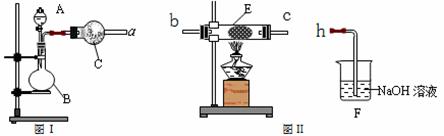
¢ŁBÄŚŠč¼ÓČė¹ĢĢåŹŌ¼ĮµÄĆū³ĘĪŖ____________________£¬BÖŠÄܲśÉś°±ĘųŗĶŃõĘų»ģŗĻĘųĢåµÄŌŅņŹĒ_______________________________________________________________”£
¢ŚŹµŃéÖŠ¹Ū²ģµ½EÄŚÓŠŗģ×ŲÉ«ĘųĢå³öĻÖ£¬Ö¤Ć÷°±Ęų¾ßÓŠ_________ŠŌ£¬EÖŠ·¢Éś·“Ó¦µÄĮ½øö»Æѧ·½³ĢŹ½ĪŖ£ŗ____________________________ŗĶ2NO + O2 £½£½ 2NO2”£
27£®( 12·Ö) A”¢B”¢C”¢DĖÄÖÖŌŖĖŲŌ×ÓŗĖµēŗÉŹżŅĄ“ĪŌö“ó(¾łŠ”ÓŚ20)£¬Ę䵄֏¼°ĻąÓ¦µÄ»ÆŗĻĪļÄÜ·¢ÉśČēĻĀ·“Ó¦¹ŲĻµ£ŗ
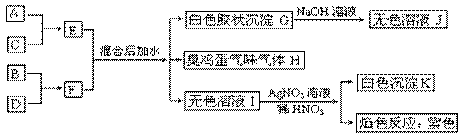
(1)Š“³öĖÄÖÖŌŖĖŲŌŖĖŲ·ūŗÅ£ŗA”¢____B”¢____C”¢____D”¢____”£
(2) FµÄµē×ÓŹ½£ŗ_________________”£
(3)Š“³öE”¢F»ģŗĻŗó¼ÓĖ®µÄĄė×Ó·½³ĢŹ½£ŗ_________________________________”£
(4)Š“³öG”śJµÄĄė×Ó·½³ĢŹ½£ŗ_________________________________”£
(5)Š“³öCµ„ÖŹÓėHĖ®ČÜŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ_____________________________”£
26£®(14·Ö)ŌĖÓĆ»Æѧ·“Ó¦ŌĄķŃŠ¾æµŖ”¢ŃõµČµ„ÖŹ¼°Ęä»ÆŗĻĪļµÄ·“Ó¦ÓŠÖŲŅŖŅāŅ唣
(1)ŗĻ³É°±·“Ó¦N2 (g)+3H2(g) 2NH3(g)£¬ČōŌŚŗćĪĀ”¢ŗćŃ¹Ģõ¼žĻĀĻņĘ½ŗāĢåĻµÖŠĶØČėė²Ęų£¬ŌņĘ½ŗā””””””””””
ŅʶÆ(Ģī”°Ļņ×ó”±”°ĻņÓŅ”±»ņ”°²»”±)£»Ź¹ÓĆ“ß»Æ¼Į£¬ÉĻŹö·“Ó¦µÄ”÷H________(Ģī”°Ōö“ó”±
”°¼õŠ””±
»ņ”°²»øı䔱)”£
2NH3(g)£¬ČōŌŚŗćĪĀ”¢ŗćŃ¹Ģõ¼žĻĀĻņĘ½ŗāĢåĻµÖŠĶØČėė²Ęų£¬ŌņĘ½ŗā””””””””””
ŅʶÆ(Ģī”°Ļņ×ó”±”°ĻņÓŅ”±»ņ”°²»”±)£»Ź¹ÓĆ“ß»Æ¼Į£¬ÉĻŹö·“Ó¦µÄ”÷H________(Ģī”°Ōö“ó”±
”°¼õŠ””±
»ņ”°²»øı䔱)”£
(2)Ņ»Ńõ»ÆĢ¼ŌŚøßĪĀĻĀÓėĖ®ÕōĘų·“Ó¦µÄ·½³ĢŹ½ĪŖ£ŗCO+H2O£½CO2+H2”£ŅŃÖŖ²æ·ÖĪļÖŹČ¼ÉÕµÄČČ»Æѧ·½³ĢŹ½ČēĻĀ£ŗ 2H2 (g) + O2(g) £½ 2H2O(l);”÷H=£571.6kJ”¤mol£1
”””””””””””” ”””””””””””””””””” 2CO (g) + O2(g) £½ 2CO2”” (g) ;”÷H=£566kJ”¤mol£1
”””””””””””””””””” ÓÖÖŖ1molH2O(g)×Ŗ±äĪŖ1mol H2O(l)Ź±·Å³ö44.0kJČČĮ攣Š“³öCOŗĶĖ®ÕōĘųŌŚøßĪĀ“߻ƼĮĻĀ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½”””””””””””””””””””””””””””””””””””””””””””” ”£
(3)ŌŚ25”ęĻĀ£¬ĻņÅضČĪŖ0.1 mol”¤L-1µÄAlCl3ČÜŅŗÖŠÖšµĪ¼ÓČė°±Ė®£¬Éś³ÉøĆ³ĮµķµÄĄė×Ó·½³ĢŹ½ĪŖ______________________________”£
(4)ÓŠČĖÉčĻėŃ°ĒóŗĻŹŹµÄ“߻ƼĮŗĶµē¼«²ÄĮĻ£¬ŅŌN2”¢H2ĪŖµē¼«·“Ó¦Īļ£¬ŅŌHCl-NH4ClĪŖµē½āÖŹČÜŅŗÖĘŌģŠĀŠĶČ¼ÉÕµē³Ų,·Åµē¹ż³ĢÖŠ£¬ČÜŅŗÖŠļ§øłĄė×ÓÅضČÖš½„Ōö“ó”£ĒėŠ“³öøƵē³ŲµÄÕż¼«·“Ó¦Ź½”””””””””””””””””””””””””” ”£
(5)ijĪĀ¶Č(t”ę)Ź±£¬²āµĆ0.01mol”¤L£1µÄNaOHČÜŅŗµÄpH£½11”£ŌŚ“ĖĪĀ¶ČĻĀ£¬½«pH£½1µÄH2SO4ČÜŅŗVaLÓėpH£½11µÄNaOHČÜŅŗVbL»ģŗĻ£¬ČōĖłµĆ»ģŗĻŅŗĪŖÖŠŠŌ£¬Ōņ
Va©UVb£½”””””””””””” ”””” ”£
(6)ŌŚ25”ęĻĀ£¬½«a mol”¤L-1µÄ°±Ė® Óė0.01 mol”¤L-1µÄŃĪĖįµČĢå»ż»ģŗĻ£¬·“Ó¦Ę½ŗāŹ±ČÜŅŗÖŠc(NH4+)=c(Cl-)”£ŌņČÜŅŗĻŌ_____________ŠŌ(Ģī”°Ėį”±”°¼ī”±»ņ”°ÖŠ”±)£»
Óė0.01 mol”¤L-1µÄŃĪĖįµČĢå»ż»ģŗĻ£¬·“Ó¦Ę½ŗāŹ±ČÜŅŗÖŠc(NH4+)=c(Cl-)”£ŌņČÜŅŗĻŌ_____________ŠŌ(Ģī”°Ėį”±”°¼ī”±»ņ”°ÖŠ”±)£»
25£®Ņ»¶ØĢõ¼žĻĀ£¬Ä³ĆܱÕČŻĘ÷ÖŠ³äČėµČĪļÖŹµÄĮæµÄA”¢BĮ½ÖÖĘųĢ壬·¢Éś·“Ó¦£ŗ
A(g) + B(g)  ””2C(g)”£“ļµ½Ę½ŗāŗó£¬Ö»øı䷓ӦµÄŅ»øöĢõ¼ž£¬²āµĆČŻĘ÷ÖŠø÷ĪļÖŹµÄÅØ¶Č”¢·“Ó¦ĖŁĀŹĖꏱ¼ä±ä»ÆČēĻĀĮ½Ķ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ(”””” )
””2C(g)”£“ļµ½Ę½ŗāŗó£¬Ö»øı䷓ӦµÄŅ»øöĢõ¼ž£¬²āµĆČŻĘ÷ÖŠø÷ĪļÖŹµÄÅØ¶Č”¢·“Ó¦ĖŁĀŹĖꏱ¼ä±ä»ÆČēĻĀĮ½Ķ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ(”””” )
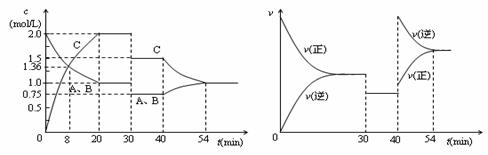
A£®30minŹ±¼õŠ”ČŻ»ż”””””” ””””””””””””””””””””””””
B£®40minŹ±¼ÓČė“߻ƼĮ
C£®0-8minÄŚAµÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ0.17 mol/(L”¤min) -1””
D£®Õż·“Ó¦ĪŖ·ÅČČ·“Ó¦
µŚ¢ņ¾ķ(60·Ö)
24£®ŠĀŠĶ NaBH4/H2O2Č¼ĮĻµē³Ų(DBFC)µÄ½į¹¹ČēÓŅĶ¼£¬(ŅŃÖŖÅšĒā»ÆÄĘÖŠ
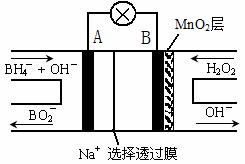 ĒāĪŖ£1¼Ū)£¬ÓŠ¹ŲøƵē³ŲµÄĖµ·ØÕżČ·µÄŹĒ(”””” )
ĒāĪŖ£1¼Ū)£¬ÓŠ¹ŲøƵē³ŲµÄĖµ·ØÕżČ·µÄŹĒ(”””” )
A£®µē¼«B²ÄĮĻÖŠŗ¬MnO2²ć£¬MnO2æÉŌöĒæµ¼µēŠŌ
B£®µē³Ųøŗ¼«ĒųµÄµē¼«·“Ó¦ĪŖ£ŗ
”” ”” ””””BH4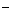 + 8OH
+ 8OH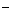 -8e
-8e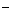 = BO
= BO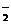 + 6H2O
+ 6H2O
C£®·Åµē¹ż³ĢÖŠ£¬Na+“ÓÕż¼«ĒųĻņøŗ¼«ĒųĒØŅĘ
D£®ŌŚµē³Ų·“Ó¦ÖŠ£¬ĆæĻūŗÄ1L 6 mol/LH2O2ČÜŅŗ£¬
ĄķĀŪÉĻĮ÷¹żµēĀ·ÖŠµÄµē×ÓĪŖ6NAøö
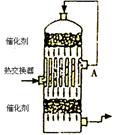
23£®ŌŚĮņĖį¹¤ŅµÉś²śÖŠ£¬ĪŖĮĖÓŠĄūÓŚSO2µÄ×Ŗ»Æ£¬ ĒŅÄܳä·ÖĄūÓĆČČÄÜ£¬²ÉÓĆĮĖÖŠ¼äÓŠČČ½»»»Ę÷½Ó“„ŹŅ(¼ūÓŅĶ¼)”£°““ĖĆܱÕĢåĻµÖŠĘųĢåµÄ Į÷Ļņ£¬ŌņŌŚA“¦Į÷³öµÄĘųĢåĪŖ”””” (”””” )””””””””””””””””””””””””””””””””””
”””””” A£®SO2”””””””””””””””””””” B£®SO3”¢O2””””””””””””””””””””””””””
”””””” C£®SO2”¢”¢SO3”””””””””””””””””””” D£®SO2”¢O2””””””””””
22£®ÓŠ100mL3.5mol/LNaOHČÜŅŗŗĶ100mL1mol/LµÄAlCl3ČÜŅŗ, °“ÕÕČēĻĀĮ½ÖÖ·½·Ø½ųŠŠŹµ
Ńé£ŗ¢Ł ½«ĒāŃõ»ÆÄĘČÜŅŗÖšµĪ¼Óµ½ĀČ»ÆĀĮČÜŅŗÖŠ£»¢Ś ½«ĀČ»ÆĀĮČÜŅŗÖšµĪ¼Óµ½ĒāŃõ»ÆÄĘ
ČÜŅŗÖŠ”£ ±Č½ĻĮ½“ĪŹµŃéµÄ½į¹ūŹĒ (”””” )
A£®ĻÖĻó²»Ķ¬, ³ĮµķĮæĻąµČ”””””””””” ””””””B£®ĻÖĻó²»Ķ¬, ³ĮµķĮæ²»Ķ¬
 C£®ĻÖĻóĻąĶ¬, ³ĮµķĮæ²»Ķ¬””””””””””””””
D£®ĻÖĻóĻąĶ¬,
³ĮµķĮæĻąĶ¬
C£®ĻÖĻóĻąĶ¬, ³ĮµķĮæ²»Ķ¬””””””””””””””
D£®ĻÖĻóĻąĶ¬,
³ĮµķĮæĻąĶ¬
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com