
题目列表(包括答案和解析)
22.(6分)实验室用高锰酸钾和浓盐酸反应制取氯气:K^S*5U.C#O
KMnO4+ HCl - Cl2↑+ MnCl2+ KCl+ H2O
(1)配平上述的反应方程式,并标出电子转移的方向和数目(用双线桥)
(2)其中还原剂是_______。若消耗0.1 mol氧化剂,则被氧化的还原剂的物质的量是____mol。
21.(4分)(1)3.4克NH3含质子的物质的量为 ,该气体在标准状况下的体积是 。
(2)已知500mL
Al2(SO4)3溶 液
液 中含有Al3+为0.5mol,则Al2(SO4)3溶液的物质的量浓度为 mol/L,取上述溶液50mL加水到150mL,此溶液中SO42-的物质的量浓度为 mol/L。
中含有Al3+为0.5mol,则Al2(SO4)3溶液的物质的量浓度为 mol/L,取上述溶液50mL加水到150mL,此溶液中SO42-的物质的量浓度为 mol/L。
20.某无色溶液中只可能含有Na+ 、Ba2 +、 Cl一、 Br一、SO32一、SO42一,对该溶液进行下列实验,实验操作和现象如下表:
|
步骤 |
操 作 |
现 象 |
|
(1) |
取少量溶液滴加几滴石蕊试液 |
溶液变蓝 |
|
(2) |
另取少量溶液滴加过量氯水,再加入CCl4振荡,静置 |
上层无色,下层呈橙红色 |
|
(3) |
取(2)上层溶液,加入过量Ba(NO3)2溶液和稀HNO3, 过滤 过滤 |
有白色沉淀产生 |
|
(4) |
向(3)的滤液中加入过量AgNO3溶液和稀HNO3 |
有白色沉淀产生 |
下列结论正确的是( )
A.可能含有 Cl一、 SO32一、SO42一 B.肯定没有 Ba2 +、Cl一、Br一
C.不能确定 Na+ 、 SO32一、SO42一 D.肯定含有 Na+、 Br一、SO32一
第Ⅱ卷(非选择题,共40分)
19.配制100 mL 1 mol·L-1氢氧化钠溶液,下列操作错误的是( )
A.在托盘天平上放两片大小、质量一样的纸,然后将氢氧化钠放在纸片上进行称量
B.把称得的氢氧化钠放入盛有适量蒸馏水的烧杯中,溶解、冷却,再把溶液移入容量瓶中
C.用蒸馏水洗涤烧杯、玻璃棒2-3次,洗涤液也移入容量瓶中
D.沿着玻璃棒往容量瓶中加入蒸馏水, 到离刻度线1-2cm时改用胶头滴管滴加,直到溶液凹面恰好与刻度相切
到离刻度线1-2cm时改用胶头滴管滴加,直到溶液凹面恰好与刻度相切
18.同温同压下,等体积的两容器内分别充满由14N、13C、18O三种原子构成的一氧化氮和一氧化碳气体。下列对两容器中气体的说法正确的是( )
A.所含分子数和质量均不相同 B.含有相同数目的分子和电子
C.含有相同数目的中子、原子和分子 D.含有相同数目的质子和中子
17.1L 1mol/L
NaOH溶液吸收0.8moL CO2 所得溶液中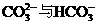 的物质的量浓度之比为( )
的物质的量浓度之比为( )
A.1∶3 B.2∶1 C.2∶3 D.3∶2
16.下表中评价合理的是( )
|
选项 |
化学反应及其离子方程式 |
评价 |
|
A |
Fe3O4与稀硝酸反应: 2 Fe3O4 +18 H+=6 Fe3+ + H2↑+8 H2O |
正确 |
|
B |
向碳酸镁中滴加稀盐酸: CO32-+2H+=CO2↑+H2O |
错误,碳酸镁不应写成离子形式 |
|
C |
向硫酸铵溶液中加入氢氧化钡溶液: SO42-+ Ba2+== BaSO4↓ |
正确 |
|
D |
FeBr2溶液与等物质的量的Cl2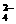 反应: 反应:2Fe2++2Br-+2Cl2=2Fe3++4Cl- + B   r2 r2 |
错误,Fe2+与Br-的化学计量数之比为1:2 |
15.下列是某兴趣小组根据课本实验设计的一个能说明Na2CO3与NaHCO3热稳定性的套管实验。请观察下图的实验装置、分析实验原理,下列说法错误的是( )
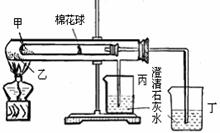 A.甲为小苏打,乙为纯碱
A.甲为小苏打,乙为纯碱
B.要证明NaHCO3受热能产生水,可在小试管内塞上沾有无水硫酸铜粉末的棉花球
C.整个实验过程中可以看到丙烧杯的澄清石灰水没变浑浊
D.同质量的甲和乙完全反应消耗的同浓度的盐酸体积:甲>乙
14.向含有Na+、Mg2+、Fe2+和Al3+的溶液中加入足量Na2O2微热并搅拌后,再加入过量稀盐酸,溶液中大量减少的离子是( )
A.Na+ B.Fe2+ C.Mg2+ D.Al3
13.用NA表示阿伏加德罗常数的值。下列叙述正确的是( )
A.由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA
B.1 mol FeCl3完全水解转化为氢氧化铁胶体后能生成NA个胶粒
C.1 mol H2O2在MnO2作催化剂的条件下完全分解生成O2,转移电子数为2NA
D.1 mol Na2O2中含有的阴离子数目为2NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com