
题目列表(包括答案和解析)
7.将80 mL盐酸与120 mLNaOH溶液混合,所得溶液pH=12,若混合前盐酸与NaOH溶液的物质的量浓度相等,则混合前它们的浓度是(忽略混合时溶液体积的变化)
A.0.1 mol/L B.0.05 mol/L
C.0.5 mol/L D. 1 mol/L
6.下列实验能达到实验目的且符合安全要求的是
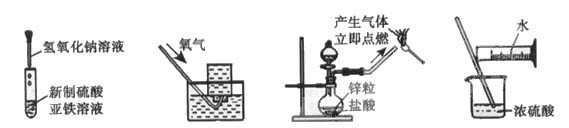
5.在pH为4-5的环境中,Cu2+、Fe2+不会沉淀,而Fe3+几乎完全沉淀。工业上制CuCl2是将浓盐酸加热到80℃左右,再慢慢加入粗氧化铜(含有杂质FeO),并充分搅拌使之溶解。欲除去溶液中的杂质离子,下述方法正确的是
A.加入纯Cu将Fe2+还原
B.向溶液中加入Na2S使Fe2+沉淀
C.直接加热使杂质离子水解除去
D.在溶液中通入Cl2,再加入CuO粉末调节pH为4-5
4.以下反应均与几种常见的金属元素有关,其离子方程式不正确的是
A.FeCl3溶液与H2S溶液反应:2Fe3++H2S=2Fe2++S↓+2H+
B.AlCl3溶液与NaAlO2溶液反应:Al3++3 AlO2-+6H2O=4 Al(OH)3↓
C.Fe(OH)2与HNO3溶液反应:Fe(OH)2+2H+= Fe 2++2H2O
D.Zn与CuSO4溶液反应:Zn+Cu2+=Zn2++Cu
3. “互滴法”是一种鉴别物质的方法,它依据的是试剂的滴加顺序不同对应的现象不同。下列几组无色溶液不能用互滴法鉴别的是
A.Na2CO3溶液与稀盐酸 B. AlCl3溶液与NaOH溶液
C. NaHCO3溶液与稀盐酸 D. NaAlO2溶液与稀硫酸
2.下列说法正确的是 ://
A.金属单质在化学反应中既能被氧化,又能被还原
B.除去铝锅表面油污的适宜方法是用钢丝球摩擦清洗
C.Fe3O4常温下是一种黑色固体,俗称磁性氧化铁
D.可以用镁与稀硝酸反应来制取氢气
1.世界气候变化峰会于2009年12月19日在丹麦首都哥本哈根闭幕。下列措施有利于改善全球气候条件及环境质量的是
①发展核电,以减少火力发电带来的二氧化碳排放问题
②积极推行“限塑令”,加快研发利用二氧化碳合成的可降解塑料
③加速建设地铁轻轨等轨道交通,减少汽车尾气排放
④发展低碳经济、循环经济,推广可利用太阳能、风能的城市照明系统
⑤使用生物酶降解生活废水中的有机物,使用填埋法处理未经分类的生活垃圾
A.①②③④ B.①②⑤ C.①②④⑤ D.③④⑤
26. 向由Cu、Cu2O和CuO组成的混合物中,加入10mL6mol·L-1的稀硝酸溶液,恰好使混合物完全溶解,同时收集到标准状况下NO 224 mL。请回答以下问题:
(1)写出Cu20与稀硝酸反应的化学方程式 (不必配平)。
(2)产物中硝酸铜的物质的量为
(3)若原混合物中有0.01molCu,则其中Cu2O的物质的量为
CuO的物质的量为
25. 某课外活动小组利用以下装置探究氯气与氨气之间的反应。其中A 、F 分别为氨气和氯气的发生装置,C为纯净的氯气于氨气反应的装置。
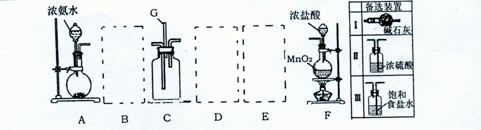
请回答下列问题:
(1)装置F中发生反应的离子方程式 。
(2)装置A中烧瓶内固体可以选用 (选填以下选项的代号)。
A.碱石灰 B.生石灰 C.二氧化硅D.五氧化二磷 E.烧碱F.氢氧化钠和氯化铵的混合物
(3)上图A-F是按正确实验装置顺序排列的。虚线框内应添加必要的除杂装置,
请从上图的备选装置中选择,并将编号填人下列空格:B
D ,E
(4)氯气和氨气在常温下混合就会反应生成氯化铵和氮气,写出反应的化学方程式 。
装置C内出现浓厚的白烟并在容器内壁凝结,请设计一个实验方案检验其中的NH4+
(5)若从装置C的G处逸出的尾气只含有N2和少量Cl2,应如何处理才能不污染环境?
24. (1)空气质量越来越受到人们的关注,下列是某省部分城市空气质量周报:
|
城市 |
污染指数 |
首要污染物 |
空气质量等级 |
|
甲 |
98 |
SO2 |
Ⅱ |
|
乙 |
47 |
|
Ⅰ |
|
丙 |
103 |
TSP |
Ⅲ |
|
丁 |
90 |
NOX |
Ⅱ |
注:TSP--总悬浮颗粒物;NOx--氮氧化物.
①由上表可知,最容易出现酸雨的城市是________.
②悬浮颗粒物不易沉降,它与空气中的SO2、O2接触时,SO2会部分转化为SO3,悬浮颗粒物所起的作用是________.(填序号)
A.氧化剂 B.还原剂 C.催化剂 D.吸附剂
③氮的氧化物也是大气污当物之一.目前,治理NO的方法是在一定条件下用氨把一氧化氮还原为氮气和水.科学家又设想,在相同条件下可采用价格比NH3更便宜的天然气来处理NO,可得到同样效果,写出该反应的化学方程式________ _.
(2)某中等城市每年燃煤约300万吨,其含硫量按1.00%计算,若硫全部转化为SO2,SO2有60.0%转化为硫酸,相当于生成________________吨98.0%的硫酸?(列式计算)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com