
题目列表(包括答案和解析)
21.(8分)水是自然界中普遍存在的一种物质,根据下列信息回答问题:
 (1)
(1) 氧原子基态时价层电子的电子排布图为_______ _________。
氧原子基态时价层电子的电子排布图为_______ _________。
(2)已知2H2O = H3O+ + OH-,H3O+的立体构型是___________________,中心原子的杂化类型是__________________。
(3)s轨道与s轨道重叠形成的共价键可用符号表示为:δs-s,p轨道与p轨道以“头碰头”方式重叠形成的共价键可用符号δp-p,则H2O分子含有的共价键用符号表示为_________。
(4)试比较同主族元素的氢化物H2O、H2S和H2Se的稳定性和沸点高低,并说明理由。
稳定性: 理由: 。
沸点: 理由: 。
20.(8分)用酸式滴定管准确移取25.00mL某未知浓度的盐酸溶液于一洁净的锥形瓶中,然后用0.2000mol·L -1的氢氧化钠溶液(指示剂为酚酞)滴定得结果如下:
|
|
NaOH起始读数 |
NaOH终点读数 |
|
第一次 |
0.40mL |
18.50mL |
|
第二次 |
1.30mL |
18.05mL |
|
第三次 |
3.10mL |
21.20mL |
(1)达到滴定终点的时溶液颜色的变化为 色到 色;
(2)根据以上数据可以计算出盐酸的物质的量浓度为 ;
(3)以下操作造成测定结果偏高的原因可能是 。
A、 滴定终点读数时,俯视滴定管的刻度,其它操作均正确
B、 盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
C、 滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
D、 未用标准液润洗碱式滴定管
19.(12分)请将氧化还原反应:2Fe3++2I- 2Fe2++I2设计成带盐桥原电池。
2Fe2++I2设计成带盐桥原电池。
试剂:FeCl3溶液,KI溶液;其它用品任选。请回答下列问题。
(1)请画出设计的原电池装置图,并标出电极材料,电极名称及电解质溶液。

(2)发生还原反应的电极为电池的 极,其电极反应式为 。
(3)反应达到平衡时,外电路导线中 (填“有”或“无”)电流通过。
(4)平衡后向FeCl3溶液中加入少量FeCl2固体,当固体全部溶解后,则此时该溶液中电极变为 (填“正”或“负”)极。
(5)请设计简单实验,证明溶液中同时存在Fe3+ 、Fe2+ 。
18.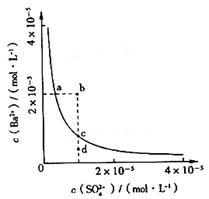 某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是( )
某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。下列说法正确的是( )
A.加入Na2SO4可以使溶液由a点变到b点
B.通过蒸发可以使溶液由d点变到c点
C.d点无BaSO4沉淀生成
D.a点对应的Ksp大于c点对应的Ksp
第Ⅱ卷(非选择题 共54分)
17.用质量均为100 g的铜作电极,电解硝酸银溶液,电解一段时间后,两电极的质量差为28 g,此时两电极的质量分别为( )
A.阳极100 g,阴极128 g B.阳极93.6 g,阴极121.6 g
C.阳极91.0 g,阴极119.0 g D.阳极86.0 g,阴极114.0 g
16.将0.2 mol·L-1 HCN溶液和0.1 mol·L-1的NaOH溶液等体积混合后,溶液显碱性,下列关系中正确的是( )
A.c(HCN)<c(CN-) B.c(Na+)>c(CN-)
C.c(HCN)- c(CN-)=c(OH-) D.c(HCN)+ c(CN-)=0.1 mol·L-1
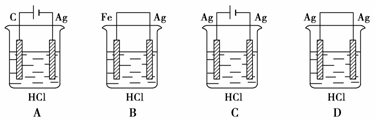
15.某学生欲完成反应2HCl+2Ag 2AgCl↓+H2↑而设计了下列四个实验,你认为可行的是( )
2AgCl↓+H2↑而设计了下列四个实验,你认为可行的是( )
14.在密闭容器中,一定量混合气体发生下列反应: aM(g)+ bN(g) cW(g),达一平衡后,测得M气体的浓度为0.5mol/L。当在恒温下,将密闭容器的体积扩大1倍,再达平衡时,测得M气体的浓度为0.3mol/L。则下列叙述正确的是
( )
cW(g),达一平衡后,测得M气体的浓度为0.5mol/L。当在恒温下,将密闭容器的体积扩大1倍,再达平衡时,测得M气体的浓度为0.3mol/L。则下列叙述正确的是
( )
A.反应速率增大 B.平衡向正反应方向移动
C.N的转化率提高 D.W的体积分数降低
13.一定条件下的可逆反应:2SO2(g) + O2(g) 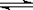 2SO3(g),若改变下列条件,可提高反应物中的活化分子百分数的是( )
2SO3(g),若改变下列条件,可提高反应物中的活化分子百分数的是( )
A.升高温度 B.加催化剂 C.增大压强 D.增大反应物浓度
12.某同学在实验报告中记录下列数据,其中正确的:( )
A.用 25mL 量筒量取 18.63mL 盐酸
B.用托盘天平称取 12.15克食盐
C.用标准的 NaOH 溶液滴定未知浓度的盐酸,用去 NaOH 溶液32.30mL
D.用 pH 试纸测得某溶液 pH 为 5.5
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com