
题目列表(包括答案和解析)
3.已知化合物A的结构简式为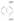 ,A的n溴代物的同分异构体的数目和m溴代物的同分异构体的数目相等,则n和m一定满足的关系式是( )。
,A的n溴代物的同分异构体的数目和m溴代物的同分异构体的数目相等,则n和m一定满足的关系式是( )。
A.n+m=6 B.n=m C.2n=m D.n+m=8
答案:A
2.合成有机玻璃的单体是甲基丙烯酸甲酯(CH2=C-COOH3),此单体不能发生的反应是( )。
|
CH3
A.加聚 B.酯化 C.氧化 D.水解
答案:B
1.现在大量使用的塑料,如聚苯乙烯,因为难以分解而造成严重的“白色污染”,铁道部下令全国铁路餐车停止使用聚苯乙烯制造的餐具,改用降解塑料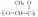 。该塑料在乳酸菌作用下能迅速分解为无毒物质,下列有关降解塑料的叙述正确的是( )。
。该塑料在乳酸菌作用下能迅速分解为无毒物质,下列有关降解塑料的叙述正确的是( )。
A.降解塑料是一种纯净物 B.其相对分子质量为72
C.它是经缩聚反应生成的 D.其单体是CH3CH(OH)COOH
答案:CD
27.(15分) 生物质能是一种洁净、可再生的能源。生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一。
生物质能是一种洁净、可再生的能源。生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一。
 (1)上述反应的催化剂含有Cu、Zn、Al等元素。
(1)上述反应的催化剂含有Cu、Zn、Al等元素。
① 写出基态Cu原子的核外电子排布式 。
② 金属铜采用下列 (填字母代号)堆积方式。
A.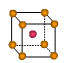 B.
B.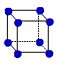 C.
C.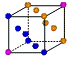 D.
D.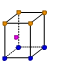
 (2)根据等电子原理,写出CO分子的结构式
。
(2)根据等电子原理,写出CO分子的结构式
。
 (3)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。
(3)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。
 ① 甲醇的沸点比甲醛的高,其主要原因是
;甲醛分子中碳原子轨道的杂化类型为
杂化。
① 甲醇的沸点比甲醛的高,其主要原因是
;甲醛分子中碳原子轨道的杂化类型为
杂化。
 ② 甲醛分子的空间构型是
;
② 甲醛分子的空间构型是
;
1mol甲醛分子中σ键的数目为 。
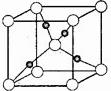
 ③ 在1个Cu2O晶胞中(结构如图所示),所包含的
③ 在1个Cu2O晶胞中(结构如图所示),所包含的
Cu原子数目为 。
(4)科学家通过X射线推测胆矾中既含有配位键,又含有氢键。其结构示意图可简单表示如下,其中配位键和氢键均采用虚线表示。
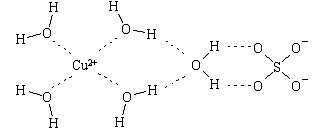
①写出胆矾晶体中水合铜离子的结构简式(必须将配位键表示出来): 。
②水分子间存在氢键,请你列举两点事实说明氢键对水的性质的影响 、 。
26.(11分)已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素的氢化物的沸点高。E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,三个氯离子位于外界。请根据以上情况,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为 。
(2)A的氢化物的分子空间构型是 ;其中心原子采取 杂化。
(3)写出化合物AC2的路易斯结构式 ;一种由B、C组成的化合物与AC2互为等电子体,其化学式为 。
(4)写出E原子的价层电子的轨道表示式是 ,
ECl3形成的配合物的化学式为 。
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反应的化学方程式是 。
25. (11分)下表为长式周期表的一部分,其中的编号代表对应的元素。
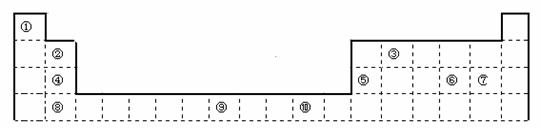
请回答下列问题:
(1)表中属于d区的元素是 (填编号)。
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为 ;③和⑦形成的常见化合物的晶体类型是 。
(3)某元素的特征电子排布式为nsn npn+1,该元素原子的核外最外层电子的孤对电子数为 ;该元素与元素①形成的分子X的空间构型为 。
(4)某些不同族元素的性质也有一定的相似性,如上表中元素⑤与元素②的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式: 。
(5)1183 K以下⑨元素形成的晶体的基本结构单元如图1所示,1183 K以上转变为图2所示结构的基本结构单元,在两种晶体中最邻近的原子间距离相同。
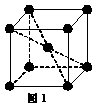
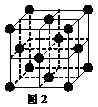
在1183 K以下的晶体中,与⑨原子等距离且最近的⑨原子数为 个,在1183 K以上的晶体中,与⑨原子等距离且最近的⑨原子数为 , 转变温度前后两者的密度比(1183 K以下与1183 K以上之比) (用根号表示)。
24.(5分)某烃类化合物A的相对分子质量为84,分子中含有一个碳碳双键,其分子中只有一种类型的氢原子。
(1)A的分子式为 ,该分子式属于烯烃的同分异构体有 种;
(2)A的结构简式为 ,名称为 ;
(3)A中的碳原子是否都处于同一平面? (填“是”或者“不是”)。
23.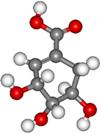 (8分)莽草酸的分子结构模型如图所示(分子中只有C、H、O三种原子)。请回答下列问题:
(8分)莽草酸的分子结构模型如图所示(分子中只有C、H、O三种原子)。请回答下列问题:
(1)观察图中分子结构模型,写出莽草酸的结构简式,并用*表示出手性碳原子:
(2)写出莽草酸分子中包含的官能团的名称 。
22. (7分)分子式为C7H6O3的芳香族化合物,
(1)写出苯环上有两个侧链的异构体的结构简式并命名(有几种写几种)
;
(2)苯环上有三个侧链的异构体共有 种。
21.(3分)碳正离子(例如:CH3+、CH5+、(CH3)3C+等)是有机反应中重要的中间体,欧拉因在此领域研究中的卓越成就而荣获1994年诺贝尔化学奖。碳正离子CH5+ 可以通过CH4在“超强酸”中获得一个H+而得到,而CH5+失去H2可得CH3+。
(1)CH3+是反应性很强的正离子,是缺电子的,其电子式是 ;
(2)CH3+的空间构型是 ;
(3)CH3+中的C原子的杂化方式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com