
题目列表(包括答案和解析)
20.一定条件下将2mol SO2和2mol SO3气体混合于一固定容积的容器中,发生反应:
2SO2+O2 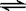 2SO3,平衡时SO3为n mol,在相同温度下,分别按下列配比在上述容器中放入起始物质,平衡时SO3的物质的量可能大于n的是( )
2SO3,平衡时SO3为n mol,在相同温度下,分别按下列配比在上述容器中放入起始物质,平衡时SO3的物质的量可能大于n的是( )
A.2 mol SO2 + 1 mol O2
B.1mol SO2 + 1 mol O2
C.2 mol SO2 + 1 mol O2 + 2 mol SO3
D.1 mol SO2 + 2 mol SO3
第Ⅱ卷(非选择题,共40分)
19.化学反应可视为旧键断裂和新键形成的过程。共价键的键能是两种原子间形成1mol共价键(或其逆过程)时释放(或吸收)的能量。已知H─H键的键能为436kJ/mol,Cl─Cl键的键能为243kJ/mol,H─Cl键的键能为431kJ/mol,则H2(g)+Cl2(g)=2HCl(g)的反应热(△H)等于( )
A.-183 kJ/mol B. 183 kJ/mol C. -862 kJ/mol D. 862 kJ/mol
18. 体积相同的甲、乙两个容器中,分别都充有等物质的量的SO2和O2,在相同温度下发生反应:2SO2+O2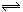 2SO3,并达到平衡。在这过程中,甲容器保持压强不变,乙容器保持体积不变,若甲容器中SO2的转化率为P%,则乙容器中SO2的转化率 ( )
2SO3,并达到平衡。在这过程中,甲容器保持压强不变,乙容器保持体积不变,若甲容器中SO2的转化率为P%,则乙容器中SO2的转化率 ( )
A.等于P% B.小于P% C.大于P% D.无法判断
17. 在两个恒容容器中有平衡体系:A(g) 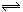 2B(g)和2C(g)
2B(g)和2C(g) 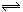 D(g),X1和X2分别是A和C的转化率。在温度不变情况下,均增加相同的A和C的物质的量,下列判断正确的是: ( )
D(g),X1和X2分别是A和C的转化率。在温度不变情况下,均增加相同的A和C的物质的量,下列判断正确的是: ( )
A.X1降低,X2增大 B.X1、X2均降低 C.X1增大,X2降低 D.X1、X2均增大
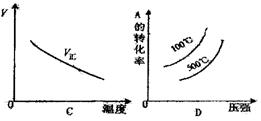
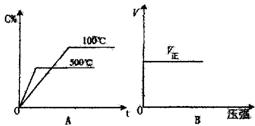
16. 下列各图中能表示A(g)+B(g)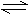 2C(g)(正反应放热)这个可逆反应的图像为( )
2C(g)(正反应放热)这个可逆反应的图像为( )
15.下列热化学方程式中,△H能正确表示物质的燃烧热的是 ( )
A.CO(g) +1/2O2(g) ==CO2(g); △H=-283.0 kJ/mol
B C(s) +1/2O2(g) ==CO(g); △H=-110.5 kJ/mol
C. H2(g) +1/2O2(g)==H2O(g); △H=-241.8 kJ/mol
D.2C8H18(l) +25O2(g)==16CO2(g)+18H2O(l); △H=-11036 kJ/mol
14. 已知热化学反应方程式:
Zn(s)+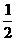 O2(g)
O2(g) ZnO(s);ΔH=-351.5 kJ·mol-1
ZnO(s);ΔH=-351.5 kJ·mol-1
Hg(l)+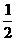 O2(g)
O2(g)  HgO(s);ΔH=-90.84 kJ·mol-1
HgO(s);ΔH=-90.84 kJ·mol-1
则锌汞电池中热化学反应方程式:Zn(s)+HgO(s)  ZnO(s)+Hg(l)的ΔH为
ZnO(s)+Hg(l)的ΔH为
A. ΔH =+260.7 kJ·mol-1 B. ΔH =-260.7 kJ·mol-1
C. ΔH =-444.2 kJ·mol-1 D. ΔH =+444.2 kJ·mol-1
13. 在容积可变的密闭容器中存在如下反应: A(g)+3B(g) 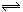 2C(g) 该反应正反应为放热反应。某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:下列判断一定错误的是( )
2C(g) 该反应正反应为放热反应。某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:下列判断一定错误的是( )
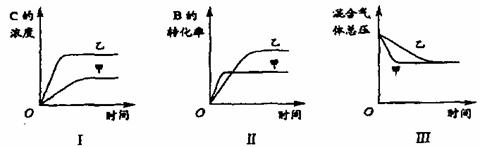
A.图Ⅱ研究的是温度对反应的影响,且甲的温度较高
B.图Ⅲ研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较高
C.图I研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高
D.图I研究的是压强对反应的影响,且乙的压强较高.
12. 热化学方程式C(s)+H2O(g)  CO(g)+H2(g);△H =+131.3kJ/mol表示( )
CO(g)+H2(g);△H =+131.3kJ/mol表示( )
A.碳和水反应吸收131.3kJ能量
B.1mol碳和1mol水反应生成一氧化碳和氢气并吸收131.3kJ热量
C.1mol固态碳和1mol水蒸气反应生成一氧化碳气体和氢气,并吸热131.3kJ
D.1个固态碳原子和1分子水蒸气反应吸热131.1Kj
11. 一定温度下,在容积一定的容器中,可逆反应A(s)+3B(g) 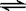 3C(g)达到平衡的标志是( )
3C(g)达到平衡的标志是( )
A.容器内每减少1mol A,同时生成3mol C
B.容器内每减少1mol A,同时消耗3mol B
C.混合气体总的物质的量不变
D.容器内的气体密度不再改变
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com