
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
23ЁЂ(12Зж)ФГвЛЗДгІЬхЯЕгаЗДгІЮяКЭЩњГЩЮяЙВЮхжжЮяжЪЃКO2ЁЁ .H2CrO4. Cr(OH)3.ЁЁ H2O H2O2вбжЊИУЗДгІжаH2O2жЛЗЂЩњЗДгІЙ§ГЬ: H2O2ЁњO2
(1)ЁЂИУЗДгІЕФЛЙдМСЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
(2)ЁЂИУЗДгІЕФбѕЛЏЙ§ГЬЪЧЁЁЁЁЁЁ ЁЁЁЁЁњ ЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁ (3)ЁЂаДГіЗДгІЕФЛЏбЇЗНГЬЪНВЂБъУїЕчзгзЊвЦЕФЗНЯђКЭЪ§ФП
ЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁ
(4)ЁЂШчЙћЗДгІзЊвЦСЫ0.3ФІЕчзгЃЌдђВњЩњЕФЦјЬхдкБъПіЯТЕФЬхЛ§ЪЧЁЁЁЁЁЁ Щ§ЁЃ
ЁЁ
22ЁЂ(8Зж)вбжЊ:H+(aq)+OH-(aq) H2O(l);ІЄH=-57.3 kJЁЄmol-1ЃЌМЦЫуЯТСажаКЭЗДгІжаЗХГіЕФШШСПЁЃ
H2O(l);ІЄH=-57.3 kJЁЄmol-1ЃЌМЦЫуЯТСажаКЭЗДгІжаЗХГіЕФШШСПЁЃ
(1)гУ20 g NaOHХфГЩЯЁШмвКИњзуСПЕФЯЁбЮЫсЗДгІЃЌФмЗХГіЁЁЁЁЁЁЁЁ kJЕФШШСПЁЃ
(2)гУ0.1 mol Ba(OH)2ХфГЩЯЁШмвКИњзуСПЕФЯЁЯѕЫсЗДгІЃЌФмЗХГіЁЁЁЁЁЁЁЁЁЁ kJЕФШШСПЁЃ
(3)гУ1.00 L 1.00 molЁЄL-1ДзЫсШмвКгы2.00 L 1.00 molЁЄL-1 NaOHШмвКЗДгІЃЌЗХГіЕФ
ШШСП(ЬюДѓгкЁЂаЁгкЛђЕШгк)ЁЁЁЁЁЁЁЁЁЁ 57.3 kJРэгЩЪЧЃК
ЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
21ЁЂ(10Зж)ДПМюжаГЃКЌгаЩйСПЕФNaClЕШдгжЪЃЌЯТЭМвЧЦїзАжУПЩгУРДВтЖЈДПМюжаNa2CO3ЕФжЪСПЗжЪ§ЁЃЁЁ
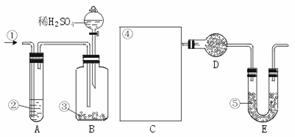
ЭМжаЃКЂйПеЦјЂкФГШмвКЂлДПМюЂмФГШмвКЂнМюЪЏЛв(зЂЃКМюЪЏЛвМШФмЮќЪеCO2ЃЌгжФмЮќ
H2OЁЃЦфЪЕбщВНжшЪЧЃКaЃЎАДЩЯЭМЫљЪОЃЌзщзАКУЪЕбщвЧЦїЃЌВЂМьВщЦфЦјУмадЁЃbЃЎзМШЗГЦСПЪЂгаМюЪЏЛвЕФИЩдяЙмDЕФжЪСП(ЩшЮЊm1 g)ЁЃcЃЎзМШЗГЦСПвЛЖЈСПЕФДПМю(ЩшЮЊn g)ЃЌВЂНЋЦфЗХШыЙуПкЦПФкЁЃdЃЎДгЗжвКТЉЖЗжаЛКТ§ЕЮШывЛЖЈСПЕФЯЁСђЫсЃЌВЂДгЁА1ЁБДІЛКТ§ЙФШыПеЦјЃЌжБЕНBШнЦїжаВЛдйВњЩњЦјЬхЮЊжЙЁЃeЃЎзМШЗГЦСПИЩдяЙмDЕФзмжЪСП(ЩшЮЊm2 g)ЁЃ
ИљОнЩЯЪіЪЕбщЛиД№ЯТСаЮЪЬтЃКЁЁ
(1)ИУЪЕбщНјааЕНВйзїdЪБЃЌвЊЛКЛКЙФШыПеЦјЃЌЦфзїгУЪЧ____________________ ЁЃзА
жУAжаЪЂзАЕФвКЬхЁА2ЁБгІбЁгУ________________ЃЌзАжУAЕФзїгУЪЧ________________ЃЌ
ШчЙћГЗШЅзАжУAЃЌжБНгЯђBжаЛКЛКЙФШыПеЦјЃЌдђЛсЕМжТЪЕбщВтЖЈНсЙћ(ЬюЁАЦЋДѓЁБЁАЦЋ
аЁЁБЛђЁАВЛБфЁБ)________________ЁЃЁЁ
(2)дкПеАзИёФкЛГізАжУCМАЪдМСЂмЪЧ__________ ЃЛзАжУCЕФзїгУЪЧ
________________ЃЛШчЙћГЗШЅзАжУCЃЌдђЛсЕМжТВтЖЈНсЙћ________________(ЬюЁАЦЋДѓЁБЁАЦЋЁЁ аЁЁБЛђЁАВЛБфЁБ)ЁЁ
(3)ИљОнДЫЪЕбщЃЌМЦЫуДПМюжаNa2CO3ЕФжЪСПЗжЪ§ЕФЪ§бЇЪНЮЊ________________
(гУm1ЁЂm2ЁЂnБэЪО)ЁЁ
(4)зАжУEЕФзїгУЪЧ________________________ЁЃЁЁ
20ЁЂвдЯТИїжжЮВЦјЮќЪезАжУжаЃЌЪЪКЯгкЮќЪевзШмадЦјЬхЃЌЖјЧвФмЗРжЙЕЙЮќЕФЪЧ(ЁЁ )
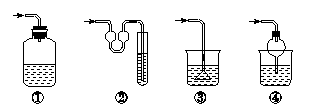 ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЁЁA.ЂкЂмЁЁЁЁЁЁЁЁЁЁЁЁ B.ЂйЂкЁЁЁЁЁЁЁЁЁЁЁЁ C.ЂйЂлЁЁЁЁЁЁЁЁЁЁЁЁ D.ЂлЂм
АрМЖЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁаеУћЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЗжЪ§ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЂђОэ(40Зж)
19ЁЂФмЙЛжЄУївЛжжНКСЃЪЧДје§ЕчКЩЛЙЪЧДјИКЕчКЩЕФЪЕбщЪЧ()
A.ЖЁДяЖћЯжЯѓЪЕбщЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ B.ЕчгОЪЕбщ
C.ЩјЮіЪЕбщЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ D.МгШШЪЙНКЬхОлГСЪЕбщ
18ЁЂЯТСажЦБИЗНЗЈКЭЯжЯѓЖМе§ШЗЕФЪЧ(ЁЁ )
A.ШЁаТжЦFeSO4ШмвКзЂШыЪдЙмЃЌдйЯђЪдЙмжаЕЮМгNaOHШмвКЃЌСЂМДгаАзЩЋГСЕэЩњГЩ
B.ЭљБНЗгШмвКжаЕЮМгМИЕЮХЈфхЫЎЪБЃЌгаАзЩЋГСЕэЮіГі
C.ЯђЪЂга0.01 molЁЄL-1 KIШмвКЕФЪдЙмжаЕЮМгЯрЭЌХЈЖШЕФAgNO3ШмвКЃЌБпЕЮБпеёЕДЃЌПЩЕУЕНЧГЛЦЩЋЕФAgIНКЬх
D.ЕэЗлгыЯЁH2SO4ЙВжѓКѓЃЌМгШыаТжЦCu(OH)2дйМгШШЃЌгаКьЩЋГСЕэЩњГЩ
17ЁЂвбжЊI-ЁЂFe2+ЁЂSO2ЁЂCl-КЭH2O2ОљгаЛЙдадЃЌЫќУЧдкЫсадШмвКжаЛЙдадЕФЧПШѕЫГађЮЊH2O2ЃМCl-ЃМFe2+ЃМI-ЃМSO2ЃЌдђЯТСаЗДгІВЛФмЗЂЩњЕФЪЧЁ(ЁЁ )
A.2Fe3++SO2+2H2O 2Fe2++
2Fe2++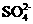 +4H+ ЁЁЁЁЁЁB.I2+2H2O+SO2
+4H+ ЁЁЁЁЁЁB.I2+2H2O+SO2 H2SO4+2HI
H2SO4+2HI
C.H2O2+H2SO4 SO2+O2Ёќ+2H2OЁЁЁЁ D.2Fe3++2I-
SO2+O2Ёќ+2H2OЁЁЁЁ D.2Fe3++2I- 2Fe2++I2
2Fe2++I2
16ЁЂНгДЅЗЈжЦСђЫсЕФЗаЬкТЏГіРДЕФТЏЦјБиаыОЙ§ОЛЛЏДІРэЃЌЦфе§ШЗЙ§ГЬЪЧЁЁЁЁ (ЁЁЁЁ )
ЁЁ AЃЎЯДЕгЁЂИЩдяЁЂГ§ГОЁЁЁЁ BЃЎИЩдяЁЂГ§ГОЁЂЯДЕг
ЁЁ CЃЎГ§ГОЁЂЯДЕгЁЂИЩдяЁЁЁЁ DЃЎГ§ШЅЮјКЭЩщЕФЛЏКЯЮяЁЁ
15ЁЂвбжЊШШЛЏбЇЗДгІЗНГЬЪНЃКZn(s)+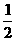 O2(g)
O2(g) ZnO(s);ІЄH=-351.5 kJЁЄmol-1;
ZnO(s);ІЄH=-351.5 kJЁЄmol-1;
Hg(l)+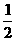 O2(g)
O2(g)  HgO(s);ІЄH=-90.84 kJЁЄmol-1ЃЌдђаПЙЏЕчГижаШШЛЏбЇЗДгІЗНГЬЪНЃКZn(s)+HgO(s)
HgO(s);ІЄH=-90.84 kJЁЄmol-1ЃЌдђаПЙЏЕчГижаШШЛЏбЇЗДгІЗНГЬЪНЃКZn(s)+HgO(s)  ZnO(s)+Hg(l)ЕФІЄHЮЊ(ЁЁ )
ZnO(s)+Hg(l)ЕФІЄHЮЊ(ЁЁ )
A.ЁЂІЄH=+260.7 kJЁЄmol-1ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЁЂ.ІЄH=-260.7 kJЁЄmol-1
ЁЁCЁЂ.ІЄH=-444.2 kJЁЄmol-1ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ D.ЁЂІЄH=+444.2 kJЁЄmol-1
ЁЁ
14ЁЂНЋвЛЖЈСПЕФФЦЁЂТСКЯН№жУгкЫЎжаЃЌКЯН№ШЋВПШмНтЃЌЕУЕН20mlЁЂpH=14ЕФШмвК.ШЛКѓгУ1mol/LЕФбЮЫсЕЮЖЈжСГСЕэСПзюДѓЪБЃЌЯћКФбЮЫс40mlЁЃдКЯН№жаФЦЕФжЪСПЮЊЁЁЁЁЁЁЁЁЁЁ
ЁЁЁЁЁЁ AЃЎ0.92g ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ BЃЎ0.69gЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ CЃЎ0.64gЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎ0.23g
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com