
31.(8分)[化学--化学与技术]
往有机聚合物中添加阻燃剂,可增加聚合物的使用安全性,扩大其应用范围。例如,在某聚乙烯树脂中加入等质量由特殊工艺制备的阻燃型Mg(OH)2,树脂可燃性大大降低。该Mg(OH)2的生产工艺如下:







 → 合成 → 水热处理 → 过滤 → 水洗 → 表面处理 → 过滤水洗 → 干燥
→ 合成 → 水热处理 → 过滤 → 水洗 → 表面处理 → 过滤水洗 → 干燥
(1)精制卤水中的MgCl2与适量石灰乳反应合成碱式氯化镁[Mg(OH)2-xClx ·mH2O],反应的化学方程式为
__________________________________________________。
(2)合成反应后,继续在393K-523K下水热处理8h,发生反应:
[Mg(OH)2-xClx·mH2O]=(1-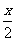 )Mg(OH)2+
)Mg(OH)2+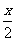 MgCl2+mH2O
MgCl2+mH2O
水热处理后,过滤、水洗。水洗的目的是 。
(3)已知热化学方程式:
Mg(OH)2(s)=MgO(s)+H2O(g) △H1=+81.5kJ·mol-1
Al(OH)3(s)=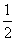 Al2O3(s)+
Al2O3(s)+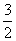 H2O(g) △H2=+87.7kJ·mol-1
H2O(g) △H2=+87.7kJ·mol-1
①Mg(OH)2和Al(OH)3起阻燃作用的主要原因是 。
②等质量Mg(OH)2和Al(OH)3相比,阻燃效果较好的是 ,原因是 。
(4)常用阻燃剂主要有三类:A.卤系,如四溴乙烷;B.磷系,如磷酸三苯酯;C.无机类,主要是Mg(OH)2和l(OH)3。从环保的角度考虑,应用时较理想的阻燃剂是 (填代号)。
30.(13分)短周期的四种元素A、B、C、D,原子序数依次增大。A、B、C三种元素原子核外电子层数之和是5,A、B两元素原子最外电子层上电子数之和等于C元素原子最外电子层上的电子数,B元素原子最外电子层上的电子数是它的电子层数的2倍,A和C可以形成化合物CA3,B与D的原子序数之比为3:4。
请回答:
(1)写出化合物CA3的电子式: 。
(2)由四种元素中的三种组成的甲、乙两种化合物,甲属于盐类,其溶液呈酸性,请用离子方程式表示其溶液呈酸性的原因
乙为常见的天然高分子化合物,写出该高分子化合物充分水解的化学方程式:
(3)丙、丁两种化合物,它们均含上述四种元素,既可以与盐酸反应又可以与NaOH溶溶液反应,丙为无机盐,其化学式为 ,丁为有机物,且是同类有机物中相对分子质量最小的,其结构简式为 。
(4)A和B组成的化合物M,分子中A与B的原子个数比是3:1,常温常压下,0.5mol M完全燃烧放出780kJ的热量,请写出表示M燃烧热的热化学方程式:
[选做部分]
共8个题,考生从中选择2个物理题、1个化学题和1个生物题作答。
29.(17分)大气为地球上各种生物的生存提供了条件。但是,随着工业和交通运输迅速发展,城市人口高度集中,人类向大气中大量排放烟尘和有害气体等,正在对大气造成污染。我国某工业城市的“空气质量日报”显示,该城市的空气受到一定程度的污染。某研究性学习小组对该城市的空气污染进行了下列研究:
(1)小组内一同学初步分析得出,该城市空气污染的主要原因有三个:A.使用石油液化气 B.燃烧含硫煤 C.粉尘污染。另一同学认为还有一个不可排除的原因是:D.
研究性学习小组就造成该城市空气污染的最主要原因调查了该市100名市民和100位环保部门人士。调查结果如下图所示:
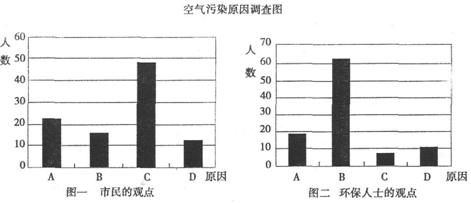
从环保人士的观点上分析,你认为造成该城市空气污染的主要有害成分是 (用化学式表示)。
(2)空气污染易形成酸雨。研究性学习小组对该城市的雨水进行了采样与分析,刚采集时测得pH为4.82,放在烧杯中经2h后,再次测得pH为4.68。对此,你的合理解释是
(3)研究性学习小组同学取空气(含氮气、氧气、二氧化碳、二氧化硫等)10.0L(已折算成标准状况),缓慢通过足量溴水,在所得溶液中加入过量的氯化钡溶液,产生白色沉淀,将沉淀洗涤、干燥,称得其质量为0.0233g。试回答该白色沉淀的化学式为 ,通过计算得该空气中主要有害气体成分的体积分数为 。
(4)该小组同学提出下列措施以减少空气污染的主要有害成分排放量,你认为合理的是 (填序号)。
①用天然气代替煤炭作民用燃料 ②改进燃煤技术,减少煤的用量 ③工厂生产时将燃煤锅炉的烟囱造得更高 ④燃煤中加入适量石灰石后使用
(5)在容积均为1L(容积不可变)的甲、乙两个容器中,分别加入2molSO2、1molO2和4mol SO2、2 mol O2,在相同温度、催化剂下使其反应。最终达到平衡后,两容器中SO2转化率分别为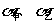 ,甲容器中平衡常数表达式为
,此时
,甲容器中平衡常数表达式为
,此时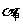
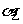 (填“大于”、“小于”或“等于”)。
(填“大于”、“小于”或“等于”)。
28.(12分)化学几乎渗透于所有的行业,在考古工作中,化学就起着不可替代的作用。
(1)古墓中,石灰岩(主要成分CaCO3)上绘制的壁画在潮湿的条件下往往覆盖了一层白色薄膜,经测定为CaCO3,用化学反应方程式表示生成CaCO3的过程:
(2)古画颜料中的铅白[Pb2(OH)2CO3]由于受空气中硫化氢气体的作用而变成溶解度极小的黑色硫化铅(反应I),影响画面的色泽,当用过氧化氢处理后,可使硫化铅变成白色的物质(反应Ⅱ)。据此回答下列问题:
①铅白中铅元素的化合价呈 价。
②反应Ⅱ中生成的白色物质的化学式为 。
③反应I的化学反应方程式 。
(3)古代铁器(埋藏在地下)在严重缺氧的环境中,仍然锈蚀严重(电化腐蚀)。原因是一种叫做硫酸盐还原菌的细菌,能提供正极反应的催化剂,可将土壤中的SO42-还原为S2-,该反应放出的能量供给细菌生长、繁殖之需。
①写出该电化腐蚀的正极反应的电极反应 。
②文物出土前,铁器表面的腐蚀产物可能有(写化学式) 。
15.下列溶液中有关微粒的物质的量浓度关系正确的是
A.NaHSO3和NaHCO3的中性混合溶液中(S和C均用R表示):c(Na+)=c(HRO3-)+2c(RO32-)
B.常温下将醋酸钠、盐酸两溶液混合后,溶液呈中性,则混合后溶液中:c(Na+)>c(Cl-)>c(CH3COOH)
C.常温下物质的量浓度相等的①(NH4)2CO3、②(NH4)2SO4、③NH4HSO4三种溶液中c(NH4+):①<②<③
D.相同条件下,pH=5的①NH4Cl溶液、②CH3COOH溶液、③稀盐酸溶液中由水电离出的c(H+):①>②>③
第Ⅱ卷(必做120分+选做32分,共152分)
[必做部分]
14.下列离子方程式正确的是
A.碳酸氢钠溶液与少量石灰水反应:HCO3-+Ca2++OH-=CaCO3↓+H2O
B.氯化铵与氢氧化钠两种浓溶液混合加热:NH4++OH- H2O+NH3↑
H2O+NH3↑
C.实验室制Fe(OH)3胶体:Fe3++3OH-=Fe(OH)3(胶体)
D.次氯酸钙溶液中通人少量SO2气体:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO
13.已知25℃时,电离常数Ka(HF)=3.6×10-4mol/L,溶度积常数Ksp(CaF2)=1.46×10-10mol3/L3。现向1L 0.2mol/L HF溶液中加入1L0.2mol/L CaCl2溶液,则下列说法中,正确的是
A.25℃时,0.1mol/L HF溶液中pH=1
B.Ksp(CaF2)随温度和浓度的变化而变化
C.该体系中,Ksp(CaF2)=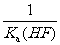
D.该体系中有CaF2沉淀产生
12.用NA表示阿伏加德罗常数的值,下列说法中不正确的是
A 7.8g Na2O2与足量潮湿的CO2反应,转移的电子数为0.1NA
B.常温常压下,20g D2O和足量的金属钠反应产生气体的分子数为NA
C.室温下,42.0g乙烯和丙烯的混合气体中含有的碳原子数为3NA
D.4.4g由N2O和CO2组成的混合气体含0.3NA个原子
11.长征2号火箭承担运载“神六”的使命。氢化锂、氘化锂、氚化锂可以作为起动长征2号火箭(CZ2F)发射的动力源,下列说法正确的是
A.等物质的量的LiH、LiD、LiT中所含质子数不相同
B.它们都是氧化剂
C.H、D、T之间互称同素异形体
D.它们都是强还原剂
10.下列各组离子在溶液中能大量共存,当溶液呈强酸性时,有气体产生;而当溶液呈强碱性时,又能生成沉淀。该组离子可能是
A.Na+、Cu2+、NO3-、CO32- B.NH4+、K+、Cl-、HCO3-
C.Mg2+、NH4+、SO42-、Cl- D.Fe2+、Na+、SO42-、NO3-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com